14. Tumeurs appendiculaires (hors TNE)
(Dernière mise à jour le : )Groupe de travail et relecteurs
Groupe de travail :
Cécile Brigand (Strasbourg), coordonnateur,
Gerlinde Averous (Strasbourg), Anthony Dohan (Paris), François Quenet (Montpellier), Laurent Villeneuve (Lyon), Benoit You (Lyon).
Relecteurs :
Frédéric Bibeau (Besançon ; RENAPATH), Olivier Bouché (Reims ; COPIL TNCD), Sébastien Gaujoux (Paris ; COPIL TNCD), Olivier Glehen (Lyon ; RENAPE), Thierry Lecomte (Tours ; COPIL TNCD), Pascale Mariani (Paris ; COPIL TNCD), Pierre Michel (Rouen ; FFCD), Marc Pocard (Paris ; RENAPE), Emmanuelle Samalin (Montpellier ; UNICANCER), Philippe Soyer (Paris ; SFR), Jean-Jacques Tuech (Rouen ; RENAPE), Thomas Walter (Lyon ; RENATEN).
Relecteurs regionaux :
Karine Abboud (Saint Etienne), Koceila Amroun (Reims), Bogdan Badic (Brest), Bachir Elias (Thionville), Cécilia Frasconi (Marseille), Pierre Guillet (Toulon), Dine Koriche (Béthune, Lens), Jean-Pierre Machayekh (Guilherand-Granges), Frédéric Marchal (Vandoeuvre Les Nancy), Pierre Meeus (Lyon), Jean-François Paitel (Saint-Raphaël), Guillaume Passot (Lyon), Pierre-Guillaume Poureau (Brest), Charles Sabbagh (Amiens), Alexis Vinet (Châteauroux)
Comment citer ce chapitre du TNCD ?
Delhorme JB, Villeneuve L, Bouché O, Averous G, Dohan A, Gornet JM, You B, Bibeau F, Dartigues P, Eveno C, Fontaine J, Kepenekian V, Pocard M, Rousset P, Quenet F, Mariani P, Glehen O, Goéré D. Appendiceal tumors and pseudomyxoma peritonei: French Intergroup Clinical Practice Guidelines for diagnosis, treatments and follow-up (RENAPE, RENAPATH, SNFGE, FFCD, GERCOR, UNICANCER, SFCD, SFED, SFRO, ACHBT, SFR). Dig Liver Dis. 2022 Jan;54(1):30-39.
14.1. Introduction, méthodologie et classifications à utiliser
14.1.1. Introduction
Ce texte est consacré aux tumeurs épithéliales appendiculaires, hors néoplasies neuroendocrines (NNE), qui font l’objet du chapitre 11 du TNCD. Cependant, le « goblet cell carcinoma », non traité dans ce chapitre NNE, sera traité dans ce chapitre 14.
Les tumeurs épithéliales appendiculaires sont rares, présentes sur 2% des pièces d’appendicectomie, mais représentent une large gamme d’entités clinico-pathologiques avec plusieurs systèmes de classification pathologiques et des comportements biologiques différents. La majorité des tumeurs découvertes sur pièce d'appendicectomie sont des NNE (95%).
Ainsi, les modalités de traitement varient selon le type histologique et le stade de la maladie. Celles-ci peuvent varier de la simple appendicectomie par cœlioscopie à la chirurgie de cytoréduction complète (CCR) avec chimiothérapie hyperthermique intrapéritonéale (CHIP) et/ou chimiothérapie systémique.
Compte tenu de la rareté de certaines situations, la décision de la stratégie thérapeutique, adaptée à chaque patient, nécessite un bilan pré-thérapeutique spécialisé, un examen clinique par un chirurgien spécialisé dans la prise en charge des tumeurs rares du péritoine et une discussion en réunion de concertation pluridisciplinaire (RCP) spécialisée, RCP RENAPE (Réseau National de prise en charge des Tumeurs Rares du Péritoine), mise en place dans les centres de référence appartenant à ce réseau. http://www.renape-online.fr/fr/centres.html
Un chirurgien non spécialisé dans la prise en charge de ces tumeurs rares ne sera confronté à ces entités qu’une à deux fois dans sa carrière, le plus souvent après analyse histo-pathologique de la pièce d’appendicectomie.
Il est donc important de connaitre les modalités de prise en charge des tumeurs appendiculaires, car ces tumeurs sont souvent de stade avancé au moment du diagnostic et les décisions concernant la prise en charge chirurgicale peuvent avoir des effets importants sur la survie de ces patients (risque de résection inadaptée R1 voire R2).
Les tumeurs épithéliales appendiculaires peuvent être responsables de mucocèle appendiculaires (MA) ; définie comme une distension progressive de l’appendice, d’origine obstructive, par accumulation intra-luminale de matériel mucoïde. Les tumeurs épithéliales appendiculaires, incluant celles avec un potentiel de malignité incertain et les adénocarcinomes, sont connues pour leur capacité à produire du mucus et donc, appartiennent au groupe des tumeurs mucineuses appendiculaires. Certaines, lorsque perforées (de manière spontanée ou iatrogène), sont la cause principale du pseudomyxome péritonéal (PMP), caractérisé par l’accumulation d’ascite et d’implants mucineux dans la cavité péritonéale et d’implants mucineux dans la cavité péritonéale (cf. TNCD chapitre 16. Pseudomyxome péritonéal).
Il n’y a pas d’essai en cours en France concernant les tumeurs épithéliales appendiculaires.
14.1.2. METHODOLOGIE
La méthode d’élaboration de ces recommandations a été faite par un groupe de travail issu du réseau RENAPE, en collaboration avec les experts internationaux du Peritoneal Surface Oncology Group International (PSOGI) ayant récemment établi un consensus sur la prise en charge des tumeurs appendiculaires et pseudomyxomes péritonéaux (Govaerts et al., 2020) et des mésothéliomes péritonéaux (Kusamara et al., 2020). Ces recommandations sont issues de questions évaluées selon la méthode Delphi et le GRADE system a été utilisé pour leur gradation (Lurvink et al., 2019). Ce consensus a impliqué 80 experts internationaux (chirurgiens et oncologues) pour les tumeurs appendiculaires. Un total de 35 questions sur les tumeurs appendiculaires a été soumis au cours du processus Delphi.
Pour chaque chapitre, une recherche exhaustive des données de la littérature a également été effectuée :
- Interrogation en mai 2018 de la base de données Medline® (interface OVID) à l’aide d’équations de recherche. La stratégie de recherche bibliographique a été limitée aux publications en français et en anglais ;
- les types d’études recherchés ont été les suivants : méta-analyses sur données inpiduelles ou publiées, revues systématiques, essais randomisés, essais contrôlés (rétrospectifs ou prospectifs), études prospectives ou rétrospectives non comparatives, recommandations pour la pratique clinique
- Consultation des sites internet pertinents (https://www.e-cancer.fr/, par exemple)
- une sélection des articles pertinents selon des critères prédéfinis sur la base des informations contenues dans les résumés (abstracts) puis la sélection finale a été établie sur la base des textes intégraux ;
- une analyse critique des données scientifiques ainsi sélectionnées permettant d’attribuer un niveau de preuve aux conclusions issues de la littérature.
Le groupe de travail s’est réuni à 2 reprises en février 2018 et en février 2019.
La gradation des présentes recommandations correspond au niveau de preuves disponibles dans la littérature et/ou aux résultats du vote Delphi effectué par les experts du PSOGI, sur lesquelles reposent les conclusions formulées.
En cas de preuves insuffisantes, les présentes recommandations ont été gradées selon l’avis d’experts.
Le mode de présentation retenu pour le TNCD selon 4 niveaux (A, B, C, accord ou avis d’experts) est résumé dans le tableau 1.
Tableau 1
Système de gradation des recommandations utilisé dans ce chapitre
| -GRADE- | -NIVEAU DE PREUVE CORRESPONDANT- |
|---|---|
| -A- | -Recommandation forte basée par exemple sur un/des essai(s) comparatif(s) randomisé(s) de forte puissance, une/des méta-analyse d’essai(s) comparatif(s) randomisé(s), ou une analyse de décision fondée sur des études bien menées.- |
| -B- | -Recommandation basée sur une présomption scientifique à partir d’essais comparatifs randomisés de faible puissance, d’études comparatives non randomisées bien menées ou d’études de cohortes.- |
| -C- | -Recommandation basée sur un faible niveau de preuve à partir d’études cas-témoins, d’études comparatives comportant des biais importants, d’études rétrospectives, de séries de cas, d’études épidémiologiques descriptives (transversale, longitudinale).- |
| -Accord ou Avis d’experts- | -Recommandation basée sur un accord d’experts ou un avis d’experts en l’absence de données suffisantes de la littérature- |
14.1.3. CLASSIFICATIONS
Le consensus du groupe international d’étude des maladies du péritoine (PSOGI) (Carr et al., 2017) classifie les tumeurs appendiculaires en :
- Adénomes : Il s’agit de proliférations épithéliales du revêtement cylindrique de type intestinal similaires aux adénomes colo-rectaux. Ils sont rares dans l’appendice et peuvent comporter des degrés de dysplasie variables parfois de haut grade et représentent des précurseurs des adénocarcinomes de type colorectal.
- Polypes festonnés (adénomes dentelés / serrated adenoma) : Il s’agit de proliférations épithéliales d’aspect « dentelé » avec ou sans dysplasies de bas ou de haut grade et correspondent aux potentiels précurseurs des adénocarcinomes mucineux. Des mutations des gènes KRAS (52%) et beaucoup plus rarement BRAF (4%) ont été décrites.
- Tumeurs appendiculaires mucineuses de bas grade (LAMN) : Il s’agit d’une prolifération d’épithélium cylindrique mucosécrétant très bien différencié, d’architecture plane ou villeuse avec atypies cyto-nucléaires de bas grade, à l’origine d’une distension et souvent d’une rupture appendiculaire sans infiltration destructrice mais avec extension expansive « pushing type » au-delà de la séreuse appendiculaire avec risque de pseudomyxome péritonéal. La LAMN est observée dans 2% des pièces d’appendicectomie.
Sur le plan moléculaire prédominent les mutations de KRAS (100%) dans les codons 12 et 13 (G12D et G12V). Des mutations de GNAS ont été décrites dans 50% des cas (Borazanci et al., 2017).- Diagnostics différentiels : polype / adénome dentelé, endométriose avec métaplasie intestinale (Misdraji et al., 2014), diverticule appendiculaire rompu, appendicite avec hyperplasie de la muqueuse.
- Tumeurs appendiculaires mucineuses de haut grade (HAMN) : Le terme « tumeur mucineuse appendiculaire de haut grade » a récemment été rajouté dans la classification des néoplasies mucineuses, mais ces tumeurs sont extrêmement rares et donc encore peu connues (Legué et al., 2019). Ces lésions ont la même architecture que les tumeurs mucineuses de bas grade mais avec des atypies cytologiques de haut grade. On pourrait considérer les tumeurs mucineuses appendiculaires de haut grade comme un groupe intermédiaire entre les tumeurs mucineuses de bas grade et les adénocarcinomes mucineux (Legué et al., 2019). Il s’agit d’une prolifération de l’épithélium cylindrique mucosécrétant très bien différencié d’architecture plane ou villeuse avec atypies cyto-nucléaires de haut grade sans invasion destructrice, ni extension au-delà de la musculeuse.
L’extension péritonéale des LAMN/HAMN est à l’origine d’un PMP. Le grade histo-pathologique de ces tumeurs dépend d’une part du caractère expansif (bas grade) ou infiltratif (haut grade) et des atypies cyto-nucléaires (de bas ou de haut grade) et d’autre part de la présence ou non de cellules en bague à chaton « signet ring cells ». (Carr et al., 2016)
- Adénocarcinome mucineux (sans ou avec ou à cellules en bague à chaton) : Il s’agit d’un adénocarcinome avec au moins 50% de cellules mucosécrétantes. Les atypies cyto-nuclaires et/ou la présence d’une composante à cellules en bague à chaton (« signet ring cells ») déterminent le grade histologique (voir tableaux). Un adénocarcinome avec une majorité de cellules en bague à chaton (>50%) est appelé adénocarcinome à cellules en bague à chaton.
Les métastases ganglionnaires lymphatiques sont présentes dans 6 % des tumeurs de bas grade contre 20% des tumeurs de haut grade. La survie à 5 ans est de 75-81% dans les tumeurs de bas grade et de 45-65% dans les adénocarcinomes mucineux de haut grade.- Sur le plan moléculaire dans les tumeurs mucineuses prédominent des mutations KRAS (probable mutation driver du PMP) et GNAS, qui semble en rapport avec la production de mucus mais sans lien pronostique (Nishikawa et al., 2013). D’autres mutations comme APC, ATM, PIK3CA, SMAD4, NRAS, TP53 et la voie TGF-β sont également observées, le plus souvent dans les adénocarcinomes (Zhang et al., 2018).
- Immunohistochimie : CK20+, CDX2+, MUC2+ (Carr et al., 2017)
- Adénocarcinome non mucineux (type colorectal) : Il survient dans la 6ème décennie (62-65 ans) et présente un risque important de métastases ganglionnaires lymphatiques et hématogènes, respectivement de 23 et 37%.
- Sur le plan moléculaire, il existe une prédominance des mutations de KRAS (50,4%), p53 (21,9%), GNAS (17,6%) et SMAD4 (16,6%) à côté de mutations des gènes APC (10%), PIK3CA (5,5%) et FBXW (5%). Le profil moléculaire ressemble d’avantage à celui des adénocarcinomes pancréatiques, que colo-rectaux (Zhang et al., 2018).
- Immunohistochimie : CD20+, CDX2+
Tableau 2
Terminologie OMS (2019) versus PSOGI (2016) adoptée par l’AJCC 8ème édition
| Terminologie OMS (2019) | Terminologie PSOGI (2016) |
|---|---|
Lésions précurseurs : adénome conventionnel, adénome/polype dentelé, polype hyperplasique
Néoplasie mucineuse appendiculaire de bas grade (LAMN) - G1 | Lésions non invasives Néoplasie appendiculaire mucineuse de bas grade (LAMN) * – extension « pushing type » jusque dans la musculeuse = pTis Néoplasie appendiculaire mucineuse de bas grade (LAMN) * – extension « pushing type » jusque dans la musculeuse = pTis Néoplasie appendiculaire mucineuse de haut grade (HAMN)* –extension « pushing type » jusque dans la musculeuse = pTis* *La totalité de l’appendice doit être soumis à l’examen histologique |
| Adénocarcinome mucineux >50% mucosécrétion, < 50% de cellules en bague à chaton - G2 Adénocarcinome à cellules en bague à chaton >50 % de cellules en bague à chaton - G3 | Lésions invasives Adénocarcinome mucineux >50% mucosécrétion, < 50% de cellules en bague à chaton Adénocarcinome à cellules en bague à chaton >50 % de cellules en bague à chaton |
| Adénocarcinome non mucineux - type colorectal classique - bas grade ou haut grade | Adénocarcinome non mucineux (type colorectal classique) |
Tableau 3
Stadification selon TNM et AJCC 8ème édition :
Néoplasie mucineuse appendiculaire de bas grade (LAMN) et de haut grade (HAMN)*
| Stade pTNM de la tumeur | Descriptif |
|---|---|
| pTis | Extension « pushing type » jusque dans la musculeuse |
| pT1 et pT2 | Non applicables pour les LAMN / HAMN* |
| pT3 | La tumeur s’étend à travers la musculeuse dans la sous-séreuse ou le méso appendiculaire |
| pT4a | La tumeur pénètre au-delà du péritoine viscéral Ceci comprend des cellules tumorales et/ou du mucus acellulaire (sans cellules tumorales identifiables) |
| pT4b | La tumeur s’étend par contiguïté à d’autres organes dont le péritoine incluant la présence de mucus acellulaire |
| M1a | Mucus intra-péritonéal acellulaire (sans cellules tumorales identifiables) |
| M1b | Métastases intra-péritonéales avec cellules tumorales et implants ± infiltration superficielle d’organes abdomino-pelviens (rate, capsule hépatique, ovaires, intestins, ou autre) |
| M1c | Métastases extra-péritonéales** |
*Ce diagnostic n’est possible qu’après inclusion et analyse histologique de la totalité de l’appendice
** Notamment pleurale ou pulmonaire
Adénocarcinome appendiculaire non mucineux
| STADE PTNM DE LA TUMEUR | DESCRIPTIF |
|---|---|
| pTis | Prolifération imitée à la muqueuse |
| pT1 | Infiltration de la sous-muqueuse |
| pT2 | Infiltration de la musculeuse |
| pT3 | Infiltration de la sous-séreuse |
| pT4a | Extension tumorale au-delà du péritoine viscéral |
| pT4b | Infiltration d’autres organes par contiguïté |
| M1a | Mucus intra-péritonéal acellulaire (sans cellules tumorales identifiables) |
| M1b | Métastases intra-péritonéales avec cellules tumorales et implants ± infiltration superficielle d’organes abdomino-pelviens (rate, capsule hépatique, ovaires, intestins, ou autre…) |
| M1c | Métastases extra-péritonéales |
| Ganglions lymphatiques régionaux (N) | |
|---|---|
| N0 | Pas d'adénopathie régionale métastatique |
| N1 | 1 à 3 adénopathies régionales métastatiques N1a : 1 adénopathie régionale métastatique N1b : 2 à 3 adénopathies régionales métastatiques N1c : résurgences tumorales dans la sous-séreuse ou le tissu adipeux non péritonéalisé sans métastases ganglionnaires lymphatiques |
| N2 | ≥4 adénopathies régionales métastatiques |
| Nx | Pas de ganglion lymphatique analysé |
Tableau 4
Grading des néoplasies mucineuses appendiculaires (AJCC 8ème édition)
| Grade AJCC 8ème édition, OMS 2019 | Caractéristiques | Grade selon Davison et al. (2014) |
|---|---|---|
| G1 bien différencié | Néoplasie mucineuse de bas grade cyto-nucléaire (LAMN) | Bas grade |
| G2 modérément différencié | Haut grade cyto-nucléaire (HAMN et adénocarcinome mucineux) sans cellules en bague à chaton | Haut grade |
| G3 peu différencié | Haut grade cyto-nucléaire avec cellules en bague à chaton |
Tableau 5
Terminologie OMS 2019, AJCC 8ème édition versus PSOGI 2016
(proposition d’une terminologie homogène entre les tumeurs primitives et les localisations péritonéales)
| Tumeur primitive OMS 2019 | Maladie péritonéale Terminologie PSOGI 2016** Métastase péritonéale (OMS 2019) | Néoplasie appendiculaire et péritonéale – Terminologie AJCC 8ème édition |
|---|---|---|
| Néoplasie appendiculaire mucineuse de bas grade (LAMN) | Carcinose mucineuse péritonéale de bas grade | Néoplasie mucineuse de bas grade (G1) |
| HAMN et Adénocarcinome mucineux sans cellules en bague à chaton | Carcinose mucineuse péritonéale de haut grade | Adénocarcinome mucineux modérément différencié (G2) |
| Adénocarcinome mucineux avec ou à cellules en bague à chaton | Carcinose mucineuse péritonéale de haut grade avec cellules en bague à chaton | Adénocarcinome mucineux et/ou à cellules en bague à chaton (G3) |
**Rarement des discordances entre le grade de la tumeur appendiculaire et celui de la localisation péritonéale existent. Le grade de la maladie péritonéale reflète mieux l’évolution clinique et devrait donc être pris en compte pour la prise en charge thérapeutique
- L’atteinte ou l’intégrité de la base appendiculaire doit être précisée. L’encrage de la section proximale peut aider à apprécier cette notion.
- Les critères morphologiques pour la définition du grade histo-pathologique de la carcinose mucineuse incluent le degré d’atypies cyto-nucléaires, le caractère infiltratif ou expansif et la présence ou non de cellules en bague à chaton. L’infiltration destructrice, le grade nucléaire élevé et la présence de cellules en bague à chaton sont en faveur d’un PMP de haut grade.
- Le PMP est rarement d’origine extra-appendiculaire. Il peut être d’origine ovarienne à partir d’une tumeur mucineuse développée sur tératome ovarien ou d’origine pancréatique à partir de tumeurs mucineuses papillaires intra-canalaires (TIPMP) avec ou sans adénocarcinome mucineux /colloïde associé.
- Goblet cell adénocarcinome (GCC) (ancien « goblet cell carcinoïde ») : il s’agit d’une tumeur mixte constituée d’éléments épithéliaux et neuroendocrines avec présence de cellules caliciformes « goblet cells » de type intestinal. Il survient à un âge moyen de 58,9 ans avec une prépondérance féminine et intéresse 14-19% des carcinomes appendiculaires (Clift et al., 2018).
- Immunohistochimie : CK20+/-, ACE, chromogranine +/-, synaptophysine +/-.
Tableau 6
Grading OMS 2019 en fonction des composantes tumorales
de haut et de bas grade en fonction des composantes architecturales :
Bas grade : architecture tumorale avec tubes et clusters (amas cellulaires)
Haut grade : cellules isolées, massifs cribriformes, plages diffuses, atypies nucléaires de haut grade, nécrose, importante activité mitotique
| Classification OMS | Architecture par tubes et cluster | Perte de l’architecture par tubes ou cluster |
|---|---|---|
1 (bas grade)
| > 75 % | < 25 %
|
2 (haut grade)
| 50 - 75 %
| 25 - 50 %
|
3 (haut grade)
| <50 %
| > 50 %
|
La stadification TNM des GCC suit celle des adénocarcinomes appendiculaires (WHO Classification of Tumors, Digestive System Tumors).
- Néoplasies neuroendocrines (cf. TNCD chapitre 11. NNE)
- Tumeurs mésenchymateuses (sarcome, GIST (cf. TNCD chapitre 12. GIST)…)
- Autres (lymphomes, métastases)
REFERENCES
- La totalité de l'appendice doit être soumis à l'examen histologique. (accord d’experts)
- Une relecture par les anatomopathologistes du groupe RENAPATH (TENpath pour les tumeurs neuroendocrines) est proposée en cas de doute. (accord d’experts)
http://www.renape-online.fr/fr/espace-professionnel/groupe-rena-path.html - La classification PSOGI 2016 doit être adoptée pour les tumeurs appendiculaires. (accord d’experts)
14.2. Epidémiologie, dépistage des formes familiales et d'autres cancers associés
Les tumeurs épithéliales appendiculaires sont identifiées dans 0,9 à 1,4% des pièces d’appendicectomies (Hatch and Gilbert, 2018). Les plus fréquentes sont les NNE (non traités dans ce chapitre) (Hatch and Gilbert, 2018). Le MA est diagnostiqué sur la pièce opératoire chez 0,2-0,3% des patients appendicectomisés (Gillion et al., 2009).
Du fait de la rareté de ces tumeurs, aucune forme familiale n’a été décrite à ce jour.
Cependant, il faut noter l’incidence élevée de polypes coliques (44%) associés à la présence d’une tumeur épithéliale appendiculaire. Embryologiquement, l’appendice dérive du colon avec des caractéristiques architecturales histologiques similaires. Chez les patients ayant une tumeur épithéliale appendiculaire, quel que soit son type histologique, il existe une incidence élevée de néoplasie colorectale, qu’elle soit synchrone ou métachrone (dans environ 10% des cas pour les tumeurs carcinoïdes et dans plus de 50% des cas pour les tumeurs épithéliales appendiculaires malignes) (voir plus loin) (Smeenk et al., 2008; Trivedi et al., 2009).
14.3. Modes de découverte
Une tumeur appendiculaire est responsable d’une symptomatologie peu spécifique, et plus de 50% des patients sont asymptomatiques. Dans les autres cas, il peut s’agir de douleurs abdominales aigues (pouvant mimer une appendicite aigue) ou chroniques, d’une masse abdominale ou d’une perte de poids (Legué et al., 2019; 2014). L’examen clinique n’est pas suffisant pour affirmer le diagnostic de tumeur appendiculaire épithéliale.
Le mode de découverte le plus fréquent est la découverte d’une tumeur épithéliale appendiculaire sur pièce d’appendicectomie, qui correspond à environ 2/3 des cas (Gillion et al., 2009). L’enjeu est alors de définir les groupes à risque de récidives sous forme de métastases à distance et/ou sous forme de carcinose péritonéale et/ou de PMP. Les facteurs pronostiques qui seront pris en compte sont le type histologique, le geste chirurgical (perforation, caractère complet ou non de la résection de l’appendice et du méso-appendice), la cytologie péritonéale et les adénopathies du méso-appendice (voir infra chapitre 14.6.1.) (2014).
Cependant, le pourcentage de tumeurs appendiculaires découvertes de manière fortuite augmente avec le temps (Legué et al., 2019). Ainsi, une autre situation clinique est la découverte d’une tumeur épithéliale appendiculaire en pré et per opératoire sans atteinte péritonéale synchrone apparente. Dans ce cas l’enjeu est de respecter les critères carcinologiques de résection dans le but d’éviter une perforation de la tumeur épithéliale ou du MA en résultant.
Enfin, la dernière situation clinique est la découverte d’une tumeur épithéliale appendiculaire avec atteinte synchrone du péritoine. Dans le cas d’une tumeur épithéliale mucineuse, quel que soit son grade, il s’agit d’un authentique PMP (se référer au TNCD chapitre 16. Peudomyxome péritonéal). Dans les autres cas, il s’agit d’une carcinose péritonéale synchrone d’une tumeur appendiculaire. Dans tous les cas, l’enjeu ici est d’évaluer la résécabilité des lésions et l’opérabilité du patient en vue d’une CCR et CHIP.
14.4. Explorations pré-thérapeutiques selon le mode de découverte
14.4.1. Découverte d’une tumeur épithéliale appendiculaire sur pièce d’appendicectomie
La découverte d’une tumeur sur pièce d’appendicectomie n’est pas rare. Souvent, la tumeur n’est pas visible sur les examens d’imagerie préopératoire et n’est pas vue en per-opératoire.
- Dans le cas d’une tumeur épithéliale, quel que soit son stade, le bilan d’extension doit être complété par une tomodensitométrie (TDM) thoraco-abdomino-pelvienne (niveau recommandation grade A).(Dohan et al., 2018; Durot et al., 2018)
- Il doit être complété par une coloscopie complète à la recherche d’une autre localisation tumorale.
- En cas de contre-indication absolue à l’injection de produit de contraste iodée (insuffisance rénale sévère avec un débit de filtration glomérulaire inférieur à 40 mL/min), la TDM avec injection de produit iodé peut être remplacée par une imagerie par résonnance magnétique (IRM) hépatique injectée avec un chélate de gadolinium (non linéaire) et couplée à une TDM thoracique sans injection. En cas d’allergie suspectée à un produit de contraste iodé, un bilan allergologique doit être réalisé afin d’identifier les produits de contraste à risque et ceux que l’on peut utiliser.
- En cas de néoplasie mucineuse ou d’adénocarcinome à contingent mucineux, plusieurs études rétrospectives de faibles effectifs suggèrent une supériorité de l’IRM dans le bilan d’extension initial et de suivi. (Low et al., 2008, 2015). Celle-ci doit être réalisée par un centre expert en selon un protocole standardisé (http://www.renape-online.fr/data/document/protocole-irm-crinose-rena-rad.pdf).
- Cet examen peut être proposé en cas de suspicion de mucocèle appendiculaire rompue, ou dans le cadre du suivi chez les patients jeunes (accord d’experts) (Menassel et al., 2016). L’IRM ne remplace pas la TDM thoraco-abdomino-pelvienne mais vient en complément.(Bouquot et al., 2018; Dohan et al., 2017)
- Il n’y a aucune place pour la tomographie par émission de positons (TEP) au [18F]-fluoro-2-désoxyglucose (FDG) (18FDG-TEP) dans cette indication.(Moulton et al., 2014).
14.4.2. Découverte d’une tumeur épithéliale appendiculaire avec atteinte synchrone du péritoine
En cas de suspicion ou d’atteinte avérée du péritoine, le bilan d’extension est identique à celui d’une tumeur de découverte fortuite.
- La combinaison de la TDM et de l’IRM péritonéale améliore le bilan topographique de la maladie dans des études rétrospectives de faible effectif (niveau recommandation grade C). (Dohan et al., 2017; Low et al., 2015)
- Toutefois, il n’a pas été montré d’impact de l’IRM sur la prise en charge globale et son utilisation est pour l’instant limitée au bilan topographique préopératoire dans les centres qui en ont l’habitude. (accord d’expert).
- Il n’y a aucune place pour la 18FDG-TEP dans cette indication, hormis lors de la présence d’une lésion extra-abdominale douteuse en TDM (accord d’experts). (Moulton et al., 2014)
L’IRM péritonéale n’apporte pas toutes les informations qu’apporte l’IRM hépatique, qui peut être indiquée en complément pour la caractérisation de lésions hépatiques douteuses (niveau recommandation grade A).
14.4.3. Découverte d’une tumeur épithéliale appendiculaire en pré et per opératoire sans atteinte péritonéale synchrone apparente
Le bilan d’extension est le même qu’en cas de découverte sur pièce anatomopathologique :
- TDM thoraco abdomino-pelvienne ± IRM hépatique en cas de lésion hépatique douteuse (niveau recommandation grade A).
- Le complément par IRM péritonéale peut être proposé en cas de doute sur une atteinte péritonéale (accord d’experts). (Dohan et al., 2018)
REFERENCES
- Seule une TDM abdominopelvienne avec injection de produit de contraste iodé est recommandée pour le bilan d’une tumeur épithéliale appendiculaire et d’une perforation. (niveau recommandation grade A)
- Une coloscopie est recommandée pour exclure une seconde localisation (accord d’experts).
OPTIONS
- IRM péritonéale (niveau recommandation de grade C)
- Marqueurs tumoraux : la littérature concernant le dosage des marqueurs tumoraux ne concerne que les tumeurs épithéliales appendiculaires associées à une atteinte péritonéale. Les marqueurs tumoraux (ACE, Ca-125, Ca-15-3, Ca-19-9) manquent de spécificité diagnostique mais peuvent être dosés dans le suivi évolutif. En pratique courante, l’apport des marqueurs tumoraux reste très modeste (accord d’experts). (2014).
14.5. Traitements
14.5.1. TRAITEMENT CHIRURGICAL
La chirurgie est la base du traitement curatif.
REFERENCES
Appendicectomie
- Tumeur mucineuse appendiculaire de bas grade
- Il est recommandé (accord d’experts) que face à tout appendice distendu, dont l’aspect évoque un mucocèle appendiculaire (MA) sur une tumeur épithéliale appendiculaire, une manipulation avec une extrême précaution, afin d’éviter toute extravasation de mucus ou rupture du mucocèle dans la cavité péritonéale (accord d’experts) et la réalisation d’une cytologie péritonéale (accord d’experts). L’exploration complète quadrant par quadrant (optique 30°) de la cavité abdominale doit être réalisée pour rechercher une atteinte péritonéale non visible sur les examens d’imagerie préopératoire. L’extraction de la pièce opératoire doit se faire dans un sac d’extraction et sur la ligne médiane. (accord d’experts)
- L’exérèse de l’appendice doit être complète avec son mésoappendice permettant un curage ganglionnaire, et la section de la pièce opératoire doit passer en zone saine au niveau de sa base (agrafage caecal) (niveau recommandation grade C)
- La voie d’abord coelioscopique est faisable (niveau recommandation grade C) pour des équipes entrainées. Les trocarts doivent être placés de préférence sur la ligne médiane (accord d’experts). Sinon une laparotomie médiane sous ombilicale doit être proposée.
- Il est nécessaire d’évaluer cette voie d’abord et d’autre dans des essais randomisés comparatifs (accord d’experts).
Colectomie droite
- Tumeurs mucineuses appendiculaires de haut grade, adénocarcinomes mucineux appendiculaires (quel que soit le grade, avec ou sans cellules en bague à chaton) et Goblet cell adénocarcinome (GCC) (niveau recommandation grade C)
- Colectomie droite avec anastomose iléo-colique et avec curage ganglionnaire.
- Exérèse en bloc du mésocôlon attenant avec repérage du pédicule vasculaire, devant prélever au moins 12 ganglions à analyser.
- La colectomie droite n’est pas indiquée en cas de tumeur mucineuse appendiculaire de bas grade et en cas de pseudomyxome appendiculaire (PMP) avec mucine acellulaire ou de bas grade (accord d’experts).
Chirurgie de cytoréduction avec CHIP
- En cas d’atteinte péritonéale (niveau recommandation grade B)
- En centre expert (accord d’experts)
- Indication à discuter « en adjuvant » en cas de perforation tumorale (spontanée ou iatrogène) après résection appendiculaire ou après résection R2 associée ou non à des lésions péritonéales. (accord d’experts)
Le score PCI (Jacquet and Sugarbaker, 1996) est établi en utilisant la mesure de la taille des lésions péritonéales (accord d’experts).

- Chirurgie de cytoréduction : elle doit permettre l’exérèse de l’ensemble des lésions macroscopiques.
- Quantification de l’éventuelle maladie résiduelle après cytoréduction (CC score) (accord d’experts) (Jacquet and Sugarbaker, 1996) :
- CC0 : pas de maladie résiduelle
- CC1 : maladie résiduelle < 2,5 mm
- CC2 : maladie résiduelle > 2,5 mm
- CC3 : maladie résiduelle > 25 mm (n’est en règle jamais utilisé)
- En cas de cytoréduction complète : chimiothérapie hyperthermique intrapéritonéale (CHIP)
- Pas de consensus sur le protocole de CHIP (voir TNCD chapitre 16. Pseudomyxome péritonéal)
OPTIONS
Chirurgie de cytoréduction seule
- Une chirurgie de debulking en centre expert à visée symptomatique peut être proposée chez les patients ayant des co-morbidités ne permettant pas de réaliser une chirurgie de cytoréduction complète (CCR) suivie de CHIP, ou ayant une maladie non résécable en totalité. (accord d’experts)
Stratégie de « wait and see » en centre expert
- Patient opéré d’une appendicectomie avec envahissement péritonéal minimal ou mucine acellulaire réséquée, spécialement chez les jeunes femmes en âge de procréer. (accord d’experts)
ESSAI CLINIQUE
- Aucun
14.5.2. TRAITEMENT MÉDICAL
14.5.2.1. Traitement médical dans un contexte palliatif
14.5.2.1.1. Etudes rétrospectives
- Deux études rétrospectives portants sur 196 patients (54 et 142 patients) ont suggéré la faisabilité et l’efficacité potentielles de différents protocoles à base de 5FU, le plus souvent associés à de l’oxaliplatine, et parfois une thérapeutique ciblée de type bevacizumab ou cetuximab. Les taux de contrôle tumoral variait entre 56% et 86%, et le taux de réponse entre 3,7% et 44% (Shapiro et al., 2010) (Lieu et al., 2012) (niveau recommandation grade C).
- Une étude rétrospective s’est intéressée à l’effet des anti-angiogéniques sur des tumeurs épithéliales de l’appendice non-résécable. Il s’agissait de 130 patients atteints de tumeurs épithéliales de l’appendice naïfs de tout traitement anti-cancéreux. L’utilisation du bevacizumab a permis d’augmenter la survie globale (HR = 0,49 ; IC 95 % = 0,25 – 0,94, P = 0,03) et la survie sans progression (HR = 0,69 ; IC 95 % = 0,47 – 0,99, P = 0,47) pour tous les sous-types histologiques. La survie sans progression était plus importante sur les tumeurs peu différenciées, par rapport aux tumeurs bien différenciées (9 versus 3 mois) (Choe et al., 2015) (niveau recommandation grade C).
14.5.2.1.1. Etudes prospectives
Seulement 2 essais prospectifs ont évalué l’efficacité de protocoles de chimiothérapie dans les tumeurs mucineuses de l’appendice en situation palliative. Les chimiothérapies utilisées n’étaient pas associées à des thérapeutiques ciblées.
- Un premier essai de phase II a évalué l’efficacité de l’association capecitabine et mitomycine C chez 40 patients atteints de pseudomyxomes non résécables. Le taux de contrôle tumoral était de 38%, et 2 patients ont pu être opérés par chirurgie de cytoréduction (Farquharson et al., 2008) (niveau recommandation grade B).
- Une deuxième étude s’est intéressée à l’efficacité du FOLFOX 4 chez des patients atteints de pseudomyxomes péritonéaux non résécables, ou en rechute. 20 patients ont été inclus entre 2011 et 2013. Le taux de réponses était de 20 %, pendant que 45 % des patients avaient une stabilisation, et 35 % une progression. La durée médiane de réponses était de 14,2 mois. Le taux de contrôle tumoral était de 65 %. A noter que 2 patients ont eu une réponse suffisante pour être opérés, dont un avec une chirurgie CC0. La survie sans progression médiane était de 8 mois et la survie globale médiane est de 26,2 mois (Pietrantonio et al., 2014) (niveau recommandation grade B).
14.5.2.2. Place de la chimiothérapie néoadjuvante et/ou adjuvante dans un contexte potentiellement curatif
14.5.2.2.1. Etudes rétrospectives
- Plusieurs études rétrospectives rapportent des résultats discordants. Cinq études rétrospectives portants sur plus de 3574 patients atteints de pseudoxymomes péritonéaux et/ou tumeurs mucineuses de l’appendice ont suggéré des survies plus faibles chez patients traités par chimiothérapie systémiques, notamment lorsqu’elle était donné en situation néoadjuvante (Baratti et al., 2008) (Chua et al., 2012a) (Shaib et al., 2015) (Munoz-Zuluaga et al., 2019). Il s’agissait d’études de faibles niveaux de preuve (niveau recommandation grade C) en raison de leur caractère rétrospectif, et de l’absence de score de propension. En effet, le plus mauvais pronostic des patients traités par chimiothérapie néoadjuvante est probablement le reflet de maladies plus agressives.
- Une étude rétrospective portant sur 72 patients atteints de carcinoses péritonéales liées à des tumeurs de l’appendice a suggéré une amélioration potentielle de la survie des patients lorsqu’ils recevaient une chimiothérapie néoadjuvante (Milovanov et al., 2015) (niveau recommandation grade C).
14.5.2.2.2. Etudes prospectives
Deux études de phase II ont prospectivement évalué l’utilité de la chimiothérapie néoadjuvante chez des patients atteints de carcinoses péritonéales liées à des tumeurs de l’appendice :
- Résultats d’efficacité chez 34 patients traités par chimiothérapie préopératoire (FOLFOX 88%, XELOX 12%, associée à du bevacizumab pour 62%) comparés à 24 patients opérés d’emblée. Le taux de réponse était de 47 %, et le taux de progression de 50 % dans le groupe chimiothérapie néoadjuvante. L’index de carcinose péritonéale était plus faible dans le groupe chimiothérapie néoadjuvante. (19 versus 28, P = 0.0003), avec moins de résections viscérales dans le groupe chimiothérapie néoadjuvante (2,7 versus 4,4) et le taux de chirurgie CC0 était de 65 % dans le bras chimiothérapie première, contre 50 % dans le bras chirurgie d’emblée. (Bijelic et al., 2012) (niveau recommandation grade B).
- Résultats d’efficacité chez 34 patients par FOLFOX en situation néoadjuvante. L’évaluation clinique retrouvait une stabilisation de la maladie chez 71 % des patients, l’évaluation radiologique retrouvait une stabilité de la maladie chez 65 % des patients. L’exploration coelioscopique de la carcinose avait montré une progression chez 50 % des patients. Histologiquement, une réponse partielle a été identifiée chez 20 % des patients, une réponse complète histologique chez 9 % des patients (Sugarbaker et al., 2010) (niveau recommandation grade B).
14.5.2.3. Synthèse
- Au total, parmi les traitements médicaux les plus étudiés dans les tumeurs de l’appendice, les chimiothérapies à base de 5FU dominent, avec notamment l’association FOLFOX-4 permettant d’observer des taux de réponses compris entre 20% et 40%. Aucune étude n’a réellement démontré l’avantage d’associer une thérapeutique ciblée, de type anti-angiogénique ou un anti-EGFR avec la chimiothérapie systémique, même si cette stratégie est couramment pratiquée. Il existe des données précliniques et quelques données cliniques de faible niveau de preuve (niveau recommandation grade C) pour suggérer la place prometteuse d’anti-angiogéniques dans cette maladie.
- Aucun essai clinique randomisé ne valide une stratégie thérapeutique par rapport à d’autres en termes de traitement médical à administrer.
- Même s’il est considéré que les tumeurs de bas grade ont une mauvaise réponse à la chimiothérapie, il n’existe pas dans la littérature de données corroborant cette hypothèse. Il paraît cependant logique de réserver la chimiothérapie aux adénocarcinomes et tumeurs peu différenciées de même celles avec cellules en bague à chaton en raison leur plus mauvais pronostic.
- Concernant la place des traitements médicaux en situation péri-opératoire, les données disponibles à faible niveau de preuve sont discordantes. Plusieurs études rétrospectives de faible niveau de preuve suggèrent l’effet délétère d’une chimiothérapie première sur des indicateurs de survie sans progression et de survie globale, ou encore de rechutes à distance. D’autres études suggèrent l’absence de toxicités et la possibilité de faciliter le geste chirurgical. Le taux de réponses limité de la chimiothérapie dans ces maladies explique ces avis discordants.
- L’effet délétère de la chimiothérapie sur la survie doit cependant être analysé de façon prudente, car un biais de sélection pourrait expliquer ces résultats. En effet la chimiothérapie serait préférentiellement administrée aux patients en mauvais état général ou présentant des maladies plus agressives. L’absence d’essai clinique randomisé expose à ce risque.
14.6. Indications thérapeutiques
14.6.1. TRAITEMENT CHIRURGICAL
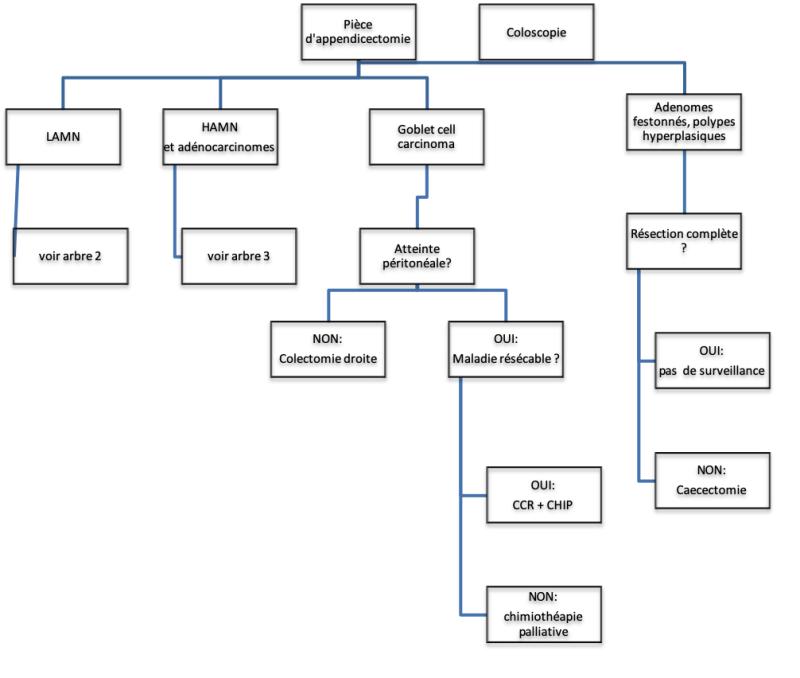
14.6.1.1. Découverte d’une tumeur épithéliale appendiculaire sur pièce d’appendicectomie (situation la plus fréquente) (cf. 14.8.1. algorithme 1)
REFERENCE
Prendre en compte (niveau recommandations grade C) :
- le type histologique
- la cytologie péritonéale (si réalisée)
- la notion de perforation (spontanée ou iatrogène)
- l’exérèse complète du mésoappendice ou non
- l’envahissement ganglionnaire
- la résection complète ou non de la tumeur épithéliale appendiculaire.
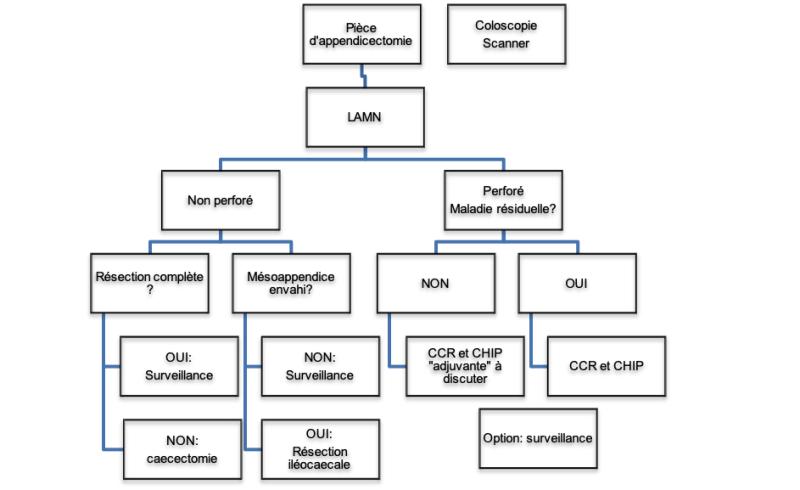
14.6.1.1.1. Tumeur mucineuse appendiculaire de bas grade (cf. 14.8.2. algorithme 2)
Dans ces cas, la survie globale à 3 ans est de 80 % (Bradley et al., 2006).
Les facteurs de mauvais pronostic en analyse univariée sont un âge inférieur à 53 ans, un délai de prise en charge de plus de 24 mois, des complications majeures post opératoires et une résection incomplète (Omohwo et al., 2009) . En analyse multivariée, la résection incomplète est une variable associée à un mauvais pronostic (Chua et al., 2012b).
Bien que la perforation appendiculaire soit considérée comme un facteur pronostic de développement de PMP (Murphy et al., 2006), ce n’est pas évident dans la majorité d’autres études (Fournier et al., 2017; Guaglio et al., 2018; McDonald et al., 2012).
- Selon deux études, une approche expectative pourrait être considérée pour le traitement d’une tumeur mucineuse appendiculaire de bas grade sans ou avec dissémination péritonéale très limitée, car le risque de développer un PMP après appendicectomie et exérèse de la maladie péritonéale est faible : 0% et 4,9% à 40 et 58 mois, respectivement (Guaglio et al., 2018; McDonald et al., 2012). D’autres taux de récidive plus élevés ont été rapportés dans 3 autres études : 23%, 26% et 52% avec un suivi médian de 50, 31 et 50 mois, respectivement (Foster et al., 2016; Fournier et al., 2017; Honoré et al., 2015).
- Cependant, des dosages normaux initiaux de l’ACE, du CA-125 et du CA19-9 montrent une augmentation de la DFS et pourraient être utilisés dans la sélection des patients pour une approche « wait and see » (Fournier et al., 2017).
- Une attitude expectative (« wait and see »), en comparaison d’une approche plus radicale (CCR + CHIP), signifie que le traitement définitif va être effectué à une phase plus tardive de l’histoire de la maladie. Les tumeurs mucineuses appendiculaires de bas grade sont, par définition, des entités avec une faible agressivité biologique, caractérisées par une évolution indolente. On pourrait donc supposer que la réalisation d’une CCR et CHIP au moment de la récidive, après une période de surveillance ne modifie pas la survie globale. Dans l’étude multicentrique de Chua et al. portant sur 2298 PMP que les patients aient été référés au diagnostic ou après une intervention une chirurgie de cytoréduction limitée, les patients atteints d’une tumeur mucineuse appendiculaire de bas grade avaient une survie globale de 81% à 5 ans.
- Enfin, la présence d’un envahissement ganglionnaire était trouvée chez peu de patients qui avaient une hémicolectomie droite après appendicectomie seule (Honoré et al., 2015), bien qu’elle ait été réalisée dans de nombreuses études (Fournier et al., 2017; Guaglio et al., 2018; McDonald et al., 2012).
REFERENCES
- En cas de résection incomplète (chirurgie R1 ou R2), une reprise chirurgicale sous la forme d’une caecectomie est recommandée pour obtenir une résection carcinologique en zone saine (niveau recommandation grade C).
- En cas de méso-appendice envahi, une iléo-typhlectomie sans curage est recommandée, de manière à avoir une résection R0 (niveau recommandation grade C).
- En cas de tumeur perforée (spontanée ou iatrogène) ou tumeur de stade pM1a (avec PCI>3 et plus d’un cadran atteint) ou pM1b, une chirurgie de cytoréduction complète (CCR) et CHIP « adjuvante » peut être réalisée en centre expert (accord d’experts).
- Dans les autres cas (notamment tumeur de stade pM1a avec PCI<3) : surveillance en centre expert RENAPE (accord d’experts)
OPTION
- Laparoscopie exploratrice : pour confirmer le caractère de bas grade en cas de pseudomyxome péritonéal (PMP) avec envahissement péritonéal minimal ou mucine acellulaire lorsqu’une stratégie de watch and see peut être appropriée, spécialement chez les femmes en âge de procréer ou si réévaluation péritonéale en centre expert RENAPE (bilan en vue d’une chirurgie de cytoréduction complète (CCR) et CHIP) (accord d’experts).
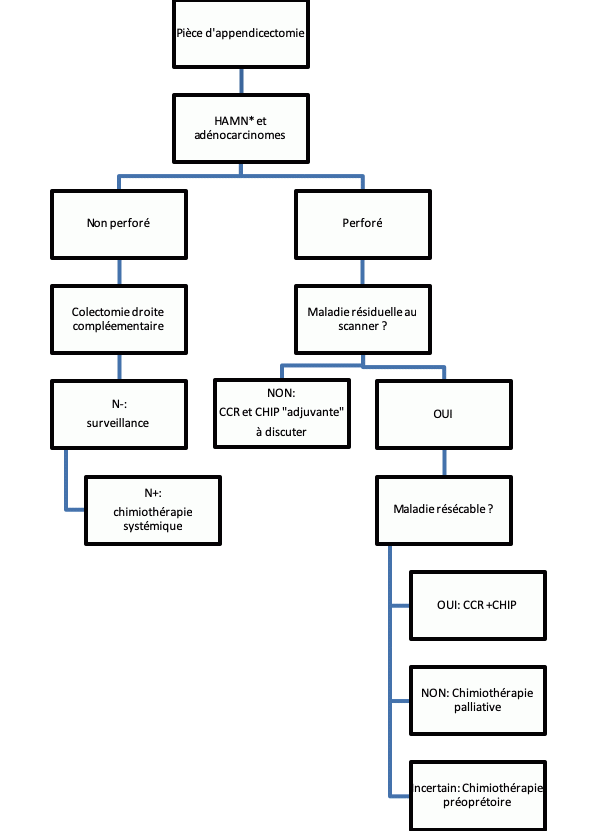
14.6.1.1.2. Tumeur mucineuse appendiculaire de haut grade et adénocarcinomes mucineux appendiculaires (cf. 14.8.3. algorithme 3)
- Des informations complémentaires sont nécessaires concernant le pronostic de ces « tumeur mucineuse appendiculaire de haut grade » récemment rajoutées dans la classification des néoplasies mucineuses, extrêmement rares et donc encore peu connues (Legué et al., 2019). Elles sont actuellement prises en charge comme les adénocarcinomes mucineux.
- Les patients atteints d’adénocarcinome appendiculaire ont une survie globale à 3 ans de 52 % mais en cas de résection complète la survie serait similaire à celle de ceux atteints de tumeurs mucineuses appendiculaires de bas grade. La résection complète lisserait le pronostic histologique (Lo and Sarr, 2003). De plus, la résection incomplète est un facteur indépendant de mauvais pronostic sur la survie globale. Les néoplasies mucineuses de haut grade ou adénocarcinomes appendiculaires diagnostiqués sur la pièce opératoire nécessitent une résection carcinologique complémentaire au même titre que l’adénocarcinome colique.
REFERENCES
- Il est recommandé de réaliser une colectomie droite avec curage ganglionnaire (niveau recommandation grade C) sauf en cas de néoplasie appendiculaire mucineuse de haut grade (HAMN) de stade pTis.
- En cas d’envahissement ganglionnaire dans le méso appendiculaire, une colectomie droite complémentaire est nécessaire (niveau recommandation grade C).
- En cas de néoplasie appendiculaire mucineuse de haut grade (HAMN) de stade pTis ou une surveillance en centre RENAPE est recommandée (accord d’experts).
- Les tumeurs mucineuses appendiculaires de haut grade et adénocarcinomes mucineux appendiculaires ont un tropisme péritonéal important (Murphy et al., 2006). En l’absence d’éléments en faveur d’une maladie péritonéale sur le bilan préopératoire, plus de 50% des patients opérés d’une chirurgie de second regard en vue d’une CCR et CHIP prophylactique après appendicectomie ont des métastases péritonéales avec un PCI médian de 5 (extrêmes : 1-28) (Mehta et al., 2017). Dans une étude récente incluant 62 patients avec tumeurs mucineuses appendiculaires de haut grade (2 HAMN, 39 adénocarcinomes avec ou sans cellules en bague à chaton, 21 Goblet cell carcinoma), 15% avaient une atteinte ganglionnaire après colectomie droite complémentaires (Mehta et al., 2017). Dans 67% des cas, des lésions péritonéales étaient trouvées à distance des régions anatomiques habituellement réséquées lors d’une hémicolectomie droite conventionnelle. De plus, 23% des patients qui présentaient des métastases péritonéales avaient aussi des ganglions positifs le long de l’axe iléocolique.
- La perforation appendiculaire n’a pas été trouvée comme facteur pronostic de dissémination péritonéale. En revanche, l’histologie « goblet cell carcinoma » augmentait le risque de dissémination péritonéale (68% versus 38% ; P=0,037).
- L’envahissement ganglionnaire semble dépendant de la différenciation tumorale ; avec plus de 29% d’envahissement en cas de tumeur peu différenciée contre 5-6% pour les tumeurs bien ou moyennement différenciées dans un étude rétrospective chez 299 patients avec PMP de haut grade chez qui une colectomie droite était réalisée (Sugarbaker, 2017). En revanche, 2 études prospectives incluant 501 patients avec carcinose péritonéale ont montré que ni l’envahissement ganglionnaire ni le type de chirurgie (hémicolectomie droite ou appendicectomie), n’influait sur la survie globale en analyse multivariée (González-Moreno and Sugarbaker, 2004; González-Moreno et al., 2005). Cependant, ces patients étaient tous atteints de carcinose péritonéale. La colectomie droite diminuait la survie globale quand aucune chimiothérapie intrapéritonéale n’était délivrée (González-Moreno and Sugarbaker, 2004). Cependant, là également, ces patients étaient tous atteints de carcinose péritonéale.
- Les auteurs suggèrent que la colectomie droite systématique ne devrait être réalisée que dans certains cas sélectionnés (González-Moreno and Sugarbaker, 2004).
REFERENCE
- En cas de tumeur perforée (spontanée ou iatrogène) ou stade pM1b, une chirurgie de cytoréduction complète (CCR) et CHIP avec colectomie droite « adjuvante » peut être réalisée en centre expert (niveau recommandation grade C).
14.6.1.1.3. Goblet cell carcinoma
- Le comportement tumoral et le pronostic de ces lésions sont similaires à ceux des tumeurs mucineuses de haut grade et des adénocarcinomes non mucineux (Reid et al., 2016).
- Les adénocarcinomes qui dérivent d’un goblet cell carcinoma ont un comportement encore plus agressif, avec un taux important d’envahissement ganglionnaire (73%) et de métastases péritonéales (60%). La survie globale médiane est de 38 mois pour ces patients (Reid et al., 2016).
REFERENCES
- Une hémicolectomie droite doit être réalisée (niveau recommandation grade C).
- En cas de métastases péritonéales résécables et de patient opérable : chirurgie de cytoréduction complète (CCR) et CHIP en centre expert (niveau recommandation grade C).
OPTION
- En cas de tumeur goblet cell carcinoma (GCC) perforée (spontanée ou iatrogène) sans lésion péritonéale décelable sur les examens préopératoires : chirurgie de cytoréduction complète (CCR) et CHIP avec colectomie droite « adjuvante » à discuter en centre expert (niveau recommandation grade C).
14.6.1.1.4. Adénomes, adénomes festonnés, polypes hyperplasiques
REFERENCE
- En cas de néoplasie appendiculaire mucineuse de bas ou haut grade (LAMN ou HAMN) au stade pTis non rompue et d’exérèse complète, d’adénomes, de polypes festonnés et de polypes hyperplasiques, le traitement par appendicectomie est suffisant si une résection complète est réalisée (accord d’experts).
14.6.1.2. Découverte d’une tumeur épithéliale appendiculaire en pré- et per-opératoire sans atteinte péritonéale synchrone apparente
REFERENCES
Diagnostic per-opératoire :
- Appendicectomie selon les critères carcinologiques dans le chapitre 5.1. (accord d’experts)
Diagnostic pré-opératoire :
- TDM abdomino-pelvienne réalisée et patient informé des risques de l’intervention et découverte potentielle
- Appendicectomie selon les critères carcinologiques dans le chapitre « traitements disponibles » (accord d’experts)
14.6.1.3. Découverte d’une tumeur épithéliale appendiculaire avec atteinte synchrone du péritoine
REFERENCES
Diagnostic pré-opératoire : il s’agit d’un authentique pseudomyxome appendiculaire (PMP) de bas ou haut grade.
- Chirurgie de cytoréduction complète (CCR) et CHIP (niveau recommandations grade B).
- Pas de consensus sur le protocole de CHIP (voir TNCD chapitre 16 Pseudomyxome péritonéal)
Diagnostic per-opératoire
- Il convient d’explorer la cavité abdominale, de décrire le plus précisément possible l’atteinte péritonéale, la présence de gouttelettes ou de plaques mucineuses et la présence ou non de nodules d’aspect infiltrant, au mieux d’établir le score d’index péritonéal de Sugarbaker (PCI) (Jacquet and Sugarbaker, 1996), et de faire figurer le schéma dans le compte-rendu opératoire. Les gestes d’exérèse doivent être limités à une biopsie péritonéale pour confirmer histologiquement le diagnostic. (niveau recommandation grade B)
- Certains auteurs suggèrent que les biopsies au niveau de coupoles diaphragmatiques sont à éviter en raison du risque de perforation pleurale et de la dissémination tumorale résultante (Iversen et al., 2013).
- Le patient est adressé au centre expert régional RENAPE pour le traitement (niveau recommandation grade B).
- L’examen extemporané n’est pas recommandé.
14.6.2. TRAITEMENT MÉDICAL
14.6.2.1. Chimiothérapie néo-adjuvante
REFERENCE
- Pour maladie de résécabilité incertaine (niveau recommandation grade B)
- FOLFOX 4 + bevacizumab pour 4 à 8 cures (niveau recommandation grade B)
ESSAIS CLINIQUE
- Aucun
14.6.2.2. Chimiothérapie adjuvante
REFERENCE
- Aucune
OPTIONS
- Pour chirurgie CC1 : FOLFOX 4 pour 12 cures (avis d’experts)
- N+ après colectomie droite : FOLFOX 4 pour 12 cures (avis d’experts)
ESSAIS CLINIQUE
- Aucun
14.6.2.3. Chimiothérapie au stade de maladie non résécable
REFERENCE
- Aucune
OPTIONS
- FOLFOX 4, FOLFIRI, LV5FU2 ou capécitabine (avis d’experts)
- ± associées à b2vacizumab, ou anti-EGFR (si statut RAS sauvage) (avis d’experts)
- Jusqu’à progression (avis d’experts)
ESSAIS CLINIQUE
- Aucun
14.7. Surveillance post-thérapeutique
REFERENCES
- TDM thoraco abdomino-pelvienne tous les 3 à 6 mois pendant les deux premières années puis annuelle pendant 5 ans. (accord d’experts)
- En cas de tumeur mucineuse appendiculaire de bas grade un suivi par IRM péritonéale uniquement en centre expert peut être proposé. (accord d’experts) (Low et al., 2008)
- En cas de pseudomyxome péritonéal (PMP) de haut grade, un suivi par IRM péritonéale au moins annuelle (accord d’experts) associée à une TDM thoracique peut être envisagé selon les mêmes modalités.
- Pas de dosage de marqueurs tumoraux (sauf pseudomyxomes péritonéaux (cf. chapitre 16 du TNCD)). (accord d’experts)
- Surveillance coloscopique seulement en cas de polypes coliques associées selon les recommandations de l’HAS. (accord d’experts)
14.8. Algorithmes décisionnels
14.8.1. Algorithme 1
14.8.2. Algorithme 2
14.8.3. Algorithme 3
14.9. Bibliographie
- Baratti, D., Kusamura, S., Nonaka, D., Langer, M., Andreola, S., Favaro, M., Gavazzi, C., Laterza, B., and Deraco, M. (2008). Pseudomyxoma peritonei: clinical pathological and biological prognostic factors in patients treated with cytoreductive surgery and hyperthermic intraperitoneal chemotherapy (HIPEC). Ann. Surg. Oncol. 15, 526–534.
- Bijelic, L., Kumar, A.S., Stuart, O.A., and Sugarbaker, P.H. (2012). Systemic Chemotherapy prior to Cytoreductive Surgery and HIPEC for Carcinomatosis from Appendix Cancer: Impact on Perioperative Outcomes and Short-Term Survival. Gastroenterol. Res. Pract. 2012, 163284.
- Borazanci, E., Millis, S.Z., Kimbrough, J., Doll, N., Von Hoff, D., and Ramanathan, R.K. (2017). Potential actionable targets in appendiceal cancer detected by immunohistochemistry, fluorescent in situ hybridization, and mutational analysis. J. Gastrointest. Oncol. 8, 164–172.
- Bouquot, M., Dohan, A., Gayat, E., Barat, M., Glehen, O., Pocard, M., Rousset, P., and Eveno, C. (2018). Prediction of Resectability in Pseudomyxoma Peritonei with a New CT Score. Ann. Surg. Oncol. 25, 694–701.
- Bradley, R.F., Stewart, J.H., Russell, G.B., Levine, E.A., and Geisinger, K.R. (2006). Pseudomyxoma peritonei of appendiceal origin: a clinicopathologic analysis of 101 patients uniformly treated at a single institution, with literature review. Am. J. Surg. Pathol. 30, 551–559.
- Carr, N.J., Cecil, T.D., Mohamed, F., Sobin, L.H., Sugarbaker, P.H., González-Moreno, S., Taflampas, P., Chapman, S., and Moran, B.J. (2016). A Consensus for Classification and Pathologic Reporting of Pseudomyxoma Peritonei and Associated Appendiceal Neoplasia: The Results of the Peritoneal Surface Oncology Group International (PSOGI) Modified Delphi Process. Am. J. Surg. Pathol. 40, 14.
- Carr, N.J., Bibeau, F., Bradley, R.F., Dartigues, P., Feakins, R.M., Geisinger, K.R., Gui, X., Isaac, S., Milione, M., Misdraji, J., et al. (2017). The histopathological classification, diagnosis and differential diagnosis of mucinous appendiceal neoplasms, appendiceal adenocarcinomas and pseudomyxoma peritonei. Histopathology 71, 847–858.
- Choe, J.H., Overman, M.J., Fournier, K.F., Royal, R.E., Ohinata, A., Rafeeq, S., Beaty, K., Phillips, J.K., Wolff, R.A., Mansfield, P.F., et al. (2015). Improved Survival with Anti-VEGF Therapy in the Treatment of Unresectable Appendiceal Epithelial Neoplasms. Ann. Surg. Oncol. 22, 2578–2584.
- Chua, T.C., Moran, B.J., Sugarbaker, P.H., Levine, E.A., Glehen, O., Gilly, F.N., Baratti, D., Deraco, M., Elias, D., Sardi, A., et al. (2012a). Early- and Long-Term Outcome Data of Patients With Pseudomyxoma Peritonei From Appendiceal Origin Treated by a Strategy of Cytoreductive Surgery and Hyperthermic Intraperitoneal Chemotherapy. J. Clin. Oncol. 30, 2449–2456.
- Chua, T.C., Liauw, W., and Morris, D.L. (2012b). Early recurrence of pseudomyxoma peritonei following treatment failure of cytoreductive surgery and perioperative intraperitoneal chemotherapy is indicative of a poor survival outcome. Int. J. Colorectal Dis. 27, 381–389.
- Clift, A.K., Kornasiewicz, O., Drymousis, P., Faiz, O., Wasan, H.S., Kinross, J.M., Cecil, T., and Frilling, A. (2018). Goblet cell carcinomas of the appendix: rare but aggressive neoplasms with challenging management. Endocr. Connect. 7, 268–277.
- Dohan, A., Hoeffel, C., Soyer, P., Jannot, A.S., Valette, P.-J., Thivolet, A., Passot, G., Glehen, O., and Rousset, P. (2017). Evaluation of the peritoneal carcinomatosis index with CT and MRI. Br. J. Surg. 104, 1244–1249.
- Dohan, A., Hobeika, C., Najah, H., Pocard, M., Rousset, P., and Eveno, C. (2018). Preoperative assessment of peritoneal carcinomatosis of colorectal origin. J. Visc. Surg. 155, 293–303.
- Durot, C., Rousset, P., Thivolet, A., Passot, G., Deguelte, S., Dohan, A., Glehen, O., and Hoeffel, C. (2018). What the radiologist should know about postoperative MDCT evaluation of a patient treated with cytoreductive surgery with or without hyperthermic intraperitoneal chemotherapy. Clin. Radiol. 73, 517–525.
- Farquharson, A.L., Pranesh, N., Witham, G., Swindell, R., Taylor, M.B., Renehan, A.G., Rout, S., Wilson, M.S., O’Dwyer, S.T., and Saunders, M.P. (2008). A phase II study evaluating the use of concurrent mitomycin C and capecitabine in patients with advanced unresectable pseudomyxoma peritonei. Br. J. Cancer 99, 591–596.
- Foster, J.M., Sleightholm, R.L., Wahlmeier, S., Loggie, B., Sharma, P., and Patel, A. (2016). Early identification of DPAM in at-risk low-grade appendiceal mucinous neoplasm patients: a new approach to surveillance for peritoneal metastasis. World J. Surg. Oncol. 14, 243.
- Fournier, K., Rafeeq, S., Taggart, M., Kanaby, P., Ning, J., Chen, H.-C., Overman, M., Raghav, K., Eng, C., Mansfield, P., et al. (2017). Low-grade Appendiceal Mucinous Neoplasm of Uncertain Malignant Potential (LAMN-UMP): Prognostic Factors and Implications for Treatment and Follow-up. Ann. Surg. Oncol. 24, 187–193.
- Gillion, J.-F., Franco, D., Chapuis, O., Serpeau, D., Convard, J.-P., Jullès, M.-C., Balaton, A., Karkouche, B., Capelle, P., Parmentier, T., et al. (2009). [Appendiceal mucoceles, pseudomyxoma peritonei and appendiceal mucinous neoplasms: update on the contribution of imaging to choice of surgical approach]. J. Chir. (Paris) 146, 150–166.
- González-Moreno, S., and Sugarbaker, P.H. (2004). Right hemicolectomy does not confer a survival advantage in patients with mucinous carcinoma of the appendix and peritoneal seeding. Br. J. Surg. 91, 304–311.
- González-Moreno, S., Brun, E., and Sugarbaker, P.H. (2005). Lymph node metastasis in epithelial malignancies of the appendix with peritoneal dissemination does not reduce survival in patients treated by cytoreductive surgery and perioperative intraperitoneal chemotherapy. Ann. Surg. Oncol. 12, 72–80.
- Govaerts, K., Lurvink, R.J., De Hingh, I.H.J.T., Van der Speeten, K., Villeneuve, L., Kusamura, S., Kepenekian, V., Deraco, M., Glehen, O., Moran, B.J.; PSOGI. (2020). Appendiceal tumours and pseudomyxoma peritonei: Literature review with PSOGI/EURACAN clinical practice guidelines for diagnosis and treatment. Eur J Surg Oncol. Feb 28. pii: S0748-7983(20)30114-1.doi: 10.1016/j.ejso.2020.02.012. [Epub ahead of print]
- Guaglio, M., Sinukumar, S., Kusamura, S., Milione, M., Pietrantonio, F., Battaglia, L., Guadagni, S., Baratti, D., and Deraco, M. (2018). Clinical Surveillance After Macroscopically Complete Surgery for Low-Grade Appendiceal Mucinous Neoplasms (LAMN) with or Without Limited Peritoneal Spread: Long-Term Results in a Prospective Series. Ann. Surg. Oncol. 25, 878–884.
- Hatch, Q.M., and Gilbert, E.W. (2018). Appendiceal Neoplasms. Clin. Colon Rectal Surg. 31, 278–287.
- Honoré, C., Caruso, F., Dartigues, P., Benhaim, L., Chirica, M., Goéré, D., and Elias, D. (2015). Strategies for Preventing Pseudomyxoma Peritonei After Resection of a Mucinous Neoplasm of the Appendix. Anticancer Res. 35, 4943–4947.
- Iversen, L.H., Rasmussen, P.C., and Laurberg, S. (2013). Value of laparoscopy before cytoreductive surgery and hyperthermic intraperitoneal chemotherapy for peritoneal carcinomatosis. Br. J. Surg. 100, 285–292.
- Jacquet, P., and Sugarbaker, P.H. (1996). Clinical research methodologies in diagnosis and staging of patients with peritoneal carcinomatosis. Cancer Treat. Res. 82, 359–374.
- Kusamura, S., Kepenekian, V., Villeneuve, L., Lurvink, R.J., Govaerts, K., De Hingh, I.H.J.T., Moran, B.J., Van der Speeten, K., Deraco, M., Glehen, O.; PSOGI. (2020). Peritoneal mesothelioma: PSOGI/EURACAN clinical practice guidelines for diagnosis, treatment and follow-up. Eur J Surg Oncol. Mar 12. pii: S0748-7983(20)30113-X. doi: 10.1016/j.ejso.2020.02.011. [Epub ahead of print]
- Lee, W.-S., Choi, S.T., Lee, J.N., Kim, K.K., Park, Y.H., and Baek, J.H. (2011). A retrospective clinicopathological analysis of appendiceal tumors from 3,744 appendectomies: a single-institution study. Int. J. Colorectal Dis. 26, 617–621.
- Legué, L.M., Creemers, G.-J., de Hingh, I.H.J.T., Lemmens, V.E.P.P., and Huysentruyt, C.J. (2019). Review: Pathology and Its Clinical Relevance of Mucinous Appendiceal Neoplasms and Pseudomyxoma Peritonei. Clin. Colorectal Cancer 18, 1–7.
- Lieu, C.H., Lambert, L.A., Wolff, R.A., Eng, C., Zhang, N., Wen, S., Rafeeq, S., Taggart, M., Fournier, K., Royal, R., et al. (2012). Systemic chemotherapy and surgical cytoreduction for poorly differentiated and signet ring cell adenocarcinomas of the appendix. Ann. Oncol. Off. J. Eur. Soc. Med. Oncol. 23, 652–658.
- Lo, N.S.F., and Sarr, M.G. (2003). Mucinous cystadenocarcinoma of the appendix. The controversy persists: a review. Hepatogastroenterology. 50, 432–437.
- Logan-Collins, J.M., Lowy, A.M., Robinson-Smith, T.M., Kumar, S., Sussman, J.J., James, L.E., and Ahmad, S.A. (2008). VEGF expression predicts survival in patients with peritoneal surface metastases from mucinous adenocarcinoma of the appendix and colon. Ann. Surg. Oncol. 15, 738–744.
- Low, R.N., Barone, R.M., Gurney, J.M., and Muller, W.D. (2008). Mucinous appendiceal neoplasms: preoperative MR staging and classification compared with surgical and histopathologic findings. AJR Am. J. Roentgenol. 190, 656–665.
- Low, R.N., Barone, R.M., and Lucero, J. (2015). Comparison of MRI and CT for predicting the Peritoneal Cancer Index (PCI) preoperatively in patients being considered for cytoreductive surgical procedures. Ann. Surg. Oncol. 22, 1708–1715.
- Lurvink, R.J., Villeneuve, L., Govaerts, K., de Hingh, I.H.J.T., Moran, B.J., Deraco, M., Van der Speeten, K., Glehen, O., Kepenekian, V., Kusamura, S., et al. (2019). The Delphi and GRADE methodology used in the PSOGI 2018 consensus statement on Pseudomyxoma Peritonei and Peritoneal Mesothelioma. Eur. J. Surg. Oncol. J. Eur. Soc. Surg. Oncol. Br. Assoc. Surg. Oncol.
- McDonald, J.R., O’Dwyer, S.T., Rout, S., Chakrabarty, B., Sikand, K., Fulford, P.E., Wilson, M.S., and Renehan, A.G. (2012). Classification of and cytoreductive surgery for low-grade appendiceal mucinous neoplasms. Br. J. Surg. 99, 987–992.
- Mehta, A., Mittal, R., Chandrakumaran, K., Carr, N., Dayal, S., Mohamed, F., Moran, B., and Cecil, T. (2017). Peritoneal Involvement Is More Common Than Nodal Involvement in Patients With High-Grade Appendix Tumors Who Are Undergoing Prophylactic Cytoreductive Surgery and Hyperthermic Intraperitoneal Chemotherapy. Dis. Colon Rectum 60, 1155–1161.
- Menassel, B., Duclos, A., Passot, G., Dohan, A., Payet, C., Isaac, S., Valette, P.J., Glehen, O., and Rousset, P. (2016). Preoperative CT and MRI prediction of non-resectability in patients treated for pseudomyxoma peritonei from mucinous appendiceal neoplasms. Eur. J. Surg. Oncol. J. Eur. Soc. Surg. Oncol. Br. Assoc. Surg. Oncol. 42, 558–566.
- Mercier, F., Dagbert, F., Pocard, M., Goéré, D., Quenet, F., Wernert, R., Dumont, F., Brigand, C., Passot, G., Glehen, O., et al. (2019). Recurrence of pseudomyxoma peritonei after cytoreductive surgery and hyperthermic intraperitoneal chemotherapy. BJS Open 3, 195–202.
- Milovanov, V., Sardi, A., Aydin, N., Nieroda, C., Sittig, M., Nunez, M., and Gushchin, V. (2015). Extensive surgical history prior to cytoreductive surgery and hyperthermic intraperitoneal chemotherapy is associated with poor survival outcomes in patients with peritoneal mucinous carcinomatosis of appendiceal origin. Eur. J. Surg. Oncol. J. Eur. Soc. Surg. Oncol. Br. Assoc. Surg. Oncol. 41, 881–885.
- Misdraji, J., Lauwers, G.Y., Irving, J.A., Batts, K.P., and Young, R.H. (2014). Appendiceal or cecal endometriosis with intestinal metaplasia: a potential mimic of appendiceal mucinous neoplasms. Am. J. Surg. Pathol. 38, 698–705.
- Moulton, C.-A., Gu, C.-S., Law, C.H., Tandan, V.R., Hart, R., Quan, D., Fairfull Smith, R.J., Jalink, D.W., Husien, M., Serrano, P.E., et al. (2014). Effect of PET before liver resection on surgical management for colorectal adenocarcinoma metastases: a randomized clinical trial. JAMA 311, 1863–1869.
- Munoz-Zuluaga, C.A., King, M.C., Ledakis, P., Gushchin, V., Sittig, M., Nieroda, C., Zambrano-Vera, K., Sardi, A. (2019). Systemic chemotherapy before cytoreductive surgery and hyperthermic intraperitoneal chemotherapy (CRS/HIPEC) in patients with high-grade mucinous carcinoma peritonei of appendiceal origin. Eur. J. Surg. Oncol. J. Eur. Soc. Surg. Oncol. Br. Assoc. Surg. Oncol. 45, 1598–1606.
- Murphy, E.M.A., Farquharson, S.M., and Moran, B.J. (2006). Management of an unexpected appendiceal neoplasm. Br. J. Surg. 93, 783–792.
- Nishikawa, G., Sekine, S., Ogawa, R., Matsubara, A., Mori, T., Taniguchi, H., Kushima, R., Hiraoka, N., Tsuta, K., Tsuda, H., et al. (2013). Frequent GNAS mutations in low-grade appendiceal mucinous neoplasms. Br. J. Cancer 108, 951–958.
- Omohwo, C., Nieroda, C.A., Studeman, K.D., Thieme, H., Kostuik, P., Ross, A.S., Holter, D.R., Gushchin, V., Merriman, B., and Sardi, A. (2009). Complete cytoreduction offers longterm survival in patients with peritoneal carcinomatosis from appendiceal tumors of unfavorable histology. J. Am. Coll. Surg. 209, 308–312.
- Pape, U.-F., Perren, A., Niederle, B., Gross, D., Gress, T., Costa, F., Arnold, R., Denecke, T., Plöckinger, U., Salazar, R., et al. (2012). ENETS Consensus Guidelines for the management of patients with neuroendocrine neoplasms from the jejuno-ileum and the appendix including goblet cell carcinomas. Neuroendocrinology 95, 135–156.
- Passot, G., Bakrin, N., Garnier, L., Roux, A., Vaudoyer, D., Wallet, F., Gilly, F.N., Glehen, O., and Cotte, E. (2014). Intraperitoneal vascular endothelial growth factor burden in peritoneal surface malignancies treated with curative intent: the first step before intraperitoneal anti-vascular endothelial growth factor treatment? Eur. J. Cancer Oxf. Engl. 1990 50, 722–730.
- Pietrantonio, F., Maggi, C., Fanetti, G., Iacovelli, R., Di Bartolomeo, M., Ricchini, F., Deraco, M., Perrone, F., Baratti, D., Kusamura, S., et al. (2014). FOLFOX-4 chemotherapy for patients with unresectable or relapsed peritoneal pseudomyxoma. The Oncologist 19, 845–850.
- Raghav, K.P.S., Shetty, A.V., Kazmi, S.M.A., Zhang, N., Morris, J., Taggart, M., Fournier, K., Royal, R., Mansfield, P., Eng, C., et al. (2013). Impact of molecular alterations and targeted therapy in appendiceal adenocarcinomas. The Oncologist 18, 1270–1277.
- Reid, M.D., Basturk, O., Shaib, W.L., Xue, Y., Balci, S., Choi, H.-J., Akkas, G., Memis, B., Robinson, B.S., El-Rayes, B.F., et al. (2016). Adenocarcinoma ex-goblet cell carcinoid (appendiceal-type crypt cell adenocarcinoma) is a morphologically distinct entity with highly aggressive behavior and frequent association with peritoneal/intra-abdominal dissemination: an analysis of 77 cases. Mod. Pathol. Off. J. U. S. Can. Acad. Pathol. Inc 29, 1243–1253.
- Shaib, W.L., Martin, L.K., Choi, M., Chen, Z., Krishna, K., Kim, S., Brutcher, E., Staley, C., Maithel, S.K., Philip, P., et al. (2015). Hyperthermic Intraperitoneal Chemotherapy Following Cytoreductive Surgery Improves Outcome in Patients With Primary Appendiceal Mucinous Adenocarcinoma: A Pooled Analysis From Three Tertiary Care Centers. The Oncologist 20, 907–914.
- Shapiro, J.F., Chase, J.L., Wolff, R.A., Lambert, L.A., Mansfield, P.F., Overman, M.J., Ohinata, A., Liu, J., Wang, X., and Eng, C. (2010). Modern systemic chemotherapy in surgically unresectable neoplasms of appendiceal origin: a single-institution experience. Cancer 116, 316–322.
- Shen, P., Thomas, C.R., Fenstermaker, J., Aklilu, M., McCoy, T.P., and Levine, E.A. (2014). Phase II trial of adjuvant oral thalidomide following cytoreductive surgery and hyperthermic intraperitoneal chemotherapy for peritoneal surface disease from colorectal/appendiceal cancer. J. Gastrointest. Cancer 45, 268–275.
- Smeenk, R.M., van Velthuysen, M.L.F., Verwaal, V.J., and Zoetmulder, F.A.N. (2008). Appendiceal neoplasms and pseudomyxoma peritonei: A population based study. Eur. J. Surg. Oncol. EJSO 34, 196–201.
- Sugarbaker, P.H. (2017). When and When Not to Perform a Right Colon Resection with Mucinous Appendiceal Neoplasms. Ann. Surg. Oncol. 24, 729–732.
- Sugarbaker, P.H., Bijelic, L., Chang, D., and Yoo, D. (2010). Neoadjuvant FOLFOX chemotherapy in 34 consecutive patients with mucinous peritoneal carcinomatosis of appendiceal origin. J. Surg. Oncol. 102, 576–581.
- Tang, L.H., Shia, J., Soslow, R.A., Dhall, D., Wong, W.D., O’Reilly, E., Qin, J., Paty, P., Weiser, M.R., Guillem, J., et al. (2008). Pathologic classification and clinical behavior of the spectrum of goblet cell carcinoid tumors of the appendix. Am. J. Surg. Pathol. 32, 1429–1443.
- Trivedi, A.N., Levine, E.A., and Mishra, G. (2009). Adenocarcinoma of the appendix is rarely detected by colonoscopy. J. Gastrointest. Surg. Off. J. Soc. Surg. Aliment. Tract 13, 668–675.
- Zhang, Y., Zulfiqar, M., Bluth, M.H., Bhalla, A., and Beydoun, R. (2018). Molecular Diagnostics in the Neoplasms of Small Intestine and Appendix: 2018 Update. Clin. Lab. Med. 38, 343–355.
- (2014). IV. Les recommandations. J. Chir. Viscérale 151, S15–S63.
- WHO Classification of Tumors – Digestive system Tumors 5th edition 2019

