6. Cancer du canal anal
(Dernière mise à jour le : )Principaux changements de la mise à jour du 01/03/2025
6.1.5. Stadification : version actualisée de classification AJCC (2023) avec ajout du tableau des stades
6.2.3. Intégration d’un algorithme de dépistage des lésions précancéreuses anales liées aux HPV (RPC 2022 de la SNFCP)
6.4.4. Intégration de résultats positifs de phase III PODIUM-303/InterAACT comparant en 1ère ligne carboplatine-pacliraxel versus même traitement + retifanlimab (anti PD1)
6.5.8 et 6.8.3. Tumeurs métastatiques : reformulation indications de chimios 1ère ligne
• Si bon état général OMS 0-1 : mDCF ou carboplatine-paclitaxel
• Si état général OMS 2 : carboplatine-paclitaxel
• Si contre-indication à taxanes : 5FU-cisplatine
6.6. et 6.8.4. Fermeture de l’essai Circa HPV (IC 2017-01)
Groupe de travail et relecteurs
Recommandations communes avec la SNFCP
(Société Nationale Française de Colo-Proctologie)

Responsable :
Dr L. Moureau-Zabotto, centre de radiothérapie du Pays d'Aix, avenue Henri pontier, 13100 Aix-en-Provence.
Groupe de travail :
Laurence Moureau-Zabotto (Aix-en-Provence), Laurent Abramowitz (Paris), Christophe Borg (Besançon), Wulfran Cacheux (Annemasse), Joseph Fabre (Bordeaux), Éric François (Nice), Diane Goere (Paris), Gaël Goujon (Paris), Christine Hoeffel (Reims), Florence Huguet (Paris), Paul Lesueur (Caen-Le Havre), Nicolas Meillan (Argenteuil), Julie Meilleroux (Toulouse), Laurent Siproudhis (Rennes), Anne-Laure Tarrerias-Imbert (Paris), Véronique Vendrely (Bordeaux).
Relecteurs :
Olivier Bouché (Reims), Christelle De La Fouchardière (Marseille), Michel Ducreux (Villejuif), Hélène Etienne (Albi), Sébastien Gaujoux (Paris), Pierre Guillet (Lyon), Boris Guiu (Montpellier), Thierry Lecomte (Tours), Côme Lepage (Dijon), Astrid Lièvre (Rennes), Pascale Mariani (Paris), Johanna Moreau (Reims), Iradj Sobhani (Créteil).
Comment citer ce chapitre ?
Moureau-Zabotto L, Vendrely V, Abramowitz L, Borg C, Francois E, Goere D, Huguet F, Peiffert D, Siproudhis L, Ducreux M, Bouché O. Anal cancer: French Intergroup Clinical Practice Guidelines for diagnosis, treatment and follow-up (SNFGE, FFCD, GERCOR, UNICANCER, SFCD, SFED, SFRO, SNFCP). Dig Liver Dis. 2017 Aug;49(8):831-840.
Et mise à jour 2025 :
Moureau-Zabotto L, Vendrely V, Abramowitz L, Borg C, Cacheux W, Fabre J, Francois E, Goere D, Huguet F, Goujon G, Hoeffel C, Lesueur P, Meillan N, Meilleroux J, Siproudhis L, Tarrerias-Imbert AL, Ducreux M, Bouché O. « Cancer du canal anal ». Thésaurus National de Cancérologie Digestive, mars 2025, en ligne [http://www.tncd.org]
6.1. Introduction
Le cancer du canal anal est un cancer rare, mais dont l’incidence augmente en lien avec les infections à papillomavirus humain, notamment chez des patients atteints par le virus de l'immunodéficience humaine (VIH) ou immunosupprimés.
Il s’agit d’un cancer lymphophile avec une extension principalement locorégionale pelvienne, les atteintes métastatiques viscérales étant rares. L’histologie la plus fréquente est le carcinome épidermoïde.
C’est un cancer curable dont le traitement repose sur la radiothérapie et la chimiothérapie, la chirurgie restant réservée aux échecs ou aux récidives après traitement. L’enjeu du traitement reste le contrôle loco-régional tout en diminuant la toxicité et les séquelles.
6.1.1. Méthodologie
La mise à jour repose sur l’extraction, à partir de la base de données Medline interrogée en février 2025, des essais randomisés, méta-analyses, conférences de consensus et recommandations de pratique clinique avec les mots-clés « anus neoplasm », « anal cancer » et «squamous cell carcinoma », en anglais ou en français, sans limitation de date.
Les présentes recommandations ont été gradées selon 4 niveaux (A, B, C, accord ou avis d’experts) qui sont résumés dans le tableau 1.
Tableau 1
Système de gradation des recommandations utilisé dans ce chapitre
| Grade | Niveau de preuve correspondant |
|---|---|
| A | Recommandation forte basée par exemple sur un/des essai(s) comparatif(s) randomisé(s) de forte puissance, une/des méta-analyse d’essai(s) comparatif(s) randomisé(s), ou une analyse de décision fondée sur des études bien menées. |
| B | Recommandation basée sur une présomption scientifique à partir d’essais comparatifs randomisés de faible puissance, d’études comparatives non randomisées bien menées ou d’études de cohortes. |
| C | Recommandation basée sur un faible niveau de preuve à partir d’études cas-témoins, d’études comparatives comportant des biais importants, d’études rétrospectives, de séries de cas, d’études épidémiologiques descriptives (transversale, longitudinale). |
Accord ou Avis d’experts | Recommandation basée sur un accord d’experts ou un avis d’experts en l’absence de données suffisantes de la littérature |
6.1.2. Epidémiologie
Le canal anal est la partie terminale du tube digestif, mesurant 3 à 4 cm et située entre le rectum et la peau de la marge de l'anus. Les tumeurs de la marge anale sont classées avec les tumeurs cutanées (OMS).
Les cancers du canal anal sont rares avec environ 2000 nouveaux cas par an en France. Ils prédominent chez la femme (sex ratio de 0,4 à 4,4 en France). Deux tiers des patients ont plus de 65 ans. Ils représentent 2,5 % des cancers digestifs (Siegel 2013), et 6 % des cancers ano-rectaux (Siegel 2013, Glynnes-Jones 2014).
Leur incidence augmente (Jemal 2013), pour de multiples raisons). Le human papillomavirus (HPV) 16 est présent dans 89 % des cancers de l’anus (Abramowitz 2011, Valmary-Degano 2013). Cette augmentation est particulièrement observée chez des hommes de la quarantaine infectés par le VIH (Abramowitz 2009, Piketty 2012, Clifford 2022).
Les cancers épidermoïdes du canal anal représentent 95% des cas de cancers du canal anal. Seuls 5% sont métastatiques au diagnostic (Abramowitz 2009, FNCLCC 1992).
Pour les deux sexes, les facteurs de risques sont les infections liées à l’HPV (Abramowitz 2011, Valmary-Degano 2013, Gross 2018, Clifford 2022), la séropositivité HIV (Piketty 2012, Frisch 2000, Clifford 2022), l’immuno-suppression (FNCLCC 1992, Penn 1986, Clifford 2022), le tabagisme, les rapports passifs anaux, la multiplication des partenaires sexuels ([Frisch 2000, Daling 2004) et l’âge (Penn 1986, Frish 2002, Clifford 2022).
6.1.3. Diagnostic histologique
6.1.3.1. Carcinomes invasifs (invasion du chorion)
La majorité des carcinomes du canal anal et de la région péri-anale sont des carcinomes épidermoïdes. Les termes de carcinome transitionnel ou cloacogénique doivent être abandonnés.
La classification de l’OMS décrit plusieurs types histologiques :
- Carcinome épidermoïde
- carcinome verruqueux (condylome géant de Buschke)
- Adénocarcinome
- Carcinome indifférencié
- Tumeurs neuro-endocrines (NET) / Carcinome neuroendocrine (NEC)
- Tumeur mixte neuro-endocrine/non neuro-endocrine (MiNEN)
- Autres : mésenchymateuses (sarcome, mélanomes), lymphomes…
6.1.3.2. Cas particulier des lésions intra-épithéliales
Si une lésion n’envahit pas le sphincter interne en échoendoscopie (lésion dite usT1), il devient alors difficile de différencier par la simple imagerie, une lésion intra-épithéliale ou pré-néoplasique, d’un carcinome épidermoïde invasif.
Comme pour le col de l’utérus, les lésions pré-néoplasiques du canal anal précèdent souvent l’apparition du carcinome invasif et sont liées à une infection par l’HPV (voir figure 1 ci-dessous).
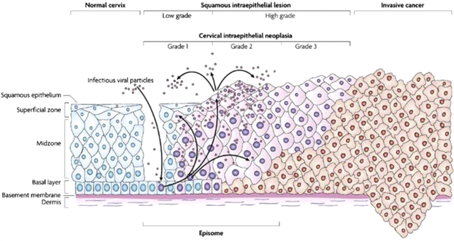
Les différents stades de lésions pré-invasives
Dans la dernière classification TNM et la classification OMS des Tumeurs Digestives de 2019 (5ème édition), le stade pTis (in situ) est désigné par quatre termes synonymes :
- Carcinome in situ
- Maladie de Bowen / papulose bowenoïde (pour les lésions périnéales et péri-anales)
- HSIL (high grade squamous intra-epithelial lesion)
- AIN II-III (anal intra-epithelial neoplasia, grade II, III)
- Ces lésions peuvent être dépistées histologiquement par la réalisation de biopsies dirigées ou cytologiquement par la réalisation de frottis (cf. chapitre 6.2. DEPISTAGE).
- Dans un souci de clarifier et d’unifier les différentes terminologies, il a récemment été proposé par le Collège Américain des Pathologistes et la Société Américaine de Pathologie cervico-utérine ; une classification plus « universelle » de ces lésions pré-néoplasiques : « le LAST project » (Lower Anogenital Squamous Terminology) dont les correspondances sont résumées dans le tableau 2 ci-dessous.
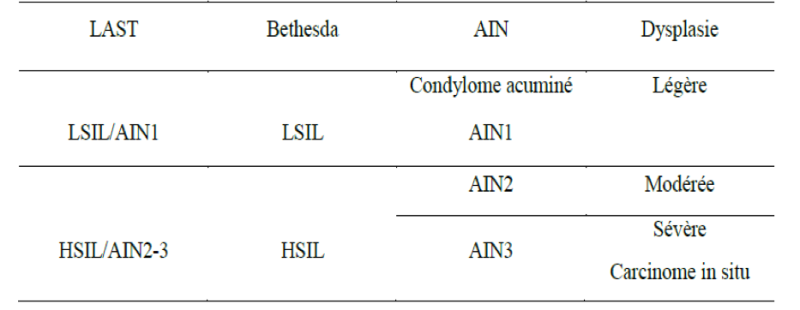
Correspondance des terminologies utilisées dans les lésions induites par l'HPV au niveau anal
- Le caractère invasif d’un carcinome est quant à lui défini histologiquement par le franchissement de la membrane basale, et une invasion du chorion sous-jacent.
- Dans le cas des lésions très exophytiques, une simple biopsie, ne permet pas toujours de « rapporter » la profondeur et d’identifier le franchissement de la basale. Il peut alors être intéressant dans ces cas-là de pratiquer une macro-biopsie voire une chirurgie d’exérèse par un proctologue formé qui fera alors une résection complète le long du sphincter interne et transmettra en anatomie pathologie une pièce étalée et orientée.
- Le compte-rendu anatomopathologique de ces pièces d’exérèse devra préciser si oui ou non il existe un franchissement de la membrane basale. Dans ce cas, le diagnostic de carcinome épidermoïde invasif pourra être porté et le compte-rendu devra alors préciser le degré de différenciation, la mesure de l’infiltration en profondeur, l’extension horizontale, l’état des marges de résection et la présence ou l’absence d’embole vasculaire.
6.1.4. Facteurs pronostiques
Outre la classification T (taille tumorale) (Ajani 2008, Flam 1996, Gunderson 2012) et N (statut ganglionnaire) (Frish 2002, Bartelink 1997, UKCCCR 1996, Northover 2010), d’autres facteurs pronostiques sont à connaitre. Cependant, ces derniers ne sont pas utilisés en pratique pour la décision thérapeutique.
Ces autres facteurs pronostiques péjoratifs sont les suivants :
- La localisation tumorale (anale, péri-anale, ou périnéale), qui n’est pronostique pas mais qui permettra de définir le type de curage ganglionnaire et l’approche thérapeutique la plus appropriée.
- Le statut HIV, reste controversé (Coghill 2015, Abramowitz 2019) et qui ne montre pas de différence si charge virale HIV bien contrôlée).
- Le sexe masculin (American Cancer Society 2017).
- Le caractère ulcéré de la tumeur (Bartelink 1997, Fenger 2000).
- Le grade histologique peu différencié.
L’absence d’HPV et de surexpression des protéines p16 et p18. Plusieurs études ont montré que l’expression de l’oncogène p16 était associée à la présence d’HPV dans ces carcinomes. La surexpression de p16 présente également un intérêt pronostique. L’absence de détection d’un génotype HPV ou l’absence d’expression de p16 est un facteur de mauvais pronostique (Koerber 2014, Meulendijks 2015, Serup-Hansen 2014).
A l’inverse, le suivi de guidelines améliore les résultats en termes de survie globale (AJCC 2011).
Facteur prédictif :
- L’expression de PDL1 a été identifiée dans près de la moitié des cas de carcinome épidermoïde, laissant présager d’une réponse possible aux anti-PDL1 (Ott PA 2017).
- La recherche de l’expression du statut PDL1 n’est cependant pour l’instant pas réalisée de façon systématique, en pratique courante.
6.1.5. Stadification
Elle est pré-thérapeutique, le traitement initial étant généralement conservateur. L'ancienne classification de l'UICC de 1967, qui reposait sur l'analyse histologique de la pièce opératoire, a été abandonnée.
Tableau 3 Classification TNM clinique de l’AJCC, 9ème édition (2023) (Amin 2017, Janczewski 2024)
Tumeur primitive
Tis : tumeur in situ
T1 : tumeur inférieure ou égale à 2 cm dans sa plus grande dimension
T2 : tumeur supérieure à 2 cm mais inférieure ou égale à 5 cm dans sa plus grande dimension (de 21 mm à 50 mm)
T3 : tumeur supérieure à 5 cm dans sa plus grande dimension
T4 : tumeur, quelle que soit sa taille, qui envahit un ou plusieurs organes adjacents (vagin, urètre, vessie) à l’exception du rectum, de la peau périnéale, du tissu cellulaire sous-cutané et du sphincter.
Tx : non évaluée
Adénopathies régionales (N)
Nx : ganglions non évalués
N0 : absence de ganglion métastatique
N1a : métastases ganglionnaires inguinales et/ou dans le mésorectum et/ou iliaque interne
N1b : métastases ganglionnaires iliaques externes
N1c : métastases ganglionnaires iliaques externes et inguinales, dans le mésorectum et/ou iliaques internes.
Métastases à distance (M)
MX : non évaluées
M0 : pas de localisation secondaire à distance de la tumeur primitive
M1 : métastases à distance
| AJCC 2023 (version 9) | |||
| T | N | M | Stade |
| T1 | N0 | M0 | I |
| T2 | N0 | M0 | IIA |
| T1 | N1 | M0 | IIB |
| T2 | N1 | M0 | IIB |
| T3 | N0 | M0 | IIIA |
| T3 | N1 | M0 | IIIA |
| T4 | N0 | M0 | IIIB |
| T4 | N1 | M0 | IIIC |
| Tout T | Tout N | M1 | IV |
6.2. Dépistage
6.2.1. Population à risque
Plusieurs facteurs indépendants à risque de survenue de dysplasie de haut grade ou de cancer invasif du canal anal ont été identifiés (Clifford 2022) :
- personnes vivant avec le VIH ;
- personnes ayant des relations sexuelles anales ;
- lésions dysplasiques anales ou génitales HPV induites ;
- carcinome HPV induit génital ou ORL ;
- maladie de Crohn notamment en cas de lésions anopérinéales associées ;
- maladies auto-immunes (lupus) ;
- immunodépression acquise ou induite (transplantation d’organe solide).
- Le risque est le plus élevé chez les hommes ayant une sexualité anale avec des partenaires multiples et vivant avec le VIH, avec une incidence de 131/100 000 personnes-années, soit 30 à 100 fois celle de la population générale.
- Cependant, la majorité des carcinomes invasifs du canal anal sont diagnostiqués chez des patients qui n’ont aucun de ces facteurs de risque.
6.2.2. Indications
Le dépistage est aujourd’hui recommandé (avis d’experts) :
- chez les personnes vivant avec le VIH
- chez les hommes ayant une sexualité anale avec les hommes
- si antécédent de cancer génital HPV induit
- si antécédent de transplantation d’organe.
L’INCa a mené en 2012 une campagne d’information sur l'importance de la prévention du cancer de l'anus par un proctologue-gastroentérologue chez les personnes vivants avec le VIH :
https://www.e-cancer.fr/Expertises-et-publications/Catalogue-des-publications/Le-proctologue-gastroenterologue-acteur-de-la-prevention-du-cancer-de-l-anus-aupres-des-patients-infectes-par-le-VIH
6.2.3. Modalités
- Le choix des stratégies de dépistage est encore discuté et en phase d’évaluation (Hillman 2019, Stewart 2018).
- Des recommandations de dépistage des personnes vivants avec le VIH ont été émises sous l’égide de l’ANRS et du CNS en 2017.
https://cns.sante.fr/wp-content/uploads/2017/10/experts-vih_cancers.pdf - Des Recommandations pour la Pratique Clinique sous l’égide de la SNFCP ont été publiées en 2022 (Spindler 2024)
https://www.snfcp.org/wp-content/uploads/2017/03/Recommandations-pour-la-pratique-clinique-2022-texte-court.pdf
REFERENCE
- Aucune
OPTIONS
- Un dépistage est recommandé annuellement mais ce rythme reste discuté en dehors du cas précis des hommes vivants avec le VIH et ayant une sexualité anale. (avis d’expert)
- Dans le cas des néoplasies intra-épithéliales de haut grade, un suivi semestriel est recommandé. (avis d’expert)
- Les stratégies de dépistage peuvent être simples (anuscopie) ou complexes (tests virologiques, cytologie, anuscopie haute résolution). (avis d’expert)
- Le traitement des néoplasies intra épithéliales de haut grade est également en phase d’évaluation. (cf. chapitre 6.5.2.)
Algorithme de dépistage proposé dans les RPC sous l'égide de la SNFCP 2022 (Spindler 2024)
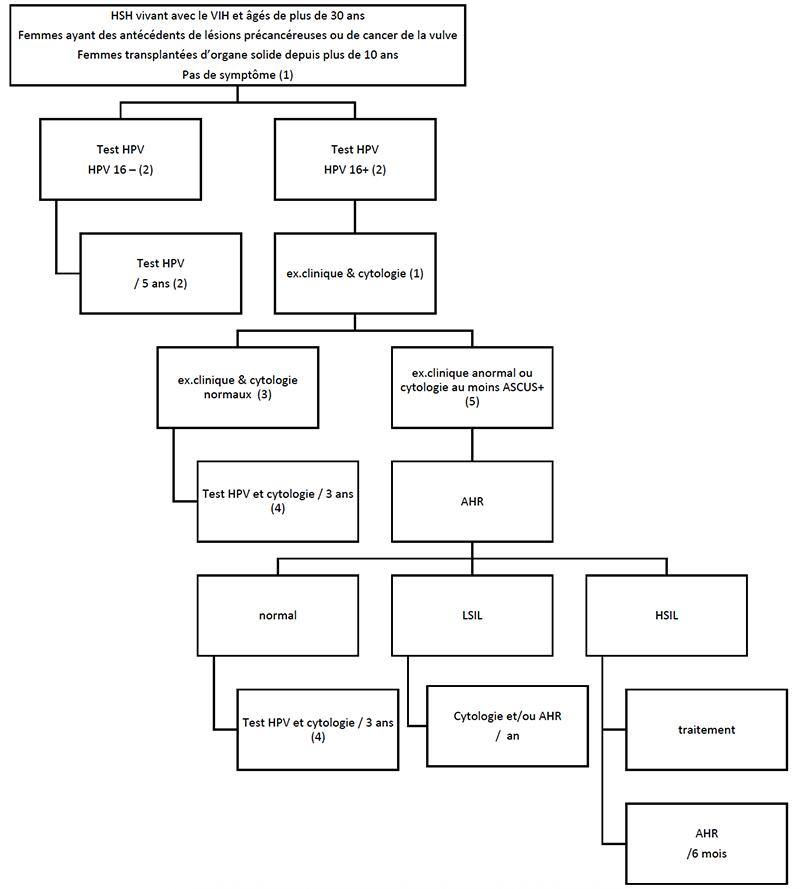
(1) L'examen clinique est indispensable en cas de symptôme. L'examen clinique est constitué d'une analyse visuelle et palpatoire de la région périanale, d'un toucher anal et rectal bas et d'une anuscopie attentive. La présence de lésions suspectes doit faire l'objet de biopsies. La palpation des aires inguinales fait partie de l'examen clinique. Cette exploration doit être réalisée après l’identification d’HPV16.
(2) La recherche de stigmates viraux d'infection HPV 16 est au cœur des tests de triage car ce type viral est associé au carcinome épidermoïde du canal anal avec une prévalence très élevée. Cette stratégie limite le recours à une consultation spécialisée. L'histoire naturelle de l'infection HPV16 et la clairance autorisent un espacement des tests de surveillance à 5 ans en l'absence de stigmate HPV 16. L'incidence cumulée d'infection HPV 16 est de 16 % à 3 ans dans les populations à risque n’ayant pas d’HPV 16 initialement.
(3) Dans l'état actuel des connaissances, la normalité de l'examen cytologique rend très peu probable la présence de lésions d’HSIL (4%).
(4) En présence de stigmates d'infection HPV 16, lorsque l'examen clinique est normal, la clairance du virus se fait lentement et elle n'est observée que chez un peu plus d'un tiers des patients après 3 ans de suivi. Il ne semble donc pas opportun de répéter le test de façon trop rapprochée dans cette population, a fortiori lorsque l’examen clinique est normal. La normalité répétée d'un examen cytologique rend peu probable la survenue d’HSIL dans les 3 ans qui suivent.
(5) La présence d'anomalies cytologiques est associée à une HSIL une fois sur trois, et plus de deux fois sur trois lorsque les lésions cytologiques sont de haut grade. Dans l'attente de tests non invasifs plus discriminants (test de méthylation, P16 Ki-67), une anuscopie haute résolution doit être réalisée dans des conditions optimales avec biopsies orientées. En l’absence d’anuscopie haute résolution accessible, l’examen clinique avec anuscopie doit être répété au minimum annuellement.
6.3. Explorations pré-thérapeutiques
6.3.1. Diagnostic
REFERENCES
- Examen clinique : toucher rectal incluant l’inspection de la marge (avec toucher bi-digitale chez la femme), évaluation de la continence anale, palpation des aires ganglionnaires inguinales.
- Réalisation d’un schéma daté localisant la tumeur.
- Ano/rectoscopie avec biopsie de la tumeur à la pince et analyse anatomo-pathologique de la tumeur anale. La biopsie large et/ou la chirurgie de cyto-réduction tumorale sont déconseillées en raison du risque de troubles sphinctériens qu’elles comportent.
- Recherche de statut HPV et de surexpression de protéine p16.
Cas particulier des lésions pré-infiltrantes ou peu invasives
REFERENCES
- Ces lésions peuvent être dépistées histologiquement par la réalisation de biopsies dirigées ou cytologiquement par la réalisation de frottis.
- Devant une lésion peu infiltrante, il est indispensable d’exiger une analyse histologique auprès d’un expert afin de s’assurer du caractère invasif ou non du carcinome avant toute radiothérapie (accord d’experts).
OPTION (accord d’experts)
- Dans le cas des lésions très exophytiques, une simple biopsie, ne permet pas toujours de « rapporter » la profondeur et d’identifier le franchissement de la basale. Il peut alors être intéressant dans ces cas-là de pratiquer une macro-biopsie voire une chirurgie d’exérèse par un proctologue formé qui fera alors une résection complète le long du sphincter interne et transmettra en anatomie pathologie une pièce étalée et orientée.
6.3.2. Bilan d'extension locorégional et général
L’objectif est de décrire les sites d'extension tumorale, afin d'adapter le traitement aux facteurs pronostiques et de limiter les volumes irradiés.
REFERENCES
- IRM pelvienne : L’IRM est d’intérêt limité pour les lésions superficielles de petite taille en raison de son champ de vue large, et inférieure à l’écho-endoscopie (Otto 2009). En revanche, pour les autres lésions (> 1 cm), l'IRM pelvienne permet une évaluation loco-régionale précise et une évaluation de l'atteinte ganglionnaire locorégionale dont les performances se rapprochent de celle de la TEP (Otto 2009, Mahmud 2017, Rao 2021). Cet examen est opérateur dépendant et doit être réalisé par un spécialiste. Les séquences pondérées en diffusion permettent de détecter des éventuels ganglions mais ne permettent pas de préjuger de leur nature tumorale ou non (Beets-Tan 2018).
- Scanner thoracique, abdominal et pelvien, avec injection de produit de contraste, incluant la totalité des aires inguinales.
- Imagerie métabolique par TEP au 18 FDG :
- Peut être intéressante pour rechercher des ganglions pelviens ou inguinaux non suspectés par l’imagerie classique en particulier pour les tumeurs T2 à T4N0 et pour les tumeurs N+ quel que soit le T (Otto 2009, NCCN 2014, Parikh 2011, Trautmann 2005), avec une meilleure sensibilité que celle du scanner (89-98% vs 58-76%) (Mahmud 2017, Trautmann 2005).
- Cependant, les récentes données de la littérature montrent des performances beaucoup plus modérées en particulier en ce qui concerne la spécificité pour l’atteinte ganglionnaire qui est théoriquement la grande force de la TEP. En effet, deux séries ont analysé les résultats à partir de ganglions prélevés (Iagaru 2009, Mistrangelo 2010). Les faux positifs pour ce critère étaient de 25 et 57% avec un risque accru de faux positif chez les patients VIH+, peut-être avant l’ère des anti-protéases. Globalement les performances de l’IRM semblent inférieures au TEP TDM (Wells 2012, Bhuva 2012) mais les études comparant IRM et TEP TDM sont anciennes.
- De ce fait il faudra être prudent en cas de discordance éventuelle notamment en cas d’adénopathie(s) hypermétabolique(s) et de tumeur de petite taille, et ne pas hésiter à explorer histologiquement ces adénopathies pour prouver leur spécificité (accord d’experts).
- Frottis cervico-vaginal de dépistage et colposcopie avec coloration : systématique avant toute irradiation pelvienne chez les femmes est systématique
- Sérologie VIH doit être systématiquement réalisée.
OPTIONS
- Echographie endo-rectale (sonde rigide) ou écho-endoscopie peut être réalisée pour :
- préciser l'épaisseur maximale de la tumeur et l'envahissement des couches
- rechercher des adénopathies péri-rectales et du promontoire recto-sigmoïdien
- exprimer l'extension locale selon le tableau ci-dessous usTN :
- usT1 : atteinte de la muqueuse et de la sous-muqueuse sans atteinte du sphincter interne
- usT2 : atteinte du sphincter interne sans atteinte du sphincter externe
- usT3 : atteinte du sphincter externe
- usT4 : atteinte d’un organe pelvien de voisinage
- usN0 : pas d'adénopathie suspecte
- usN+ : adénopathie péri-rectale de 5 à 10 mm de diamètre ayant les caractères de malignité (rond, hypoéchogène, contours nets) ou mesurant plus de 10 mm de diamètre.
- La classification écho-endoscopique a un intérêt pronostique supérieure à celle de l’UICC pour prédire le risque de rechute (Giovannini 2001).
- Dans le cas particulier des petites tumeurs T1N0 du canal anal sans preuve histologique d’infiltration, l’échoendoscopie est recommandée afin de vérifier l’absence d’atteinte du sphincter interne, avant d’envisager une exérèse chirurgicale.
- Dosage initial des SCC sériques ayant un intérêt pour le suivi si élevé au moment du diagnostic (Glynne-Jones 2014, NCCN 2014, Goldman 1993). (avis d’experts)
- Dans le cas particulier des petites tumeurs usT1N0 de la marge et/ ou du canal anal, il faudra avant toute prise de décision, réaliser un bilan paraclinique comprenant au minimum IRM pelvienne et scanner thoraco-abdomino-pelvien plus TEP-scanner, afin de ne pas méconnaitre un envahissement ganglionnaire. Dans l’étude de cohorte Anabase, 18% des tumeurs classées T1 présentaient une atteinte ganglionnaire sur le bilan d’extension réalisé (Bacci m et al 2021).
6.3.3. Si administration de chimiothérapie à base de fluroro-pyrimidines
La recherche d’un déficit partiel ou complet en DPD est obligatoire au préalable (HAS 2018, INCa 2018).
REFERENCE
- Recherche d’un déficit en DPD par phénotypage (dosage de l'uracilémie) avec ajustement des doses de 5FU et capécitabine en cas de déficit partiel et contre-indication du 5FU et de la capécitabine en cas de déficit complet (accord d’experts).
OPTION
- Génotypage du gène DPYD si phénotype DPD (uracilémie) anormal (avis d'experts).
6.4. Méthodes thérapeutiques
Le traitement repose sur la radiothérapie, le plus souvent associée à une chimiothérapie concomitante surtout dans les formes localement avancées. La chirurgie doit être discutée pour la prise en charge de la tumeur primitive, en cas d'échec de la radiothérapie/chimiothérapie ou de récidive locale et dans le traitement des adénopathies satellites résiduelles.
Les objectifs sont mesurés par la survie. La survie sans colostomie est également un élément important. L’appréciation du contrôle local et régional ainsi que la fonction sphinctérienne font partie des objectifs secondaires d’évaluation.
6.4.1. La radiothérapie
6.4.1.1. La technique de radiothérapie
La technique recommandée à l’heure actuelle est une technique de radiothérapie conformationnelle avec modulation d’intensité quel que soit sa modalité (VMAT, Tomotherapy…) qui a l’avantage de limiter le risque de toxicité aigüe et tardive liée à l’irradiation des tissus sains avoisinants (Glynne-Jones 2014, HAS 2015, Kachnic 2012, Kachnic 2013).
Cette radiothérapie doit être guidée par l’image, idéalement tridimensionnelle (MVCT ou CBCT). La mise en place de cette irradiation nécessite une étude scannographique dosimétrique réalisée en position de traitement (dans la majorité des cas en décubitus dorsal) avec un repérage de la marge anale.
Elle est réalisée vessie pleine afin de limiter l’irradiation digestive. La délinéation des volumes cibles s’appuiera non seulement sur les données du scanner de simulation, mais également sur les données du reste du bilan d’extension réalisé notamment l’IRM et le TEP-scanner si possible avec fusion d’images.
Elle est administrée si possible en un temps. Une interruption de traitement ne doit être proposée qu’en cas de toxicité limitante, et cet intervalle (ou gap) entre le temps pelvien et la surimpression doit être le plus court possible (Weber 2001, Glynne-Jones 2020).
6.4.1.2. La dose d’irradiation : elle n’est pas consensuelle
Le premier temps d’irradiation doit délivrer sur le pelvis une dose comprise entre 36 et 45 Gy en fractionnement classique (1,8 à 2 Gy par fraction, 5 fractions par semaine). La dose de 36 Gy semble suffisante pour stériliser une maladie infraclinique ganglionnaire (Lepinoy 2015).
La deuxième séquence délivre une irradiation réduite sur la tumeur et sur les adénopathies initialement atteintes, comprise en équivalent de dose biologique entre 15 et 25 Gy. Elle peut être apportée soit par radiothérapie externe soit par curiethérapie interstitielle. Cependant l’essai ACCORD 03 n’a pas prouvé de bénéfice à augmenter la dose totale au-delà de 60 Gy (Peiffert 2012).
La radiothérapie conformationnelle avec modulation d'intensité (RCMI) permet de délivrer le traitement en un temps en utilisant une technique avec complément de dose intégré (Simultaneous Integrated Boost) (Deneen 2013). Dans l’étude de Kachnic, l’IMRT avec SIB a montré une diminution des toxicités pour une efficacité équivalente (Kachnic 2013). Les résultats de l L’étude CANAL-IMRT-01 (NCT02701088, Florescu, Mahe) de promotion française, sont en attente.
Dans deux études rétrospectives le contrôle local s’est avéré meilleur lorsque les patients recevaient un complément d’irradiation par curiethérapie (Moureau-Zabotto 2013, Hannoun-Levi 2011). Cependant, le niveau de preuve reste limité puisque basé uniquement sur des séries rétrospectives, avec des techniques de radiothérapie externes conventionnelles et des étalement très prolongés qui ne sont plus utilisées a l’heure actuelle. La curiethérapie peut néanmoins être une alternative à la radiothérapie externe dans cette indication.
6.4.1.3. Volumes cibles
La délinéation des volumes cibles s’appuiera non seulement sur les données du scanner de simulation, mais également sur les données du reste du bilan d’extension réalisé notamment l’IRM et le TEP-scanner si possible en réalisant une fusion d’images.
Le volume cible anatomo-clinique comporte la tumeur primitive, le canal anal, le mésorectum inférieur pour les tumeurs T1.
Pour les tumeurs localement plus avancées, les volumes d’irradiations doivent inclure les aires ganglionnaires iliaques internes, externes, pré-sacrées et inguinales (Ortholan 2012, Peiffert 2022).
Les volumes d’irradiations ainsi que les recommandations de dose à délivrer aux organes à risques font l’objet des recommandations française de la SFRO (RECORAD) en cours d’actualisation en 2025 (Peiffert 2022).
L'irradiation des ganglions iliaques primitifs peut se discuter pour des tumeurs N3. Un atlas de délinéation a été proposé par l’AGITG (Ng 2012). La délinéation des aires ganglionnaires inguinales doit également être bien précise afin d’éviter un certain nombre de rechutes (Dapper et al 2019).
6.4.2. La chimiothérapie concomitante
La chimiothérapie comporte du 5-fluorouracile (5FU) à la dose de 1000 mg/m² par jour de J1 à J4, et de la mitomycine C à la dose de 10 mg/m² à J1 la première et cinquième semaine de traitement le premier jour du traitement (Ajani 2008, Flam 1996, Gunderson 2012, Bartelink 1997, UKCCCR 1996, Northover 2010, James 2013, Peiffert 2012). En cas de contre-indication à la mitomycine, le cisplatine est une chimiothérapie alternative.
La substitution du 5FU par la capécitabine a été validée par plusieurs études et peut être une OPTION (Glynne-Jones 2008).
Les inhibiteurs d'EGFR associés à la radiothérapie restent décevants. L'ajout du cetuximab ou du panitumab en association à une chimioradiothérapie standard avérée délétère, avec des taux de réponse particulièrement bas (Levy 2015, Garg 2016, Vendrely 2019).
6.4.3. Association radiothérapie-chirurgie
Elle est envisagée devant une tumeur de grand volume, envahissant les organes de voisinage comme la prostate ou le vagin ou lorsque la conservation d’un sphincter fonctionnel n’est pas envisageable.
La chimio-radiothérapie préopératoire, ou à défaut, la radiothérapie pelvienne préopératoire précède l’amputation abdomino-périnéale d’une période d’au moins 6 semaines.
6.4.4. Chimiothérapie exclusive
L’association 5FU plus cisplatine reposait sur des séries rétrospectives de faible effectif et deux études récentes, l’une testant l’association paclitaxel-carboplatine (Rao 2020), et l’autre une tri-chimiothérapie (docétaxel, 5FU, cisplatine) (Kim 2018, Kim 2020, Kim 2023). ont montré des résultats intéressants.
Une étude anglaise prospective randomisée de phase 2 a comparé en première ligne le protocole 5FU-cisplatine : cisplatine (60 mg / m2, J1 / 21j) + 5-FU (1000 mg / m2 / 24h, J1-4 / 21j) et le protocole carboplatine-paclitaxel : carboplatine (AUC 5, J1 / 28j) + paclitaxel (80 mg / m2, J1,8,15 / 28j), avec comme objectif principal le taux de réponse (Rao 2018). L’étude était négative pour son objectif principal (taux de réponse non significativement différents, respectivement de 57 et 59 %). Les survies sans progression médianes n’étaient pas non plus statistiquement différentes, mais il existait un avantage en survie globale dans le bras carboplatine-paclitaxel, qui pouvait s’expliquer par la variabilité des traitements post protocole (24 patients / 45 recevaient une immunothérapie dans le bras avec taxane, contre 6 patients sur 46 dans les bras Cisplatine-5-FU). Le profil de tolérance du protocole carboplatine-paclitaxel paraissait plus favorable (40 % de moins d’effet indésirable grave déclaré) et son efficacité semblait au moins équivalente au 5FU-cisplatine. Il s’agit du premier essai randomisé dans le carcinome épidermoïde de l’anus avancé et il peut être considéré comme une nouvelle option en première ligne.
Une autre option semble encore plus prometteuse, chez les patients en bon état général OMS 0-1. Lors de l’étude multicentrique française de phase 2 Epitopes-HPV02, les patients inclus recevaient en première ligne, en ouvert, au choix de l’investigateur le protocole DCF : docetaxel (75 mg/m2, J1/J21) + cisplatine (75 mg/m2, J1/J21) + 5FU (750 mg / m2 / 24H, J1-J5 / 21 jours) ou le protocole DCF modifié : docetaxel (40 mg/m2, J1 / J14) + cisplatine (40 mg/m2, J1 / J14) + 5-FU (1200 mg / m2 / 24H, J1-J2 / 14 jours) (Kim 2018).
L’objectif principal à atteindre était une survie sans progression à 1 an d’au moins 17 %. L’étude était positive avec une survie sans progression de 47 % à un an et le taux de réponse était de 86 % (44 % de réponse complète). La survie globale médiane n’était pas atteinte au moment de l’analyse finale. Le protocole DCF apparaissait nettement plus toxique que le protocole DCF modifié, avec 83 % d’effet secondaire de grade 3-4 contre 53 % et 14 % de neutropénie fébrile contre aucun cas pour le protocole modifié. Au total, le protocole DCF modifié devient un nouveau standard pour les patients en bon état général (OMS 0- 1), atteints d’un carcinome épidermoïde de l’anus métastatique ou en situation de récidive locale inopérable. De plus, des réponses immunitaires anti-Th1 étaient induites sous DCF et associées à une meilleure survie sans progression (20,6 mois). La capacité du DCF à induire des réponses immunitaires suggère l’intérêt d’associer cette chimiothérapie à des traitements d’immunothérapie.
Les patients HIV positifs doivent être traités selon le même schéma et aux mêmes doses que les patients séronégatifs (Abramowitz 2009, Fraunholz 2011, Kauh 2005). Idéalement, la charge virale doit être en dessous de 10000 copies /ml et le taux de CD4 au-dessus de 200 /mm3. Un ajustement posologique peut être envisagé chez des patients très immunodéprimés ayant un lourd passé médical (Hoffman 1999, Lim 2011, NCCN 2014).
L’utilisation de thérapies ciblées n’a pour l’instant pas fait ses preuves dans le traitement des cancers de l’anus.
L’immunothérapie semble être une des principales perspectives d’avenir, en lien avec le rôle important du système immunitaire dans la carcinogénèse viro-induite.
Chez des patients lourdement pré-traités présentant une surexpression tumorale de PDL-1 > 1 %, le pembrolizumab (anti-PD-1) a montré dans une étude de phase 1b un taux de réponse de 17 % et taux de contrôle de la maladie de 58 %, avec une toxicité acceptable (Ott 2017). Le nivolumab (anti–PD-1) a montré en phase 2 un taux de réponse de 24 % (Morris 2017). Cependant les résultats préliminaires de l’essai SCARCE-PRODIGE 60, une étude de phase 2 randomisée présentés à l’ASCO 2022 ne retrouvent aucun impact clinique significatif de l’ajout d’une immunothérapie (atézolizumab) au traitement de première ligne standard représenté par le mDCF (Kim S 2024).
En première ligne métastatique les résultats de l’étude de phase III PODIUM-303/InterAACT ont été présentés à l’ESMO 2024 : cette étude comparait une première ligne par carboplatine taxol au même traitement associe au retifanlimab un anti PD1 (Rao ESMO 2024). Cette étude, qui a inclus 308 patients dont plus de 83% métastatiques, a démontré que l’ajout du retifanlimab augmentait significativement la survie sans progression médiane (9,3 mois vs 7,4 mois, HR 0,63, p=0,0006), la survie globale (29,2 vs 23 mois , HR 0.,0 ; p=0,027), bénéfice encore majoré en tenant compte du cross over qui était autorisé dans cette étude (HR 0,63, p=0,0005) , ainsi que le taux de réponse objective (56 % vs 44 %) et de la durée de réponse.
Ce traitement en attente d’AMM n’est pas encore disponible. En France actuellement le traitement de référence de 1ère ligne métastatique reste la trichimiothérapie DCF modifié ou l’association carboplatine-paclitaxel.
6.4.5. Chirurgie
Elle est indiquée en cas de lésion usT1 si la preuve histologique du franchissement de la membrane basale n’a pu être obtenue (exiger cette précision dans le compte rendu d’anatomopathologie).
Les marges chirurgicales recommandées doivent être au minimum de 1 mm (accord d’expert) (Glynne-Jones 2014, NCCN 2014). La pièce opératoire doit être adressée orientée et étalée au médecin anatomopathologiste.
En tant que traitement curatif exclusif, elle est réservée aux petites tumeurs T1N0 de la marge anale qui s’apparentent plus à des tumeurs cutanées qu’à des tumeurs de l’anus.
- Les marges chirurgicales recommandées doivent être au minimum de 1 mm (accord d’expert) (Glynne-Jones 2014, NCCN 2014).
- En cas de marge d’exérèse < 1 mm, on peut discuter une reprise chirurgicale ou une radiothérapie (accord d‘experts).
Dans le cas de tumeurs localement évoluées, la chirurgie de la tumeur primitive est effectuée après une chimio-radiothérapie (absence de réponse complète ou poursuite évolutive sous chimio-radiothérapie ou récidive locale après réponse complète à la chimio-radiothérapie en l’absence d’extension métastatique) et comporte une amputation abdomino-périnéale, avec un résultat identique quel que soit l’indication opératoire, en terme de contrôle local ou de métastases à distance (Mariani 2008, Rouquie 2008, Lefevre 2012).
Une colostomie de décharge pré-thérapeutique peut être indiquée dans les tumeurs localement avancées avant de débuter la chimio-radiothérapie, en cas d’envahissement de la cloison recto-vaginale ou de risque sub-occlusif.
Une fistule est présente au diagnostic dans 25 % des cas et nécessite la mise en place d’un séton de drainage avant la radiothérapie et jusqu’à 18 mois après celle-ci avant d’envisager une fistulotomie (Rao 2021).
Le curage inguinal ne doit pas être réalisé de manière prophylactique, mais doit être réservé aux adénopathies résiduelles après association chimio-radiothérapie concomitante ou encore aux rechutes ganglionnaires, et ce en raison du risque de survenue d’un lymphocèle persistant et d'un lymphœdème secondaire des membres inférieurs (Fuchshuber 1997).
6.5. Indications thérapeutiques
6.5.1. Généralités
Cinq essais randomisés ont démontré la supériorité de l’association de chimio-radiothérapie par 5FU-mitomycine C comparée à la radiothérapie seule pour les tumeurs localement avancées avec une augmentation du contrôle local et de la survie sans colostomie (Flam 1996, Gunderson 2012, Bartelink 1997, UKCCCR 1996, Northover 2010).
La chimiothérapie néoadjuvante n’a pas permis d’améliorer le contrôle local et a même démontré qu’elle diminuait le taux de survie sans colostomie. Elle ne doit pas être utilisée en dehors d’essais thérapeutiques (Ajani 2008, Bartelink 1997, UKCCCR 1996). (niveau de recommandation grade A)
La chimiothérapie de maintenance ou de consolidation n’a jamais amélioré le contrôle local, la survie sans maladie ou la survie globale (Flam 1996).
La chirurgie avec amputation abdomino-périnéale est réservée aux poursuites évolutives après traitement par chimio-radiothérapie ou aux récidives locales en l’absence d’évolution métastatique. Elle peut être parfois indiquée devant des complications loco-régionales avec nécrose ou hémorragie. Dans l’essai ACT II, un délai de 26 semaines après le début du traitement a été défini comme optimal pour évaluer la réponse complète, une chirurgie plus précoce n’est donc pas indiquée en l’absence de progression manifeste (Glynne-Jones 2017).
6.5.2. Lésions pré-invasives
- Le traitement des néoplasies intra-épithéliales de haut grade est encore en phase d’évaluation.
- Des RPC sous l’égide de la SNFCP ont été publiées en 2022 (Spindler 2024)
https://www.snfcp.org/wp-content/uploads/2017/03/Recommandations-pour-la-pratique-clinique-2022-texte-court.pdf
REFERENCES (accord d’experts)
Le traitement des néoplasies intra épithéliales de haut grade peut reposer sur un traitement :
- physique (destruction par photocoagulation infrarouge ou électrocoagulation au bistouri électrique), médicamenteux topique (crème imiquimod ou FU Pommad) ;
- chirurgicale d’exérèse.
OPTIONS
- En cas de lésion AIN3 multiples, la surveillance simple (semestrielle voire annuelle par anuscopie haute résolution) reste une option (accord d’experts).
- Dans le cas d’un carcinome épidermoïde invasif du canal anal prouvé histologiquement, un traitement par radiothérapie est indiqué. Devant une lésion peu infiltrante, il est donc indispensable d’exiger une analyse histologique auprès d’un expert afin de s’assurer du caractère invasif ou non du carcinome avant toute radiothérapie (accord d’experts).
6.5.3. Stades usT1 N0 (cf. 6.7.1. Arbre décisionnel 1)
REFERENCES
- Pour les carcinomes épidermoïdes de la marge anale, l’exérèse chirurgicale en marges saines (> 1 mm) est le traitement de référence (accord d’expert).
- Pour les carcinomes épidermoïdes du canal anal :
- la radiothérapie exclusive constitue le traitement de première intention permettant d’obtenir la conservation du sphincter et un taux élevé de contrôle loco-régional (accord d’expert) à condition que le franchissement de la membrane basale soit prouvé histologiquement et précisé dans le compte-rendu anatomopathologique ;
- si le franchissement de la membrane basale n’est pas prouvé histologiquement, il convient de ne pas prendre le risque d’irradier une dysplasie anale sévère (AIN3) et de recourir à la chirurgie d’exérèse par un proctologue expérimenté, qui va effectuer une résection le long du sphincter interne et adresser en histologie une pièce étalée et orientée.
OPTIONS
En cas d’exérèse chirurgicale première pour marisque hémorroïdaire, ou lésion dysplasique et de découverte fortuite à l’analyse histologique de la pièce d’exérèse, d’un carcinome infiltrant :
- Si les marges d’exérèse sont saines (> 1 mm), et la taille tumorale inférieure à 10 mm (risque ganglionnaire <12 %) (accord d’experts), la radiothérapie post-opératoire ne sera pas indiquée.
- Dans ces deux cas (T1N0 de la marge anale et / ou du canal anal), il faudra avant toute prise de décision réaliser un bilan paraclinique comprenant au minimum une IRM pelvienne et un scanner thoraco-abdominopelvien, afin de ne pas méconnaitre un envahissement ganglionnaire. Dans l’étude de cohorte Anabase, 18% des tumeurs classées T1 présentaient une atteinte ganglionnaire sur le bilan d’extension réalisé (Bacci 2021).
- Si marge d’exérèse < 1 mm
- soit reprise chirurgicale si pas de risque de compromettre la fonction sphinctérienne (accord d’experts)
- soit radiothérapie avec une dose totale d’au minimum de 50 Gy (accord d’experts).
- L’association chimio-radiothérapie concomitante reste une option pour les tumeurs T1 avec un index de prolifération élevé et ou d’autres facteurs défavorables, chez des personnes jeunes sans comorbidités (accord d’experts).
6.5.4. Stades T2N0 ou N1 / T2N3 /T3 /T4 (cf. 6.7.2. Arbre décisionnel 2)
La chimio-radiothérapie permet de traiter avec succès les tumeurs localisées T1-2, N0 (de l’ordre de 80 à 90 % de guérison) mais les résultats restent décevants pour les tumeurs localement évoluées avec 35 % de rechute dans les deux ans, que ce soit par échec loco-régional ou par progression métastatique (Vendrely 2023).
REFERENCES
- Association chimio-radiothérapie avec 5FU–Mitomycine C concomitante : indiquée qu’elle que soit l’atteinte ganglionnaire, l’association chimio-radiothérapie concomitante exclusive avec association de 5 FU–Mitomycine C reste le traitement de première intention (niveau de recommandation grade A).
- La réponse à la chimio-radiothérapie devant être évaluée au minimum 6 à 8 semaines après la fin du traitement, un délai supplémentaire allant jusqu'à 6 mois est souvent nécessaire avant de décider une chirurgie (James 2013).
- Amputation abdomino-périnéale (AAP) et colostomie iliaque gauche ou périnéale pseudo-continente :
- chez les patients mauvais répondeurs, progressant sous chimio-radiothérapie
- en cas de maladie persistante après chimio-radiothérapie, malgré un délai d’attente suffisamment long (pouvant atteindre 6 mois (Glynne-Jones 2017) permettant de juger au mieux de l’efficacité ou de la non-efficacité de la chimio-radiothérapie (accord d’experts)
- en cas de mauvais résultats sphinctériens responsables d’incontinence anale, ou en cas de fistule recto-vaginale persistante après chimio-radiothérapie.
- en cas de rechute locale, après chimio-radiothérapie.
- La réalisation d’un PET-Scanner et d’un scanner TAP à la recherche d’une maladie extra-pelvienne est proposée avant AAP.
- AAP et colostomie périnéale pseudo-continente : chez les patients jeunes, refusant une colostomie iliaque gauche, elle permet de conserver une certaine intégrité corporelle (Goere 2009).
OPTIONS
- Radiothérapie exclusive : option pour les tumeurs “T2 N0 faible” c’est à dire de moins de 3 cm (accord d’experts). Pour ces lésions, l’apport de la chimiothérapie est controversé, sans différence selon l’étude de cohorte ANABASE (Vendrely 2023), ou au contraire intéressant (Zilli 2012).
- Chimiothérapie 5FU-cisplatine : sur la base des résultats de l’essai ACTII, alternative à l’association 5FU-mitomycine C (niveau de recommandation grade C).
- Substitution du 5FU par de la capécitabine : option validée par plusieurs études (Glynne-Jones 2008, Meulendijks 2014) (niveau de recommandation grade C).
- Radiothérapie conformationnelle avec modulation d'intensité (RCMI) : permet de délivrer le traitement en un temps en utilisant une technique avec complément de dose intégré (Simultaneous Integrated Boost), mais ce schéma reste une OPTION (accord d’experts).
ESSAI CLINIQUE
- KANALRAD PRODIGE 85 : Essai de phase III multicentrique, prospectif comparant une chimiothérapie d’induction (DCF modifié 4 cycles) suivie de radiochimiothérapie à une radiochimiothérapie standard dans le traitement des carcinomes épidermoïdes de l’anus localement évolués (T3-4 ou N2-3). Coordonnateur : V. Vendrely (Bordeaux) 4b030a7025.pdf (ffcd.fr)
6.5.5. Tumeurs métastatiques d'emblée (cf. 6.7.3. Arbre décisionnel 3)
REFERENCES
- Chimiothérapie de première intention, dont les objectifs sont le maintien de la qualité de vie et l’allongement de la durée de survie.
- Protocole mDCF, ou carboplatine-paclitaxel (recommandation de grade B) (Kim 2018, Rao 2018).
- Protocole 5FU-cisplatine en cas de contre indication aux taxane
- Chimio-radiothérapie concomitante :
- en cas de tumeur considérée comme métastatique en raison d’une atteinte ganglionnaire lombo-aortique, on pourra proposer une association chimio-radiothérapie concomitante à dose curative incluant les aires ganglionnaires lombo-aortiques, plus ou moins précédée d’une chimiothérapie première (accord d’experts).
- en cas de bonne réponse thérapeutique, on pourra discuter au cas par cas une association chimio-radiothérapie concomitante de clôture centrée sur la lésion primitive anale afin de diminuer le taux de rechute locale qui pourrait considérablement impacter la qualité de vie ultérieure. Dans le cas de tumeurs très symptomatiques, la prise en charge peut débuter par une chimio-radiothérapie concomitante (accord d’experts).
OPTIONS
- Chimiothérapie LV5FU2-cisplatine
- Colostomie de décharge : peut être indiquée afin de prendre en charge une incontinence sphinctérienne majeure.
ESSAIS CLINIQUES
- SPARTANA (phase II) : multicentrique prospective d’association de Spartalizumab, mDCF et Radiotherapie pour le canal anal metastatique. Coordinateur : S Kim ( Besancon)
https://clinicaltrials.gov/ct2/show/NCT04894370 - PEVOsq (phase II) : évaluant l’efficacité d’une immunothérapie (pembrolizumab) en association avec un traitement ciblé (vorinostat) chez des patients atteints d’un carcinome épidermoïde récidivant et/ou métastatique (localisations : tête et cou, poumon, col de l’utérus, anus, vulve et pénis). Coordinateur : C Le Tourneau (Paris)
https://www.e-cancer.fr/Professionnels-de-sante/Le-registre-des-essais-cliniques/Le-registre-des-essais-cliniques/Etudes-cliniques/Etude-PEVOsq-etude-de-phase-2-visant-a-evaluer-l-efficacite-de-la-combinaison-de-pembrolizumab-et-de-vorinostat-chez-des-patients-ayant-un-cancer-epidermoide-recurrent-et-ou-metastatique
6.6. Surveillance (cf. 6.7.4. Arbre décisionnel 4)
Le but de la surveillance est double : dépister une récidive locale ou métastatique susceptible d’être traitée à visée curative et déceler une complication locale liée au traitement.
La grande majorité des récidives surviennent dans les 2 ans après le traitement et sont, dans environ 30 % des cas, susceptibles de pouvoir être rattrapées par amputation abdomino-périnéale lorsqu’il s’agit d’une récidive locale ou loco-régionale. La fréquence des récidives locales est dépendante du stade TNM. Elle est estimée < 20 % pour les cancers classés T1, comprise entre 10 et 30 % pour les cancers classés T2, entre 20 et 40 % pour les cancers classés T3 et T4. Le dépistage précoce de ces rechutes locales est essentiel pour pouvoir en envisager une exérèse complète à visée curative.
La fréquence des complications tardives est également dépendante du volume tumoral initial. Elle est de 5 à 10 % pour les petites lésions < 5 cm, de 15 à 30 % pour les tumeurs localement avancées, classées T3-T4, après traitement chimio-radiothérapie. Une mise au point a été récemment publiée concernant le dépistage, la prévention et la prise en charge de ces complications (Camprodon 2021, Besnard 2021).
Dans le cas d’une incontinence anale tardive, il existe désormais un annuaire national des kinésithérapeutes DE spécialisés en rééducation périnéale sur ce lien :
https://afrepp.org/annuaire/
Cette surveillance est essentiellement clinique. Elle est rendue difficile par les remaniements locorégionaux induits par la fibrose post-thérapeutique (Meillan 2015).
En l’absence de lésion macroscopique visible, il est essentiel d’éviter les biopsies de contrôle systématiques dans les territoires traités, surtout après curiethérapie interstitielle, afin d’éviter, dans un tissu fibreux peu vascularisé, d’induire une nécrose locorégionale imposant une sanction chirurgicale radicale. Elles ne doivent donc être réalisées qu’en cas de forte présomption de rechute locale.
REFERENCES (accord d’experts)
- Examen clinique complet : avec toucher pelvien, anuscopie (indispensable), palpation inguinale bilatérale doit être réalisé au minimum 16 semaines après la fin de l’association chimio-radiothérapie concomitante puis tous les 4 mois pendant 2 ans puis tous les 6 mois pendant 3 ans (Glynne-Jones 2014, NCCN 2014) ; les rechutes sont très rares au-delà de 3 ans (James 2013).
- Biopsies doivent être proscrites :
- en situation de réponse complète clinico-radiologique (rapport bénéfice–risque défavorable du fait du risque de nécrose tissulaire en cas de biopsie en territoire irradié), ou encore précocement en cas de persistance de lésions lors de la première évaluation, du fait de la possibilité de régression ultérieure et des difficultés d’interprétation secondaires à l’inflammation post-thérapeutique.
- dans certains cas de tumeur initiale volumineuse, la lésion peut régresser jusqu’à 26 semaines après le début de la chimio-radiothérapie, voire au-delà̀ (Koh 2008, James 2013, Glynne-Jones 2017).
- en l’absence de progression clinique : il est donc recommandé d’attendre 6 mois après la fin du traitement avec une surveillance clinique (ainsi que radiologique) rapprochée sans pour autant réaliser de biopsie immédiate de la lésion (Glynne-Jones 2014, NCCN 2014).
- en cas de suspicion de rechute locale :
- biopsie au trucut ou à l’aiguille fine préconisée ;
- biopsie chirurgicale à éviter : en raison du risque élevé de dégâts sphinctériens et de troubles de la cicatrisation en territoire irradié.
- Suivi des effets secondaires radio-induits :
- Essentiel chez tout patient traité, au niveau de la tolérance digestive, urinaire, incontinence anale et troubles sexuels.
- Les complications osseuses (type fractures du bassin en H) doivent également être détectées.
- Ces complications doivent être évaluées selon des échelles reproductibles (CTCAE v4.0 ou RTOG) pour permettre une comparabilité des résultats obtenus (Anon 2010, Anon 2015).
Il est recommandé de réaliser un examen d’imagerie annuel pendant 5 ans qui comprendra un scanner thoraco-abdominopelvien et/ou une IRM pelvienne (accord d’experts) :
- Scanner thoraco-abdomino-pelvien
- IRM pelvienne : l’IRM s’avère très précise et très utile quant à la classification avant chirurgie de rattrapage (Robinson 2002).
OPTIONS
- Imagerie fonctionnelle TEP FDG : après la fin du traitement conservateur par chimio-radiothérapie semble donner des informations utiles et pertinentes quant à l’obtention d’une rémission clinique complète, en particulier pour la détection des poursuites évolutives ganglionnaires, mais n’est pour l’instant pas recommandé de façon formelle par les recommandations internationales (Glynne-Jones 2014, NCCN 2014). Elle a une bonne valeur prédictive négative et sa négativité est corrélée à une meilleure survie sans récidive.
- Dosage du SCC : intérêt limité dans le suivi et recommandé uniquement en cas de valeur élevée au diagnostic. Il n’est pas à l’heure actuelle recommandé de façon systématique (Glynne-Jones 2014, NCCN 2014). L’étude ANABASE, montre une très bonne corrélation entre négativité du TEP scanner à 6 mois et survie sans récidive. Cela suggère que le TEP-scanner à 6 mois pourrait orienter les modalités de surveillances en particulier pour les tumeurs localement évoluées (Combet-Curt 2024).
- Le dosage de l'ADN tumoral circulant HPV (codant les protéines oncogéniques E6/E7) est actuellement réalisé par certaines équipes. Validée dans deux cohortes ce facteur est significativement associé à la survie globale dans les carcinomes épidermoïdes du canal anal localement avancés (Cabel 2018) et métastasiques (Bernard-Tessier 2019). Cependant, à l’heure actuelle ce facteur n’a d’intérêt que dans le cadre de protocoles de recherche clinique. (avis d’experts)
Cas particulier des lésions pré-infiltrantes ou peu invasives
Le choix des stratégies est encore en phase d’évaluation.
REFERENCE
- Aucune
OPTION (accord d’experts)
- Surveillance semestrielle selon des stratégies simples (anuscopie) ou complexes (tests virologiques, cytologie, anuscopie haute résolution) (Gross 2018).
6.7. Protocoles de chimiothérapie
En cas d’administration d’un protocole de chimiothérapie à base de fluoropyrimidines, la recherche d’un déficit partiel ou complet en DPD est obligatoire au préalable (HAS 2018, INCa 2018).
REFERENCE
- Recherche d’un déficit en DPD par phénotypage (dosage de l'uracilémie) avec ajustement des doses de 5FU et capécitabine en cas de déficit partiel et contre-indication du 5FU et de la capécitabine en cas de déficit complet (accord d’experts).
OPTION
- Génotypage du gène DPYD si phénotype DPD (uracilémie) anormal (avis d'experts).
5FU-mitomycine C
4 jours administrées de façon concomitantes, la 1ère et la 5ème semaine de la radiothérapie.
J1 : Mitomycine C : 10 mg/m2 en injection IV bolus.
J1 à J4 : 5-FU « infusionnel » : 1000 mg/m2/j en infusion IV continue (infuseur ou pompe).
Différentes variations de ce protocole sont possibles concernant :
- dose unitaire de mitomycine C (10 à 15 mg/m2)
- répétition de l’injection de mitomycine C lors de la seconde cure de chimiothérapie
- la durée de l’infusion intra-veineuse de 5-FU (4 ou 5 jours)
- posologie du 5FU (750 à 1000 mg/m2/j)
Capécitabine-mitomycine C
J1 : mitomycine C : 10 mg/m2 en injection IV bolus (uniquement pour la 1ère cure de chimiothérapie).
Capécitabine chaque jour de radiothérapie en deux administrations quotidiennes de 825 mg/m2 chacune.
5FU-cisplatine
5FU 800 mg/m2 en perfusion continue de J1 à J5 sur diffuseur portable.
Cisplatine 100 mg/m2 en 1h à J2.
Hydratation obligatoire avant et après le cisplatine :
- pré-hydratation : 2 litres de glucosé à 5 % + 4g NaCl / L + 2g KCl/L + 1g sulfate de magnésium/L à passer en 4 heures
- post-hydratation : 2 litres de glucosé à 5 % + 4g NaCl / litre + 2g KCl/L+ 1 ampoule de gluconate de calcium/L à passer en 4 heures
Traitement reproduit tous les 28 jours.
LV5FU2 simplifié-cisplatine
Cisplatine 50 mg/m2 à J1 en 30 minutes dans 250 mL de chlorure de sodium à 0,9 %.
Hydratation obligatoire avant et après le cisplatine :
- pré-hydratation : 1 litre de glucosé à 5% + 4g NaCl + 2g KCl + 1g sulfate de magnésium à passer en 3 heures
- post-hydratation : 1 litre de glucosé à 5% + 4g NaCl + 2g KCl + 1 ampoule de gluconate de calcium à passer en 3 heures
Acide folinique 400 mg/m2 (ou acide l-folinique 200 mg/m2) en 2 heures dans 250 mL de G5% à J1.
Rincer puis 5FU 400 mg/m2 en 10 minutes dans 100 mL de G5% à J1.
5FU 2400 mg/m2 en perfusion continue de 44 heures sur diffuseur portable.
Traitement reproduit tous les 14 jours.
DCF modifié
Docetaxel 40 mg/m2 et
Cisplatine 40 mg/m2 à J1
et 5FU 2400 mg/m2 en perfusion continue de 48 heures sur diffuseur portable.
Traitement reproduit tous les 14 jours par voie veineuse.
Carboplatine taxol Hebdomadaire
Paclitaxel 80 mg/m2 par semaine à J1, J8, J15 et
Carboplatine AUC 5 à J1
Traitement reproduit tous les 28 jours par voie veineuse.
6.8. Arbres décisionnels
6.8.1. Arbre décisionnel 1 (Tumeur T1N0)
T1N0
REFERENCES
- T1N0 marge anale : exérèse chirurgicale en marges saines (> 1mm)
- T1N0 canal anal avec franchissement de la membrane basale prouvé histologiquement : radiothérapie exclusive.
- T1N0 canal anal sans preuve du franchissement de la membrane basale è alors ce n’est pas un T1 mais une dysplasie sévère :
=> chirurgie d’exérèse (résection le long du sphincter interne)
OPTIONS
- T1N0 canal anal : en cas d’exérèse chirurgicale première, pas de radiothérapie post opératoire si taille tumorale < 1 mm et marges saines
- Si exérèse avec marge > 1 mm : reprise chirurgicale ou radiothérapie
ESSAI CLINIQUE
- Non
6.8.2. Arbre décisionnel 2 (Tumeur T2-T4 N0-N3)
T2-T4 N0-N3
REFERENCES
- Association chimio-radiothérapie concomitante exclusive 5FU-Mitomycine C
- Colostomie avant RTCT si risque de fistule pour limiter le risque d’infection
- Amputation abdomino-périnéale en l’absence d’évolution métastatique si :
- Mauvais répondeur / progression après chimio-radiothérapie
- Maladie persistante 6 mois après la fin de l’association chimio-radiothérapie
- Rechute locale après chimio-radiothérapie
- Fistule vaginale persistant après la fin de l’association chimio-radiothérapie
- Incontinence anale totale persistant après la fin de l’association chimio-radiothérapie
- Amputation abdomino-périnéale avec colostomie périnéale pseudo-continente pour les patients jeunes et /ou refusant une colostomie iliaque gauche
OPTIONS
- T2 «faible (<3cm)» N0 : radiothérapie exclusive
- Association FU-Cisplatine peut remplacer association 5FU-Mitomycine C
- Substitution du 5FU par de la capecitabine
ESSAI CLINIQUE
- KANALRAD PRODIGE 85 (Phase III)
6.8.3. Arbre décisionnel 3 (Tumeurs métastatiques)
Tumeurs métastatiques
REFERENCES
- Protocole mDCF (docétaxel-cisplatine-5FU) ou carboplatine-paclitaxel, si patient OMS 0-1
- Protocole carboplatine-paclitaxel si patient OMS 2
- Protocole 5FU cisplatine si contre-indication à taxanes
- En cas de bonne réponse à la chimiothérapie, discuter au cas par cas une chimio-radiothérapie de clôture à discuter au cas par cas pour améliorer le contrôle local et la qualité de vie
- En cas de métas ganglionnaires lombo-aortiques exclusives : chimio-radiothérapie concomitante incluant les aires ganglionnaires lombo-aortiques, plus ou moins précédée d’une chimiothérapie première
OPTIONS
- Colostomie de décharge en cas d’incontinence sphinctérienne majeure
- Chimiothérapie par LV5-FU2-cisplatine
- Patients oligo-métastatiques : chimio-radiothérapie normo-fractionnée et traitement ablatif des localisations secondaires (chirurgie, radiothérapie stéréotaxique, thermoablation).
ESSAIS CLINIQUES
- Etude SPARTANA
- Etude PEVOsq
6.8.4. Arbre décisionnel 4 (Surveillance)
Surveillance
REFERENCES
- Examen clinique complet (toucher rectal, anuscopie et palpation des aires inguinales bilatérales)
- Sur 5 ans : tous les 4 mois pendant 2 ans puis tous les 6 mois pendant 3 ans
- Les biopsies sont proscrites en cas de réponse complète clinico-radiologique
- En cas de tumeur volumineuse, et en l’absence de progression clinique il est souhaitable d’attendre au moins 6 mois avant de réaliser une biopsie d’un éventuel résidu tumoral
- Si suspicion de rechute locale : biopsie au trucut (éviter biopsie chirurgicale)
- Scanner TAP annuel et/ou IRM pelvienne
OPTIONS
- IRM et TEP scanner avant chirurgie de rattrapage
- TEP scanner 4 à 6 mois après la fin du traitement
- Dosage des SCC sériques
6.9. Bibliographie
- Abramowitz L, Jacquard AC, Jaroud F, Haesebaert J, Siproudhis L, Pradat P, et al. Human papillomavirus genotype distribution in anal cancer in France: the EDiTH V study. Int J Cancer 2011;129:433-9.
- Abramowitz L, Mathieu N, Roudot-Thoraval F, Lemarchand N, Bauer P, Hennequin C, et al. Epidermoid anal cancer prognosis comparison among HIV+ and HIV- patients. Aliment Pharmacol Ther 2009;30:414-21.
- Ajani JA, Winter KA, Gunderson LL, Pedersen J, Benson AB, III, Thomas CR, Jr., et al. Fluorouracil, mitomycin, and radiotherapy vs fluorouracil, cisplatin, and radiotherapy for carcinoma of the anal canal: a randomized controlled trial. JAMA 2008;299:1914-21.
- AJCC. Anal Canal. 2011;7th:106-9.
- American Cancer Society. Key Statistics for Anal Cancer (2017-2020). 2017.
- Amin MB, Edge S, Greene F, Byrd DR, Brookland RK, Washington MK, et al. AJCC Cancer Staging Manual. 2017;8th.
- Anon. Common terminology criteria for adverse events (CTCAE). National Cancer Institute, Bethesda, MD 2010;Version 4.03.
- Anon. Cooperative Group Common Toxicity Criteria. Radiation Therapy Oncology Group (RTOG), Philadelphia, PA 2015.
- Bacci M, Quero L, Barbier E, Parrot L, Juguet F, Pommier P, et al.What is the optimal treatment for T1N0 anal squamous cell carcinoma? Analysis of current practices in the prospective French FFCD ANABASE cohort. Dig Liver Dis. 2021;53(6):776-784.
- Bartelink H, Roelofsen F, Eschwege F, Rougier P, Bosset JF, Gonzalez DG, et al. Concomitant radiotherapy and chemotherapy is superior to radiotherapy alone in the treatment of locally advanced anal cancer: results of a phase III randomized trial of the European Organization for Research and Treatment of Cancer Radiotherapy and Gastrointestinal Cooperative Groups. J Clin Oncol 1997;15:2040-9.
- Beets-Tan RGH, Lambregts DMJ, Maas M, Bipat S, Barbaro B, Curvo-Semedo L, et al. Magnetic resonance imaging for clinical management of rectal cancer: Updated recommendations from the 2016 European Society of Gastrointestinal and Abdominal Radiology (ESGAR) consensus meeting. Eur Radiol 2018;28:1465-75.
- Bernard-Tessier A, Jeannot E, Guenat D, Debernardi A, Michel M, Proudhon C, et al. Clinical Validity of HPV Circulating Tumor DNA in Advanced Anal Carcinoma: An Ancillary Study to the Epitopes-HPV02 Trial. Clin Cancer Res 2019;25:2109-15.
- Besnard C, Lemanski C , Vendrely V [Radiation-induced sexual toxicity] Cancer Radiother. 2021;25(8):816-821.
- Bhuva NJ, Glynne-Jones R, Sonoda L, Wong WL, Harrison MK. To PET or not to PET? That is the question. Staging in anal cancer. Ann Oncol 2012;23:2078-82.
- Cabel L, Jeannot E, Bieche I, Vacher S, Callens C, Bazire L, et al. Prognostic Impact of Residual HPV ctDNA Detection after Chemoradiotherapy for Anal Squamous Cell Carcinoma. Clin Cancer Res 2018;24:5767-71.
- Camprodon G, Huguet F.Unrecognized digestive toxicities of radiation therapy Cancer Radiother2021;25(6-7):723-728.
- Clifford GM, Georges D, Shiels MS, Engels EA, Albuquerque A, Poynten IM, de Pokomandy A, Easson AM, Stier EA. A meta-analysis of anal cancer incidence by risk group: Toward a unified anal cancer risk scale. Int J Cancer. 2021 Jan 1;148(1):38-47. doi: 10.1002/ijc.33185. Epub 2020 Jul 29. PMID: 32621759; PMCID: PMC7689909.
- Coghill AE, Shiels MS, Suneja G, Engels EA. Elevated Cancer-Specific Mortality Among HIV-Infected Patients in the United States. J Clin Oncol 2015;33:2376-83.
- Combet-Curt V, Buchalet C, Le Malicot K, Lemanski C, Deshayes E, Bonichon-Lamichhane N,et al. Prognostic Value of 18F-FDG PET/CT Assessment After Radiotherapy of Squamous Cell Carcinoma of the Anus in Patients from the National Multicentric Cohort FFCD-ANABASE. J Nucl Med. 2024 Aug 1;65(8):1194-1201.
- Daling JR, Madeleine MM, Johnson LG, Schwartz SM, Shera KA, Wurscher MA, et al. Human papillomavirus, smoking, and sexual practices in the etiology of anal cancer. Cancer 2004;101:270-80.
- Dapper H, Schiller K, Münch S, Peeken JC, Borm K, Weber W, et al.Have we achieved adequate recommendations for target volume definitions in anal cancer? A PET imaging based patterns of failure analysis in the context of established contouring guidelines, BMC Cancer. 2019; 19: 742.
- Deenen MJ, Dewit L, Boot H, Beijnen JH, Schellens JH, Cats A. Simultaneous integrated boost-intensity modulated radiation therapy with concomitant capecitabine and mitomycin C for locally advanced anal carcinoma: a phase 1 study. Int J Radiat Oncol Biol Phys 2013;85:e201-e207.
- Fenger C, Frisch M, Marti MC, Parc R. Tumours of the anal canal. Pathology and Genetic Tumors of the Digestive System. Pathology and Genetics 2000;2:145-55.
- Flam M, John M, Pajak TF, Petrelli N, Myerson R, Doggett S, et al. Role of mitomycin in combination with fluorouracil and radiotherapy, and of salvage chemoradiation in the definitive nonsurgical treatment of epidermoid carcinoma of the anal canal: results of a phase III randomized intergroup study. J Clin Oncol 1996;14:2527-39.
- FNCLCC. Enquête Permanente Cancer 1976-1989: survie à long terme des malades traités pour cancer. Monographie FNCLCC 1992.
- Fraunholz I, Rabeneck D, Gerstein J, Jack K, Haberl A, Weiss C, et al. Concurrent chemoradiotherapy with 5-fluorouracil and mitomycin C for anal carcinoma: are there differences between HIV-positive and HIV-negative patients in the era of highly active antiretroviral therapy? Radiother Oncol 2011;98:99-104.
- Frisch M, Biggar RJ, Goedert JJ. Human papillomavirus-associated cancers in patients with human immunodeficiency virus infection and acquired immunodeficiency syndrome. J Natl Cancer Inst 2000;92:1500-10.
- Frisch M. On the etiology of anal squamous carcinoma. Dan Med Bull 2002;49:194-209.
- Fuchshuber PR, Rodriguez-Bigas M, Weber T, Petrelli NJ. Anal canal and perianal epidermoid cancers. J Am Coll Surg 1997;185:494-505.
- Garg M. Phase II trials of cetuximab plus combined modality therapy (CMT) in squamous cell carcinoma of the anal canal (SCCAC) with and without human immunodeficiency virus (HIV) infection. ASCO Meeting 2016 2016.
- Giovannini M, Bardou VJ, Barclay R, Palazzo L, Roseau G, Helbert T, et al. Anal carcinoma: prognostic value of endorectal ultrasound (ERUS). Results of a prospective multicenter study. Endoscopy 2001;33:231-6.
- Glynne-Jones R, Meadows H, Wan S, Gollins S, Leslie M, Levine E, et al. EXTRA--a multicenter phase II study of chemoradiation using a 5 day per week oral regimen of capecitabine and intravenous mitomycin C in anal cancer. Int J Radiat Oncol Biol Phys 2008;72:119-26.
- Glynne-Jones R, Nilsson PJ, Aschele C, Goh V, Peiffert D, Cervantes A, et al. Anal cancer: ESMO-ESSO-ESTRO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2014;25 Suppl 3:iii10-iii20.
- Glynne-Jones R, Sebag-Montefiore D, Meadows HM, Cunningham D, Begum R, Adab F, et al. Best time to assess complete clinical response after chemoradiotherapy in squamous cell carcinoma of the anus (ACT II): a post-hoc analysis of randomised controlled phase 3 trial. Lancet Oncol 2017;18:347-56.
- Glynne-Jones : Glynne-Jones R, Meadows HM, Lopes A, Muirhead R, Sebag-Montefiore D, Adams R; ACTII study group. Impact of compliance to chemoradiation on long-term outcomes in squamous cell carcinoma of the anus: results of a post hoc analysis from the randomised phase III ACT II trial. Ann Oncol. 2020;31:1376-1385
- Goere D, Bonnet S, Pocard M, Deutsch E, Lasser P, Elias D. Oncologic and functional results after abdominoperineal resection plus pseudocontinent perineal colostomy for epidermoid carcinoma of the anus. Dis Colon Rectum 2009;52:958-63.
- Goldman S, Svensson C, Bronnergard M, Glimelius B, Wallin G. Prognostic significance of serum concentration of squamous cell carcinoma antigen in anal epidermoid carcinoma. Int J Colorectal Dis 1993;8:98-102.
- Gross GE, Werner RN, Becker JC, Brockmeyer NH, Esser S, Hampl M, et al. S2k guideline: HPV-associated lesions of the external genital region and the anus - anogenital warts and precancerous lesions of the vulva, the penis, and the peri- and intra-anal skin (short version). J Dtsch Dermatol Ges 2018;16:242-55.
- Gunderson LL, Winter KA, Ajani JA, Pedersen JE, Moughan J, Benson AB, III, et al. Long-term update of US GI intergroup RTOG 98-11 phase III trial for anal carcinoma: survival, relapse, and colostomy failure with concurrent chemoradiation involving fluorouracil/mitomycin versus fluorouracil/cisplatin. J Clin Oncol 2012;30:4344-51.
- Hannoun-Levi JM, Ortholan C, Resbeut M, Teissier E, Ronchin P, Cowen D, et al. High-dose split-course radiation therapy for anal cancer: outcome analysis regarding the boost strategy (CORS-03 study). Int J Radiat Oncol Biol Phys 2011;80:712-20.
- HAS, INCa. Des recommandations pour prévenir certaines toxicités sévères des chimiothérapies par fluoropyrimidines. 2018.
- Haute Autorité de Santé. Radiothérapie conformationnelle avec modulation d'intensité dans le cancer anal. Actualisation du rapport de 2006. 2015.
- Hillman RJ, Berry-Lawhorn JM, Ong JJ, Cuming T, Nathan M, Goldstone S, Richel O, Barrosso LF, Darragh TM, Law C, Bouchard C, Stier EA, Palefsky JM, Jay N; International Anal Neoplasia Society. International Anal Neoplasia Society Guidelines for the Practice of Digital Anal Rectal Examination. J Low Genit Tract Dis. 2019 Apr;23(2):138-146
- Hoffman R, Welton ML, Klencke B, Weinberg V, Krieg R. The significance of pretreatment CD4 count on the outcome and treatment tolerance of HIV-positive patients with anal cancer. Int J Radiat Oncol Biol Phys 1999;44:127-31.
- Iagaru A, Kundu R, Jadvar H, Nagle D. Evaluation by 18F-FDG-PET of patients with anal squamous cell carcinoma. Hell J Nucl Med 2009;12:26-9.
- INCa, HAS. Des recommandations pour prévenir certaines toxicités sévères des chimiothérapies par fluoropyrimidines. 2018.
- James RD, Glynne-Jones R, Meadows HM, Cunningham D, Myint AS, Saunders MP, et al. Mitomycin or cisplatin chemoradiation with or without maintenance chemotherapy for treatment of squamous-cell carcinoma of the anus (ACT II): a randomised, phase 3, open-label, 2 x 2 factorial trial. Lancet Oncol 2013;14:516-24.
- Janczewski LM, Asare EA, Goodman KA. Updates on the Version 9 American Joint Committee on Cancer Staging System for Anal Cancer. Ann Surg Oncol. 2024;31:4155-4158.
- Jemal A, Simard EP, Dorell C, Noone AM, Markowitz LE, Kohler B, et al. Annual Report to the Nation on the Status of Cancer, 1975-2009, featuring the burden and trends in human papillomavirus(HPV)-associated cancers and HPV vaccination coverage levels. J Natl Cancer Inst 2013;105:175-201.
- Kachnic LA, Tsai HK, Coen JJ, Blaszkowsky LS, Hartshorn K, Kwak EL, et al. Dose-painted intensity-modulated radiation therapy for anal cancer: a multi-institutional report of acute toxicity and response to therapy. Int J Radiat Oncol Biol Phys 2012;82:153-8.
- Kachnic LA, Winter K, Myerson RJ, Goodyear MD, Willins J, Esthappan J, et al. RTOG 0529: a phase 2 evaluation of dose-painted intensity modulated radiation therapy in combination with 5-fluorouracil and mitomycin-C for the reduction of acute morbidity in carcinoma of the anal canal. Int J Radiat Oncol Biol Phys 2013;86:27-33.
- Kauh J, Koshy M, Gunthel C, Joyner MM, Landry J, Thomas CR, Jr. Management of anal cancer in the HIV-positive population. Oncology (Williston Park ) 2005;19:1634-8.
- Kim S, Francois E, Andre T, Samalin E, Jary M, El HF, et al. Docetaxel, cisplatin, and fluorouracil chemotherapy for metastatic or unresectable locally recurrent anal squamous cell carcinoma (Epitopes-HPV02): a multicentre, single-arm, phase 2 study. Lancet Oncol 2018;19:1094-106.
- Kim S, Meurisse A, Spehner L, Stouvenot M, François E, Buecher B, et al. Pooled analysis of 115 patients from updated data of Epitopes-HPV01 and Epitopes-HPV02 studies in first-line advanced anal squamous cell carcinoma. Ther Adv Med Oncol. 2020 Dec 4;12:1758835920975356. doi: 10.1177/1758835920975356. PMID: 33329760; PMCID: PMC7720302.
- Kim S, Vendrely V, Saint A, André T, Vaflard P, Samalin E, et al. DCF versus doublet chemotherapy as first-line treatment of advanced squamous anal cell carcinoma: a multicenter propensity score-matching study. Exp Hematol Oncol. 2023 Jul 21;12(1):63. doi: 10.1186/s40164-023-00413-2. PMID: 37480095; PMCID: PMC10362607.
- Kim S, Ghiringhelli F, De La Fouchardiere C, Francois E, Smith D, Samalin E, et al. Atezolizumab plus modified DCF (docetaxel, cisplatin, and 5-fluorouracil) as first-line treatment for metastatic or locally advanced squamous cell anal carcinoma: A SCARCE-PRODIGE 60 randomized phase II study. Lancet Oncol 2024 (sous presse).
- Koerber SA, Schoneweg C, Slynko A, Krug D, Haefner MF, Herfarth K, et al. Influence of human papillomavirus and p16(INK4a) on treatment outcome of patients with anal cancer. Radiother Oncol 2014;113:331-6.
- Koh DM, Dzik-Jurasz A, O'Neill B, Tait D, Husband JE, Brown G. Pelvic phased-array MR imaging of anal carcinoma before and after chemoradiation. Br J Radiol 2008;81:91-8.
- Lefevre JH, Corte H, Tiret E, Boccara D, Chaouat M, Touboul E, et al. Abdominoperineal resection for squamous cell anal carcinoma: survival and risk factors for recurrence. Ann Surg Oncol 2012;19:4186-92.
- Lepinoy A, Lescut N, Puyraveau M, Caubet M, Boustani J, Lakkis Z, et al. Evaluation of a 36 Gy elective node irradiation dose in anal cancer. Radiother Oncol 2015;116:197-201.
- Levy A, Azria D, Pignon JP, Delarochefordiere A, Martel-Lafay I, Rio E, et al. Low response rate after cetuximab combined with conventional chemoradiotherapy in patients with locally advanced anal cancer: long-term results of the UNICANCER ACCORD 16 phase II trial. Radiother Oncol 2015;114:415-6.
- Lim F, Glynne-Jones R. Chemotherapy/chemoradiation in anal cancer: a systematic review. Cancer Treat Rev 2011;37:520-32.
- Mahmud A, Poon R, Jonker D. PET imaging in anal canal cancer: a systematic review and meta-analysis. Br J Radiol 2017;90:20170370.
- Mariani P, Ghanneme A, De la Rochefordiere A, Girodet J, Falcou MC, Salmon RJ. Abdominoperineal resection for anal cancer. Dis Colon Rectum 2008;51:1495-501.
- Meillan N, Huguet F, Peiffert D. Suivi après radiothérapie d'un cancer du canal anal. Cancer Radiother 2015;19:610-5.
- Meulendijks D, Dewit L, Tomasoa NB, van TH, Beijnen JH, Schellens JH, et al. Chemoradiotherapy with capecitabine for locally advanced anal carcinoma: an alternative treatment option. Br J Cancer 2014;111:1726-33.
- Meulendijks D, Tomasoa NB, Dewit L, Smits PH, Bakker R, van Velthuysen ML, et al. HPV-negative squamous cell carcinoma of the anal canal is unresponsive to standard treatment and frequently carries disruptive mutations in TP53. Br J Cancer 2015;112:1358-66.
- Mistrangelo M, Pelosi E, Bello M, Castellano I, Cassoni P, Ricardi U, et al. Comparison of positron emission tomography scanning and sentinel node biopsy in the detection of inguinal node metastases in patients with anal cancer. Int J Radiat Oncol Biol Phys 2010;77:73-8.
- Morris VK, Salem ME, Nimeiri H, Iqbal S, Singh P, Ciombor K, et al. Nivolumab for previously treated unresectable metastatic anal cancer (NCI9673): a multicentre, single-arm, phase 2 study. Lancet Oncol 2017;18:446-53.
- Moureau-Zabotto L, Vendrely V, Abramowitz L, Borg C, Francois E, Goere D, Huguet F, Peiffert D, Siproudhis L, Ducreux M, Bouché O. Anal cancer: French Intergroup Clinical Practice Guidelines for diagnosis, treatment and follow-up (SNFGE, FFCD, GERCOR, UNICANCER, SFCD, SFED, SFRO, SNFCP). Dig Liver Dis. 2017 Aug;49(8):831-840.
- Moureau-Zabotto L, Ortholan C, Hannoun-Levi JM, Teissier E, Cowen D, Salem N, et al. Role of brachytherapy in the boost management of anal carcinoma with node involvement (CORS-03 study). Int J Radiat Oncol Biol Phys 2013;85:e135-e142.
- National Comprehensive Cancer Network (NCCN). Clinical Practice Guidelines in Oncology. NCCN Clinical Practice Guidelines in Oncology 2014.
- National Comprehensive Cancer Network (NCCN). Guidelines for Anal Carcinoma. 2014;Version 2.2014.
- Ng M, Leong T, Chander S, Chu J, Kneebone A, Carroll S, et al. Australasian Gastrointestinal Trials Group (AGITG) contouring atlas and planning guidelines for intensity-modulated radiotherapy in anal cancer. Int J Radiat Oncol Biol Phys 2012;83:1455-62.
- No Authors. Epidermoid anal cancer: results from the UKCCCR randomised trial of radiotherapy alone versus radiotherapy, 5-fluorouracil, and mitomycin. UKCCCR Anal Cancer Trial Working Party. UK Co-ordinating Committee on Cancer Research. Lancet 1996;348:1049-54.
- Northover J, Glynne-Jones R, Sebag-Montefiore D, James R, Meadows H, Wan S, et al. Chemoradiation for the treatment of epidermoid anal cancer: 13-year follow-up of the first randomised UKCCCR Anal Cancer Trial (ACT I). Br J Cancer 2010;102:1123-8.
- Ortholan C, Resbeut M, Hannoun-Levi JM, Teissier E, Gerard JP, Ronchin P, et al. Anal canal cancer: management of inguinal nodes and benefit of prophylactic inguinal irradiation (CORS-03 Study). Int J Radiat Oncol Biol Phys 2012;82:1988-95.
- Ott PA, Piha-Paul SA, Munster P, Pishvaian MJ, van Brummelen EMJ, Cohen RB, et al. Safety and antitumor activity of the anti-PD-1 antibody pembrolizumab in patients with recurrent carcinoma of the anal canal. Ann Oncol 2017;28:1036-41.
- Ott PA, Piha-Paul SA, Munster P, and al. Safety and antitumor activity of the anti-PD-1 antibody pembrolizumab in patients with recurrent carcinoma of the anal canal. Ann Oncol 2017 ;28: 1036–1041,
- Otto SD, Lee L, Buhr HJ, Frericks B, Hocht S, Kroesen AJ. Staging anal cancer: prospective comparison of transanal endoscopic ultrasound and magnetic resonance imaging. J Gastrointest Surg 2009;13:1292-8.
- Parikh J, Shaw A, Grant LA, Schizas AM, Datta V, Williams AB, et al. Anal carcinomas: the role of endoanal ultrasound and magnetic resonance imaging in staging, response evaluation and follow-up. Eur Radiol 2011;21:776-85.
- Peiffert D, Huguet F, Vendrely V, Moureau-Zabotto L, Rivin Del Campo E, Créhange G, et al. Radiotherapy of anal canal cancer. Cancer Radiother. 2022 ;26:279-285.
- Peiffert D, Tournier-Rangeard L, Gerard JP, Lemanski C, Francois E, Giovannini M, et al. Induction chemotherapy and dose intensification of the radiation boost in locally advanced anal canal carcinoma: final analysis of the randomized UNICANCER ACCORD 03 trial. J Clin Oncol 2012;30:1941-8.
- Penn I. Cancers of the anogenital region in renal transplant recipients. Analysis of 65 cases. Cancer 1986;58:611-6.
- Piketty C, Selinger-Leneman H, Bouvier AM, Belot A, Mary-Krause M, Duvivier C, et al. Incidence of HIV-related anal cancer remains increased despite long-term combined antiretroviral treatment: results from the french hospital database on HIV. J Clin Oncol 2012;30:4360-6.
- Rao S, Sclafani F, Eng C, Adams RA, Guren MG, Sebag-Montefiore D, et al. International Rare Cancers Initiative Multicenter Randomized Phase II Trial of Cisplatin and Fluorouracil versus Carboplatin and Paclitaxel in Advanced Anal Cancer: InterAAct. J Clin Oncol. 2020 ;1;38(22):2510-2518
- Rao S, Guren MG, Khan K, Brown G, Renehan AG, Steigen SE,et al. ESMO Guidelines Committee. Anal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021;32(9):1087-1100.
- Rao S, Samalin-Scalzi E, Evesque L, Ben Abdelghani M, Morano F, Roy AC, Dahan L, et al. POD1UM-303/InterAACT 2: Phase III study of retifanlimab with carboplatin-paclitaxel (c-p) in patients (Pts) with inoperable locally recurrent or metastatic squamous cell carcinoma of the anal canal (SCAC) not previously treated with systemic chemotherapy (Chemo). Annf Oncol 2024 ; 35 (suppl_2): 1-72. 10.1016/annonc/annonc1623
- Robinson P, Carrington BM, Swindell R, Shanks JH, O'dwyer ST. Recurrent or residual pelvic bowel cancer: accuracy of MRI local extent before salvage surgery. Clin Radiol 2002;57:514-22.
- Rouquie D, Lasser P, Castaing M, Boige V, Goere D, Pignon JP, et al. Résection R0, seul facteur pronostique dans les amputations abdominopérinéales de rattrapage des cancers du canal anal (série consécutive de 95 patients). J Chir (Paris) 2008;145:335-40.
- Serup-Hansen E, Linnemann D, Skovrider-Ruminski W, Hogdall E, Geertsen PF, Havsteen H. Human papillomavirus genotyping and p16 expression as prognostic factors for patients with American Joint Committee on Cancer stages I to III carcinoma of the anal canal. J Clin Oncol 2014;32:1812-7.
- Siegel R, Naishadham D, Jemal A. Cancer statistics, 2013. CA Cancer J Clin 2013;63:11-30.
- Spindler L, Etienney I, Abramowitz L, de Parades V, Pigot F, Siproudhis L,et al; Société Nationale Française de Colo-Proctologie. Screening for precancerous anal lesions linked to human papillomaviruses: French recommendations for clinical practice. Tech Coloproctol. 2024 Jan 10;28(1):23.
- Stewart DB, Gaertner WB, Glasgow SC, Herzig DO, Feingold D, Steele SR; Prepared on Behalf of the Clinical Practice Guidelines Committee of the American Society of Colon and Rectal Surgeons. The American Society of Colon and Rectal Surgeons Clinical Practice Guidelines for Anal Squamous Cell Cancers (Revised 2018). Dis Colon Rectum. 2018 Jul;61(7):755-774
- Trautmann TG, Zuger JH. Positron Emission Tomography for pretreatment staging and posttreatment evaluation in cancer of the anal canal. Mol Imaging Biol 2005;7:309-13.
- Valmary-Degano S, Jacquin E, Pretet JL, Monnien F, Girardo B, Arbez-Gindre F, et al. Signature patterns of human papillomavirus type 16 in invasive anal carcinoma. Hum Pathol 2013;44:992-1002.
- Vendrely V, Lemanski C, Gnep K, Barbier E, Hajbi FE, Lledo G, Dahan L, Terrebonne E, Manfredi S, Mirabel X, Mammar V, Cowen D, Lepage C, Aparicio T; for FFCD investigators/Collaborators. Anti-epidermal growth factor receptor therapy in combination with chemoradiotherapy for the treatment of locally advanced anal canal carcinoma: Results of a phase I dose-escalation study with panitumumab (FFCD 0904). Radiother Oncol. 2019 Nov;140:84-89
- Weber DC, Kurtz JM, Allal AS. The impact of gap duration on local control in anal canal carcinoma treated by split-course radiotherapy and concomitant chemotherapy. Int J Radiat Oncol Biol Phys 2001;50:675-80.
- Wells IT, Fox BM. PET/CT in anal cancer - is it worth doing? Clin Radiol 2012;67:535-40.
- Zilli T, Schick U, Ozsahin M, Gervaz P, Roth AD, Allal AS. Node-negative T1-T2 anal cancer: radiotherapy alone or concomitant chemoradiotherapy? Radiother Oncol 2012;102:62-7.

