8. Cancer des voies biliaires
(Dernière mise à jour le : )Groupe de travail et relecteurs
Groupe de travail :
D. MALKA (Paris), coordonnateur,
J.-F. BLANC (Bordeaux), E. BOLESLAWSKI (Lille), K. BOUDJEMA (Rennes), A.-L. BRETAGNE-BIGNON (Caen), M. CAMUS-DUBOC (Paris), R. CORIAT (Paris), G. CREHANGE (Paris), T. DE BAERE (Villejuif), C. de la FOUCHARDIERE (Lyon), C. DROMAIN (Lausanne), J. EDELINE (Rennes), M. GELLI (Villejuif), B. GUIU (Montpellier), S. HORN (Lyon), V. LAURENT-CROISE (Nancy), C. LEPAGE (Dijon), A. LIEVRE (Rennes), A. LOPEZ (Nancy), S. MANFREDI (Dijon), J. MEILLEROUX (Toulouse), C. NEUZILLET (Saint-Cloud), V. PARADIS (Clichy), F. PRAT (Paris), M. RONOT (Clichy), O. ROSMORDUC (Villejuif), G. ROTH (Grenoble), A. SA CUNHA (Villejuif), M. SARABI (Lyon), O. SOUBRANE (Paris), A.TURPIN (Lille), L VERLINGUE (Lyon).
Relecteurs :
T. APARICIO (Paris), L. BENHAIM (Paris), O. BOUCHE (Reims), S. CATTAN (Lille), L. CHICHE-BENSADOUN (Bordeaux), M. DUCREUX (Villejuif), A. DUPRE (Lyon), H. ETIENNE (Albi), A. HEURGUE (Reims), F. HUGUET (Paris), J.-L. JOUVE (Dijon), T. LECOMTE (Tours), C. LOUVET (Paris), N. MAGNE (Lyon), P. MARIANI (Paris), B. MENAHEN (Caen), L. MOSSER (Rodez), G. PASSOT (Lyon), C. SILVAIN (Poitiers), B. SUC (Toulouse).
Ce travail est dédié à la mémoire du Dr Marine Gilabert.
Comment citer ce chapitre du TNCD :
Roth GS, Verlingue L, Sarabi M, Blanc JF, Boleslawski E, Boudjema K, Bretagne-Bignon AL, Camus-Duboc M, Coriat R, Créhange G, De Baere T, de la Fouchardière C, Dromain C, Edeline J, Gelli M, Guiu B, Horn S, Laurent-Croise V, Lepage C, Lièvre A, Lopez A, Manfredi S, Meilleroux J, Neuzillet C, Paradis V, Prat F, Ronot M, Rosmorduc O, Cunha AS, Soubrane O, Turpin A, Louvet C, Bouché O, Malka D. Biliary tract cancers: French national clinical practice guidelines for diagnosis, treatments and follow-up (TNCD, SNFGE, FFCD, UNICANCER, GERCOR, SFCD, SFED, AFEF, SFRO, SFP, SFR, ACABi, ACHBPT). Eur J Cancer. 2024 May;202:114000. doi: 10.1016/j.ejca.2024.114000. Epub 2024 Mar 13. PMID: 38493667.
8.1. Introduction
8.1.1. Epidémiologie
Si l’incidence des cholangiocarcinomes dans les pays à revenu élevé, estimée entre 0,35 et 2/100 000 par an (Banales 2016, GLOBOCAN 2017), est jusqu’à 40 fois plus faible que dans les régions asiatiques d’endémie de distomatoses, l'incidence des cholangiocarcinomes intra-hépatiques y augmente nettement (celle des cholangiocarcinomes extra-hépatiques variant peu) (Patel 2001, Shaib 2004, Saha 2016, Florio 2020). L’incidence exacte des différents types de cholangiocarcinome est toutefois difficile à évaluer car : 1) les cholangiocarcinomes péri-hilaires ont été classés à tort comme cholangiocarcinomes intra-hépatiques au cours des changements successifs de la Classification Internationale des Maladies (CIM) (Welzel 2006). Les codes spécifiques pour les cholangiocarcinomes intra-hépatiques (2C12.10), hilaires (2C18.0), distaux (2C15.0) et les adénocarcinomes de la vésicule biliaire (2C13.0) de la nouvelle classification CIM-11 devrait permettre d’harmoniser les futures données épidémiologiques (WHO 2019); 2) les cholangiocarcinomes intra-hépatiques peuvent être classés à tort parmi les cancers de primitif inconnu ou confondus avec des carcinomes hépatocellulaires (Hainsworth 2013).
Les cholangiocarcinomes intra-hépatiques représentent 15% des cancers primitifs du foie, au deuxième rang après les carcinomes hépatocellulaires (Lepage 2011, Rumgay 2022). Cette proportion est plus importante chez les femmes, notamment en Europe du Nord (59%) et de l’Ouest (40%) (Rumgay 2022). L’incidence en France était de 1,6 cas pour 100 000 personnes-années en 2018 (hommes : 2,2 ; femmes : 1,1) (Rumgay 2022).
Les cancers de la vésicule biliaire et des voies biliaires extra‑hépatiques sont des cancers peu fréquents. Leur incidence estimée en 2018 dans le monde était de 2,1 chez l'homme et de 2,4 chez la femme pour 100 000 personnes‑années. Les zones à forte incidence étaient en Amérique du Sud et en Asie. En France, en 2018, l'incidence était de 2,1 chez l'homme (progression de 1,1 % durant la période 1990-2018) et 1,4 chez la femme (diminution de 1,2 %, conduisant à une inversion du sexe‑ratio au cours du temps passant de 0,8 à 1,5) ; le nombre de nouveaux cas estimés en 2018 est de 2965 (Defossez 2019). L'âge médian au diagnostic est de 72 ans chez l'homme et de 78 ans chez la femme, avec une forte progression des taux d’incidence à partir de l’âge de 50 ans dans les deux sexes mais plus marquée chez les hommes. Le risque d’être atteint de ce cancer entre 0 et 74 ans varie peu chez l'homme (de 0,2 % à 0,3 %) comme chez la femme (de 0,3 % à 0,2 %) selon la cohorte de naissance.
Une inflammation chronique hépatique ou biliaire sous-tend les principaux facteurs de risque de cancer biliaire (Clements 2020) : 1) en zones d’endémie (Thaïlande, Chine, Corée, Taiwan, Vietnam), les parasitoses biliaires (distomatoses à Opisthorchis viverrini ou Clonorchis sinensis) (Sithithaworn 2014) ; 2) la lithiase hépatique, cholédocienne (cholangiocarcinome) ou vésiculaire. Si 70% à 90% des patients atteints de cancer de la vésicule biliaire ont des antécédents de lithiase biliaire, seuls 0,5% à 3% des individus porteurs de calculs développeront un cancer de la vésicule biliaire (Hsing 2007). L’impact de la diffusion de la cholécystectomie par laparoscopie sur la diminution d'incidence du cancer de la vésicule biliaire, notamment chez les femmes, est discuté (Castro 2013, Kilander 2018) ; 3) la cholangite sclérosante primitive (Lewis 2007, Chascsa 2019, Said 2008) ; 4) les anomalies structurelles ou acquises de l'arbre biliaire : anomalies de la jonction bilio-pancréatique, kystes du cholédoque (Kamisawa 2017), maladie de Caroli, papillomatose biliaire et complexes de Von Meyenbourg, drainage biliaire chirurgical ; 5) les infections chroniques à Salmonella typhi ou Helicobacter bilis (Koshiol 2016) ; 6) les hépatopathies liées à l’obésité ou au diabète (Li 2016) ; 7) les infections VHB et VHC ; 8) globalement, la fibrose, l’inflammation hépatique et surtout la cirrhose (Palmer 2012, Rizvi 2013, Clements 2020). Les rôles du tabac, de l'alcool et des antécédents hormonaux et reproductifs chez les femmes ont également été évoqués. Toutefois, la plupart des patients atteints de cholangiocarcinome ne présentent aucun facteur de risque identifiable.
Les cancers biliaires continuent d’avoir un pronostic sombre, sans grande amélioration sur les 30 dernières années en termes de résécabilité ou de diagnostic précoce, avec des taux de survie relative à 1, 3 et 5 ans de 25 %, 10 % et 7 % respectivement dans l’étude du registre Bourguignon des cancers (Lepage 2011).
Les données de PMSI portant sur 3650 cholangiocarcinomes intra-hépatiques diagnostiqués en France en 2014 et 2015 montrent que 65 % des patients n’ont pu avoir accès qu’à des soins de support et que 25 % des patients sont décédés lors de leur première hospitalisation (Neuzillet 2022). Même si le diagnostic est clairement souvent trop tardif, la question d’une prise en charge initiale sous-optimale est posée et doit amener à réfléchir au parcours de soins des patients. L’accès rapide et précoce à des équipes multidisciplinaires ayant une expertise dans les tumeurs hépato-biliaires est ainsi fondamentale.
8.2. Classifications
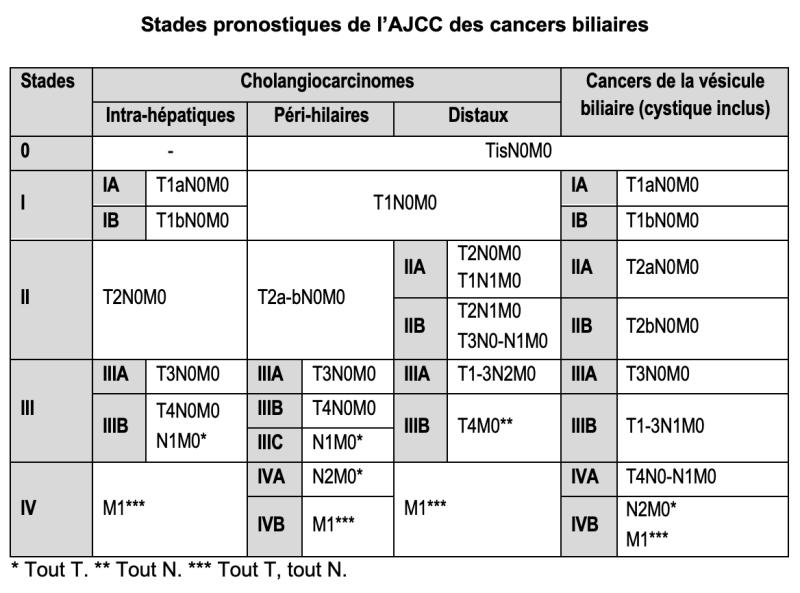
Les cancers biliaires Les cancers biliaires doivent être classés selon la classification TNM-AJCC-UICC (Amin 2017) (tableaux 1a et 1b) en fonction de leur localisation : a) cholangiocarcinomes, eux-mêmes subdivisés en 3 sous-types : 1) intra-hépatiques (anciennement « périphériques »), développés aux dépens des voies biliaires intra-hépatiques de deuxième ordre. Morphologiquement, on distingue les cholangiocarcinomes intra-hépatiques à petits et à grands canaux. Les cholangiolocarcinomes, précédemment intégrés dans les tumeurs mixtes/hépatocholangiocarcinomes, sont maintenant classés dans ce sous-type ; 2) péri-hilaires (anciennement tumeurs de Klatskin), développés aux dépens des canaux – ou conduits selon la classification internationale – hépatiques commun, droit et/ou gauche ; 3) distaux, développés sur le cholédoque en aval de l'insertion du canal cystique. Les cholangiocarcinomes péri-hilaires et distaux sont souvent regroupés en cholangiocarcinomes extra-hépatiques, appellation actuellement déconseillée. Les cholangiocarcinomes mixte/hépatocholangiocarcinomes sont classés à part ; b) carcinomes de la vésicule biliaire ; c) carcinomes de l’ampoule de Vater (traités dans le chapitre 19 du TNCD https://www.snfge.org/content/19-tumeurs-de-lampoule-de-vater).
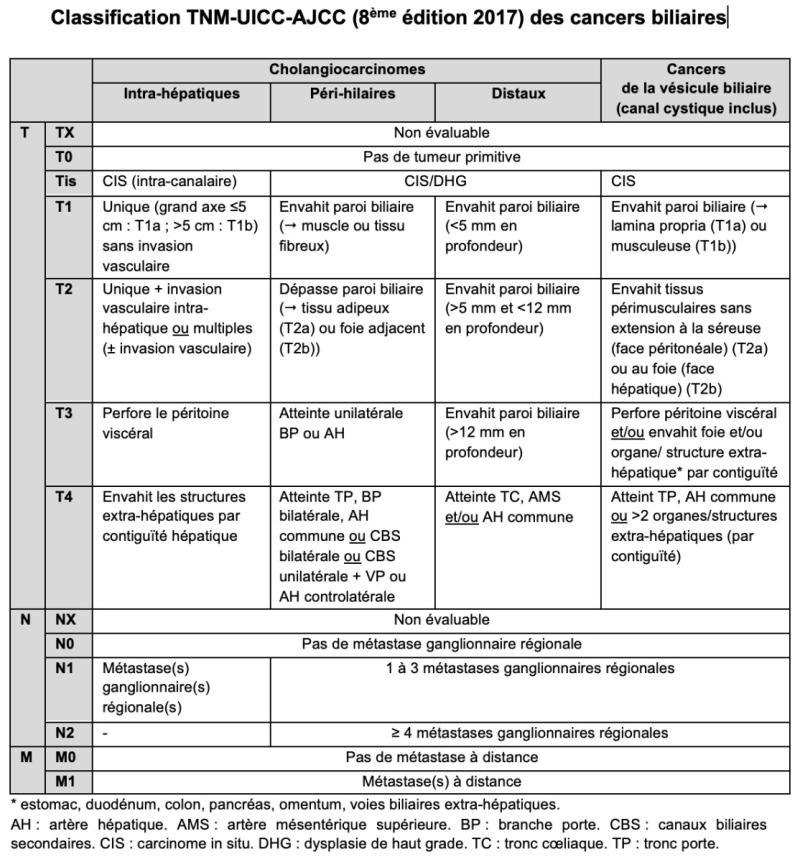
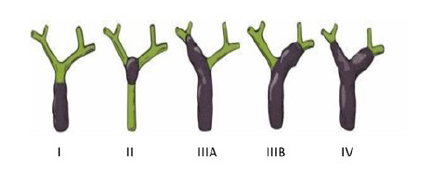
D’autres classifications sont parfois utilisées pour l’évaluation de la résécabilité des cholangiocarcinomes péri-hilaires. La classification de Bismuth-Corlette est la classification préopératoire historiquement utilisée (Bismuth 1975) (Figure 1). Elle est basée uniquement sur le niveau proximal d’extension endobiliaire de la tumeur. Elle sous-estime l’extension tumorale chez un tiers des patients. Elle ne prend pas en compte l’atteinte vasculaire éventuellement associée. D’autres classifications plus exhaustives ont été proposées mais leur application en routine est limitée par leur complexité (Jarnagin 2001, Deoliveira 2011). Plus récemment, la classification XY, plus pragmatique, a été proposée par l’équipe de Rennes (Boudjema 2013) (Figures 2 et 3). Le type X fait référence aux cancers envahissant les segments B2-B3, étendus et rarement résécables (hépatectomie gauche plus ou moins élargie). Le type Y fait référence aux cancers péri-hilaires épargnant la convergence des voies biliaires du lobe gauche (segments 2 et 3, B2-B3), et qui sont toujours résécables (lobectomie droite).
Classification XY des tumeurs péri-hilaires
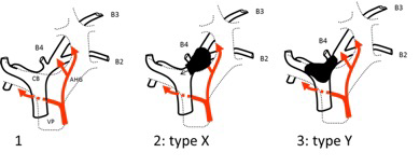
1. schéma du hile hépatique. La convergence biliaire (CB) est à droite de l’axe de la veine porte (VP). L’artère hépatique droite passe derrière le canal hépatique commun. L’artère hépatique gauche (AHG) est très à gauche de la CB. La confluence des canaux biliaires des segments 2 (B2) et 3 (B3) se situe derrière ou au bord droit de la veine porte gauche. Un canal biliaire du segment 4 (B4) est présent près de la convergence dans 80 % des cas. Le lobe hépatique gauche fait des segments 2 et 3 est facile à isoler. Il est la plus petite unité fonctionnelle et anatomique facilement conservable.
2. Le type X (X symbolise sinon la voie sans issue, au moins la difficulté d’accès) regroupe toutes les tumeurs qui envahissent la confluence B2-B3, quelle que soit leur étendue à droite. Il n’est pas possible de garder le lobe gauche et quand le malade est ictérique, témoin de l’envahissement de la convergence, la tumeur est volumineuse, envahissant les vaisseaux du hile. L’exérèse passe par une hépatectomie gauche, volontiers élargie à droite et nécessite des reconstructions vasculaires.
3. Le type Y (Y symbolise la confluence, libre, de B2 et B3) regroupe toutes les tumeurs qui laissent libre la confluence B2-B3 quelle que soit l’étendue à droite. L’exérèse est toujours possible et passe par une hépatectomie droite élargie aux segments 4 et 1. L’AHG, très à gauche, n’est jamais concernée par la tumeur. Le type Y inclut donc les types I, II, IIIA et IV (quand B4 est envahi) de la classification de Bismuth et Corlette. Le type X inclut entre autres le type IIIB de la classification de Bismuth et Corlette.
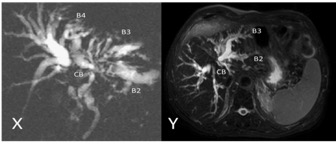
X. Cholangiocarcinome péri-hilaire type X. La tumeur obstrue la confluence B2-B3 et s’étend à la convergence des voies biliaires droite et gauche (CB). La branche droite de l’artère hépatique qui passe en arrière du canal hépatique est envahie. L’exérèse de la tumeur, si elle est localisée passe par une hépatectomie gauche, élargie, et une reconstruction artérielle, geste sinon impossible, au moins très difficile.
Y. Cholangiocarcinome péri-hilaire type Y. La convergence des voies biliaires droite et gauche est obstruée mais la confluence B2-B3 est libre. L’artère hépatique gauche n’est pas envahie et le lobe gauche pourra être conservé, le cas échéant en associant drainage biliaire gauche et embolisation portale droite.
8.3. Explorations pré-thérapeutiques
Une confirmation cyto-histologique est indispensable avant traitement palliatif (tumeur non résécable) ou néo-adjuvant. Elle demeure hautement recommandable avant chirurgie, notamment en cas de doute diagnostique à l’imagerie et en cas de maladie chronique du foie (cirrhose) sous-jacente, 10 % à 20 % des résections hépatiques « carcinologiques » étant réalisées à tort pour des lésions non cancéreuses (Erdogan 2008, Senthil Kumar 2012).
Il est important de disposer de suffisamment de matériel à la fois pour les analyses histologiques à visée de diagnostic positif et pour les analyses moléculaires théranostiques (voir chapitre « traitements ciblés »). Dans cette dernière optique, la congélation d’échantillons est recommandée. Une biopsie en foie non tumoral doit toujours s’envisager, notamment (mais non exclusivement) en cas de suspicion d’hépatopathie chronique sous-jacente.
Pour les cholangiocarcinomes intra-hépatiques, la confirmation histologique est le plus souvent obtenue par une biopsie hépatique transpariétale. Pour les cholangiocarcinomes péri-hilaires ou distaux, la preuve cytologique ou histologique est souvent difficile à obtenir en raison du stroma dense et fibreux et de la faible cellularité des formes infiltrantes très majoritaires.
8.3.1. Imagerie
L’imagerie est inutile en cas de cancer de la vésicule biliaire n’atteignant pas la séreuse. Ailleurs, elle est essentielle au diagnostic positif et différentiel (diagnostic cyto/histologique parfois difficile), au bilan d’extension et à la planification du traitement (Joo 2018). Elle doit déterminer le niveau d’obstruction des voies biliaires, l’envahissement hépatique, vasculaire, ganglionnaire et métastatique. Les examens d’imagerie doivent être réalisés avant mise en place de prothèse biliaire.
Le scanner multiphasique thoraco-abdomino-pelvien (sans injection, phase artérielle, portale et tardive) est la méthode d’imagerie standard pour le bilan d’extension locale, ganglionnaire et métastatique (Ruys 2012, Vilgrain 2008). Sa précision diagnostique pour le cholangiocarcinome intra-hépatique est de 70 %, avec une sensibilité de 78 % et une spécificité de 80 %. La précision diagnostique du scanner pour la résécabilité des cholangiocarcinomes péri-hilaires est estimée entre 60 et 87,5 % avec une valeur prédictive négative comprise entre 85 et 100 %.
L’IRM hépatique avec injection dynamique de chélates de gadolinium augmente la spécificité pour le diagnostic positif de cholangiocarcinome intra-hépatique (Saleh 2020). Les agents extracellulaires sont préférables lors de la phase initiale diagnostique. En revanche, en cas de projet de résection à visée curative, une injection d’agents hépatospécifiques et la réalisation de séquences de diffusion sont recommandées pour améliorer le bilan d’extention locale. Pour les cholangiocarcinomes péri-hilaires et distaux, il faut y associer une cholangio-IRM (Vilgrain 2008). La cholangio-IRM réalisée avant mise en place de prothèse biliaire permet une meilleure précision que le scanner de l’extension biliaire (Romagnuolo 2003) et pour la recherche de métastases hépatiques. Sa sensibilité de détection est de 95 % (Romagnuolo 2003). Elle permet d’évaluer l’extension aux canaux biliaires avec une fiabilité de 90 %, mais peut toutefois sous-estimer l’extension longitudinale des tumeurs péri-hilaires (Lopera 2001, Park 2008).
La place de la tomographie par émission de positons (TEP) au 18F-fluorodésoxyglucose (FDG) reste à définir. Elle a une sensibilité et une spécificité d'environ 80-90 % pour le diagnostic de cancer vésiculaire ou de cholangiocarcinome nodulaire ≥ 1 cm. Sa sensibilité est moins bonne (< 20 % dans certaines études) en cas de cholangiocarcinome infiltrant. Sa spécificité est moindre en cas de cholangite sclérosante primitive, de prothèse biliaire ou de maladie granulomateuse (Kluge 2001). Les méta-analyses montrent une sensibilité de la TEP-FDG pour le diagnostic des métastases ganglionnaires de 13 % à 64 % et une spécificité de 91 % à 97 % (Hu 2018, Lamarca 2019, Huang 2020). Elle permet surtout de diagnostiquer des métastases à distance (sensibilité 56 %, spécificité 95 %) (Huang 2020), mais sa valeur ajoutée par rapport à l’imagerie conventionnelle en cas de cancer biliaire est mal évaluée. Elle ne doit pas retarder la prise en charge thérapeutique.
La cholangiographie directe (percutanée trans-hépatique ou rétrograde endoscopique) doit être réservée à des fins thérapeutiques. Brossage et biopsies par voie trans-papillaire lors d’une CPRE sont recommandés en cas de suspicion de cholangiocarcinome péri-hilaire en particulier lorsqu’il existe une indication de drainage biliaire (Navaneethan 2015). Leur sensibilité respective est faible, oscillant entre 30 et 50% selon les études avec par contre une excellente spécificité avoisinant les 100 % (Burnett 2013, Navaneethan 2015b, Mehmood 2016, Kobayashi 2019, Weber 2009). La combinaison des deux méthodes lors d’un cathétérisme rétrograde peut améliorer la sensibilité à plus de 60% selon certaines études. Dans une méta-analyse récente (regroupant 32 articles publiés entre janvier 1995 et août 2020 (1123 patients atteints de cholangiocarcinome), la sensibilité diagnostique était de 56% [IC95% 48,8-63,1] pour le brossage, sigificativement inférieure à celle de la biopsie transpapillaire (67 % [60,2-73,5]), de la combinaison brossage-biopsie (71 % [64,1-76,8]) et de l'échoendoscopie avec ponction (74 % [64,7-81,5]) – sans différence significative entre ces trois modalités - (Yoon 2022). Les effets indésirables étaient comparables entre les groupes.
L’échoendoscopie avec cytoponction est utile pour les lésions biliaires distales mais aussi proximales (Weilert 2014, Moura 2018). Les résultats dans cette indication en font une des procédures de choix avec une sensibilité dépassant les 70 % dans la plupart des études (Téllez-Ávila 2014, Lee 2004, Wu 2011). C’est la technique de choix de première intention en l’absence d’indication à un drainage biliaire. Ses performances sont cependant limitées par l’absence fréquente de cible ponctionnable et/ou par la localisation péri-hilaire inconstamment accessible. Dans les centres ayant un accès facile à l’échoendoscopie avec ponction, celle-ci est couplée à la CPRE dans le même temps anesthésique permettant une amélioration des performances diagnostiques de la CPRE avec prélèvements endobiliaires. Les performances de l’échoendoscopie sont supérieures en cas d’adénopathies ponctionnables ou d’une masse à développement exobiliaire. Elle permet également la ponction de métastases du foie gauche de petite taille non visibles sur les examens en coupe traditionnels (Weilert 2014).
La cholangioscopie permet une visualisation directe de l’épithélium biliaire et des biopsies ciblées. La modalité qui fait désormais référence consiste à utiliser un cholangioscope à usage unique mono-opérateur (système Spyglass™) au cours d’une CPRE. La cholangioscopie permet le diagnostic des sténoses biliaires dites indéterminées (absence de diagnostic après bilan complet y compris un brossage cytologique) dans environ deux tiers des cas et en modifie la prise en charge, comme l’ont montré une étude prospective multicentrique (Prat 2019) et une étude rétrospective internationale (Tyberg 2019). La cholangioscopie peut en particulier écarter une suspicion de cholangiocarcinome, évitant une chirurgie inutile (15 à 20 % des sténoses péri-hilaires avant 2010 [Senthil-Kumar 2012]). Sa place en situation préopératoire n’est pas encore consensuelle, mais elle est le plus souvent proposée après une ou plusieurs CPRE avec brossages/biopsies négatifs. Dans un essai randomisé de faible effectif, la sensibilité des biopsies guidées par cholangioscopie en première intention était significativement plus élevée que celle du brossage guidé par CPRE (68,2 % vs 21,4 %, p< 0,01) (Gerges 2020). La spécificité, la valeur prédictive positive, la valeur prédictive négative et la survenue d’évènements indésirables ne présentaient aucune différence significative.
Les autres techniques d’imagerie (échographie de contraste, mini-sonde d'endosonographie, endomicroscopie confocale…) sont insuffisamment validées et/ou peu accessibles (centres experts). Elles ne devraient être employées que dans le cadre d'essais cliniques.
8.3.2. Diagnostic différentiel et marqueurs immuno-histochimiques
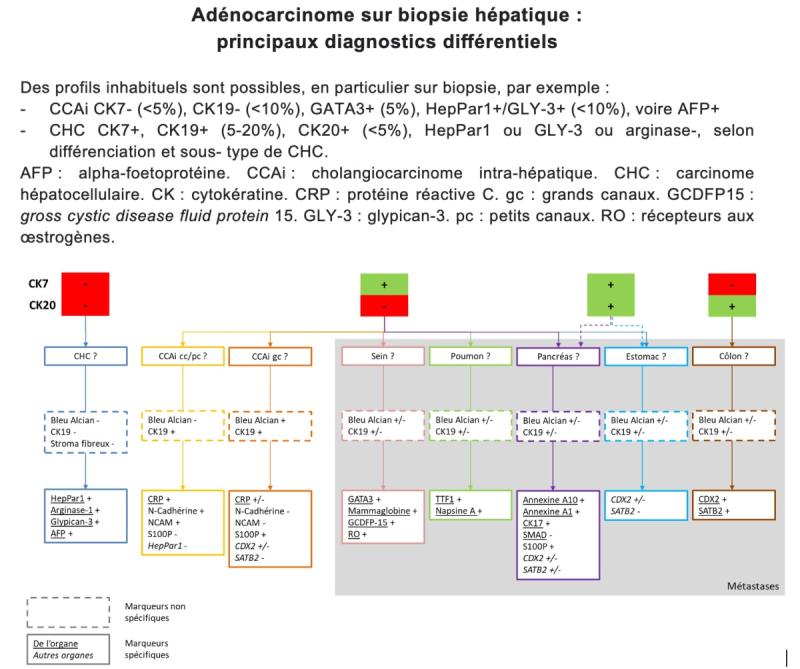
Les principaux diagnostics différentiels des cholangiocarcinomes intra-hépatiques sont les métastases d’un adénocarcinome d’autre origine, le carcinome hépatocellulaire et l’hépato-cholangiocarcinome (Figure 4). L’immunohistochimie tumorale peut aider, sous forme d’un panel de première intention comprenant cytokératine [CK]7, CK19, CK20, CDX2/SATB2 (origine gastro-intestinale), TTF1 (origine pulmonaire), et chez une femme GATA3 (origine mammaire), les cholangiocarcinomes étant classiquement CK7+, CK19+, CK20+/- (et CDX2/SATB2-, TTF1-, GATA3-). Toutefois, la sensibilité et la spécificité de ces marqueurs de première intention restent imparfaites. Dans les situations complexes, il peut être prudent de compléter le panel de base avec d’autres marqueurs plus spécifiques mais parfois moins sensibles (poumon : napsine A ; sein : gross cystic disease fluid protein 15 [GCDFP15], mammaglobine et récepteurs aux œstrogènes ; pancréas : MUC5AC, annexines A1 et A10, CK17, SMAD), tout en veillant à préserver l’échantillon tissulaire afin de permettre la réalisation ultérieure d’une analyse moléculaire à visée théranostique.
Les métastases d’adénocarcinome colique sont en règle aisément identifiables sur la morphologie standard et sur leur immunophénotype, majoritairement CK7- CK20+ CDX2+ et SATB2+, plus spécifique d’une origine colorectale que CDX2, parfois exprimé dans les cancers gastriques ou pancréatiques. L’expression de SATB2 est rare dans le cholangiocarcinome et serait restreinte aux cholangiocarcinomes extra-hépatiques (De Michele 2021). En revanche, le diagnostic différentiel avec des métastases d’origine pancréatique, gastrique ou biliaire extra-hépatique peut être difficile, nécessitant la conjonction de plusieurs marqueurs immunohistochimiques. D’autres examens morphologiques peuvent être utiles en cas de doute diagnostique (TDM thoracique, mammographie, TEP, endoscopies digestives…), orientés par l’immunohistochimie.
Jusqu’à un tiers des carcinomes de primitif inconnu avec atteinte hépatique correspondent en fait à des cholangiocarcinomes intra-hépatiques méconnus (Conway 2022). Les données anatomopathologiques, la relecture de l’imagerie par un spécialiste hépatobiliaire à la recherche de signes évocateurs (lésion hépatique dominante, rétraction capsulaire hépatique…) et le profilage moléculaire tumoral à la recherche d’altérations génétiques caractéristiques des cholangiocarcinomes intra-hépatiques (cf. infra) peuvent aider à redresser le diagnostic.
Parmi les nouveaux marqueurs immunohistochimiques, la protéine réactive C (CRP), déjà utile en pathologie hépatique pour le diagnostic des adénomes hépatocellulaires inflammatoires, apparaît comme prometteuse pour différencier les cholangiocarcinomes intra-hépatiques (notamment de type « petits canaux ») des métastases hépatiques d’adénocarcinome pancréatique et gastrique. Ses performances sont meilleures que celles de la N-cadhérine avec une sensibilité et une spécificité de 93,3% et 88,2% (sur pièce opératoire toutefois) versus 80,0 % et 88,2 % pour la N-cadhérine (Yeh 2017).
Les diagnostics différentiels des cholangiocarcinomes extra-hépatiques sont nombreux (Senthil-Kumar 2012). Les lésions bénignes sont dominées par les cholangites chroniques (cholangite sclérosante primitive et cholangite à IgG4, suivies de causes (lithiasiques, infectieuses, vasculaires, iatrogènes, toxiques, néoplasies bénignes, etc) beaucoup plus rares. Parmi les causes malignes, les métastases péri-hilaires et la carcinose du pédicule hépatique (par exemple extension d’un adénocarcinome pancréatique corporéo-caudal) peuvent mimer un cholangiocarcinome de même topographie.
8.3.3. Marqueurs tumoraux sériques
Aucun n’est spécifique des cancers biliaires. Le carbohydrate antigène (CA) 19.9 a une sensibilité et une spécificité d'environ 80 % (étudiées surtout en cas de cholangite sclérosante primitive) (Levy 2005). L’antigène carcino-embryonnaire (ACE) et le CA 125 sont moins sensibles (30-50 %) et pas plus spécifiques (Ramage 1995). Tous trois peuvent être élevés au cours des obstructions biliaires bénignes. Une élévation persistante après drainage biliaire efficace est évocatrice de cancer.
8.3.4. Résécabilité
Elle doit être évaluée par une équipe médico-chirurgicale expérimentée, chez tout patient jugé opérable, avant opacification ou drainage biliaire. Une volumétrie hépatique TDM doit être effectuée avant hépatectomie majeure. La résécabilité est aussi conditionnée par la présence ou non d’une cirrhose sous-jacente. La résécabilité ne peut souvent être affirmée (ou infirmée) définitivement qu’au cours de l’exploration chirurgicale. L’évaluation initiale en laparoscopie peut parfois permettre d’éviter un programme de préparation préopératoire lourd dans des situations à risque de non-résécabilité (suspicion de métastases péritonéales ou de métastases controlatérales). Sa rentabilité augmente avec l’extension tumorale (Weber 2002).
8.3.5. Références et options
Examens pré-thérapeutiques : voir tableau 2.
Cholangiocarcinomes péri-hilaires ou distaux
- Une cytologie suspecte est suffisante pour débuter une chimiothérapie ou poser l’indication d’une chirurgie, après validation en réunion de concertation pluridisciplinaire (RCP) spécialisée (accord d’experts). Le risque de faux positif en cas de cytologie faite après procédure de drainage biliaire devra toutefois être pris en compte.
- En cas de cytologie/histologie négative à deux reprises, devant un tableau clinique et radiologique évocateur de cholangiocarcinome et après cholangioscopie et dosage des IgG4, la prise en charge chirurgicale ne devra pas être retardée en cas de tumeur résécable. En cas de tumeur non résécable, la possibilité de débuter une chimiothérapie doit être validée en RCP (accord d’experts). Des techniques moléculaires (séquençage haut débit [NGS], hybridation in situ [ISH]) peuvent être utiles dans cette situation (grade B).
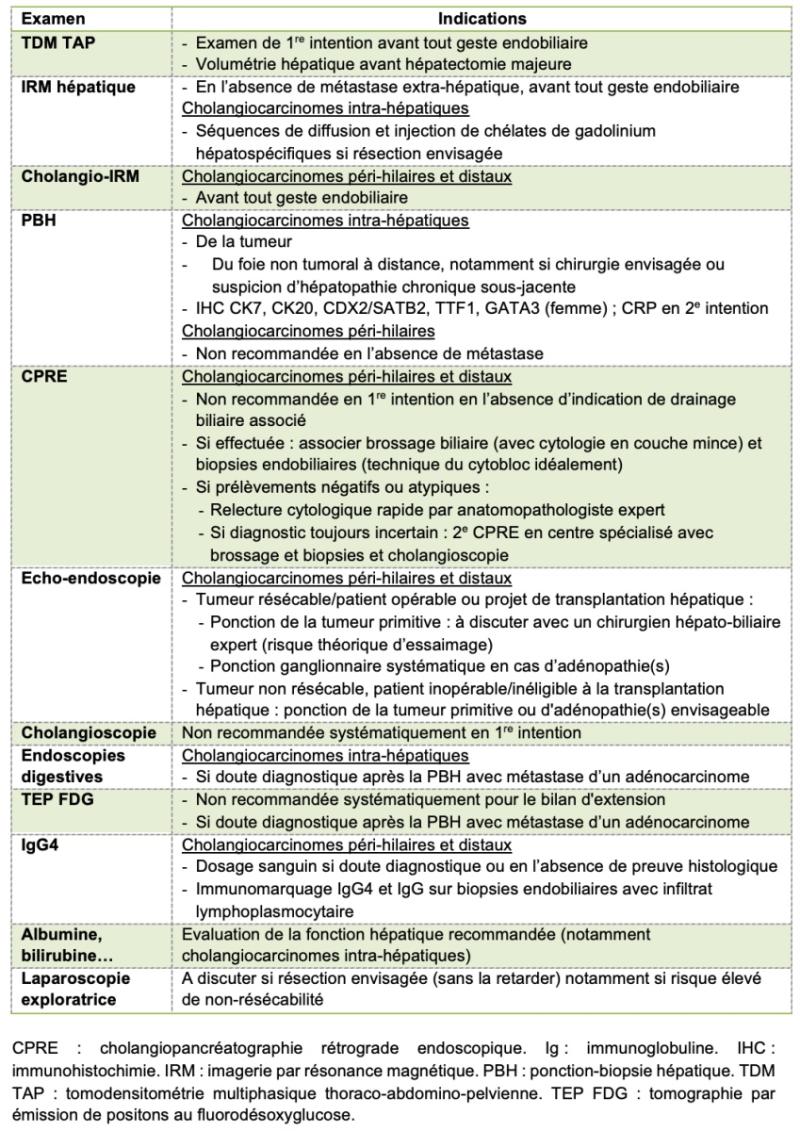
Examens pré-thérapeutiques
8.4. Dépistage des formes familiales
Les cancers biliaires peuvent s’inscrire dans le cadre d’un syndrome de prédisposition héréditaire autosomique dominant par mutation d’un gène du système MMR (syndrome de Lynch, prédisposant au cancer colorectal, de l’endomètre, de l’estomac, de l’ovaire, des voies urinaires…) ou d’un gène BRCA (prédisposant au cancer du sein, de l’ovaire, du pancréas, de la prostate). Aucun examen de dépistage des cancers biliaires n’est recommandé chez les sujets atteints de tels syndromes, en l’absence d’évaluation de cette stratégie.
En dehors de ces syndromes de prédisposition, d’exceptionnelles agrégations familiales de cancers biliaires, de substratum génétique inconnu, ont été rapportées (Hemminki 2003).
8.5. Traitements
8.5.1. Traitements à visée curative
8.5.1.1. Résection chirurgicale
8.5.1.1.1. Principes généraux
Au-delà des considérations anatomiques spécifiques des différentes localisations tumorales, l’objectif de la chirurgie est d’obtenir une résection chirurgicale avec des marges R0 tout en préservant un volume de foie restant adéquat. Toutefois, même après résection R0, la survie à 5 ans ne dépasse pas 5-10 % en cas de cancer vésiculaire et 10-40 % en cas de cholangiocarcinome.
Les facteurs principaux de mauvais pronostic sont l’envahissement ganglionnaire, l’envahissement vasculaire et l’envahissement microscopique des marges de résection (statut R1). La présence d’un seul facteur pronostique péjoratif n’est pas une contre-indication à la chirurgie en soi. L'exploration chirurgicale avec examen histologique extemporané de la ou des tranches de section biliaire est donc essentielle. L’intérêt d’un curage ganglionnaire locorégional systématique, longuement débattu dans le passé, est aujourd’hui recommandé en raison de son impact pronostique majeur en cas de métastases ganglionnaires (de Jong 2011, Weber 2015, Valle 2016, NCCN 2019). La présence d’adénopathies tumorales au-delà du premier relais ganglionnaire représente une contre-indication à la résection à visée curative.
La morbi-mortalité des résections hépatiques majeures (ou pancréatiques) pour cancer biliaire est supérieure à celle des mêmes résections effectuées pour d'autres indications et des résections biliaires seules, notamment du fait de l’âge souvent avancé ou d’un état général altéré, notamment par l’ictère (Dokmak 2013). La morbi-mortalité des hépatectomies majeures peut être diminuée par le drainage biliaire préopératoire du futur foie restant en cas d’ictère puis, le cas échéant, l’embolisation portale préopératoire du foie à réséquer afin d’hypertrophier le futur foie restant si le volume de celui-ci est insuffisant à la volumétrie TDM. Le drainage biliaire avant chirurgie à visée curative semble améliorer les résultats de la chirurgie (Grandadam 2010). Son objectif est triple : lever la congestion biliaire hépatique (et la souffrance hépatocytaire), restaurer la présence de bile dans le tube digestif (et réduire ainsi le risque de translocation bactérienne) et réduire la cholestase ictérique (pour traiter l’éventuel prurit et protéger la fonction rénale). La voie rétrograde endoscopique est plus confortable pour le malade mais le positionnement du drain dans le secteur utile est difficile. La voie antérograde trans-pariéto-hépatique permet de diriger le drainage dans le secteur voulu et présente l’avantage de ne pas franchir la tumeur. Elle est associée à un risque de déplacement du drain et de cholépéritoine, en particulier lorsque le drainage passe par le foie droit. La voie endoscopique doit être privilégiée pour les cholangiocarcinomes péri-hilaires, du fait d’un essai randomisé arrêté précocement pour surmortalité de la voie transpariétale (Coelen 2018). Seules les prothèses plastiques et éventuellement les prothèses métalliques couvertes temporaires sont autorisées. Le drainage concerne le futur foie restant dont il participe à l’hypertrophie, lorsque la ou les branche(s) porte(s) nourrissant le foie tumoral qui doit être réséqué a (ont) été embolisée(s). Le délai nécessaire entre drainage biliaire et chirurgie n’est pas défini. Il dure le temps qu’il faut pour permettre aux taux sanguins de bilirubine et de transaminases de revenir à des valeurs normales ou presque. Ainsi, dans la perspective d’une hépatectomie droite élargie (tumeur de type Y ou Bismuth IIIa), le drainage du lobe gauche par une prothèse plastique généralement longue de 10F est l’objectif prioritaire. Le drainage d’une partie non tumorale du lobe droit peut aussi être utile en cas d’ictère majeur afin d’accélérer la régression de l’ictère et la récupération nutritionnelle avant chirurgie.
Un compte-rendu anatomopathologique standardisé doit être établi : lésions (pré)néoplasiques associées (carcinome in situ, cholangite sclérosante primitive), type tumoral, grade de différenciation, stade, marges (R0, R1, R2), envahissement lymphatique, vasculaire, péri-nerveux, ganglionnaire, viscéral de contiguïté et métastatique.
8.5.1.1.2. Cholangiocarcinomes intra-hépatiques
Malgré l’absence de référence dans la littérature, une marge de sécurité de 1 cm est habituellement réalisée, puisque le pronostic en cas de marge inférieure à 5 mm est proche de celui après résection R1 (Spolverato 2015). En revanche, ni la résection hépatique anatomique (résection en bloc de la tumeur et du territoire portal concerné centré sur un pédicule glissonien), ni la résection systématique du segment I ou de la voie biliaire principale ne sont justifiées.
La lymphadénectomie locorégionale est recommandée lors de la résection d’un cholangiocarcinome intra-hépatique, l’atteinte ganglionnaire étant un des principaux facteurs pronostiques (Farges 2011, de Jong 2011, Weber 2015). Certains auteurs préconisent l’abandon de la résection en cas de positivité de ces ganglions, notamment si la résection hépatique est complexe.
8.5.1.1.3. Cholangiocarcinomes péri-hilaires
La présence d’adénopathies suspectes sur le bilan d’imagerie (dont on ignore le statut) ne doit pas représenter une contre-indication à la résection car il existe des faux positifs (Burke 1998, Jarnagin 2001, Kitagawa 2001).
La laparoscopie préopératoire peut être utile pour la stadification (Bird 2017).
La résection chirurgicale comprend au minimum la résection de la voie biliaire principale (type I de Bismuth) avec lymphadénectomie régionale. L’intérêt d’un curage étendu au rétro-duodéno-pancréas, voire plus, n’est pas démontré.
Pour des cholangiocarcinomes de type II, III ou IV de Bismuth, il est recommandé d’associer une hépatectomie majeure (droite ou gauche) voire élargie, qui permet d’augmenter le pourcentage de marges R0 et la survie à 5 ans (Neuhaus 1999). Le choix du type de résection hépatique est guidé par l’existence d’une dysmorphie hépatique et/ou d’une atteinte vasculaire unilatérale, et par l’extension biliaire. Ainsi, l'atteinte du plafond de la convergence biliaire principale (type ≥ 2 de Bismuth) impose la résection du segment I (lobe caudé ou lobe de Spiegel), car ses canaux biliaires sont alors envahis dans environ 90 % des cas. L’hépatectomie droite élargie aux segments I et IV est recommandée lorsque la tumeur épargne la convergence B2-B3 (type Y selon la classification de Rennes), pour des raisons techniques (plus grande longueur du canal hépatique gauche) et carcinologiques (fréquent envahissement de la branche artérielle droite), afin d’optimiser la probabilité d’obtenir un statut des marges R0 (Boudjema 2013) (Figures 2 et 3).
La résection de la veine porte peut être associée à l’hépatectomie, soit de manière systématique, soit par nécessité en cas d’envahissement tumoral. Elle n’augmente pas la morbidité opératoire. En revanche, la résection de l’artère hépatique doit rester exceptionnelle, le bénéfice carcinologique n’étant pas prouvé et la morbidité majorée (Nagino 2010).
Le taux de résection à visée carcinologique pour des lésions hilaires finalement bénignes peut atteindre jusqu’à 20 % des cas dans certaines séries (Juntermanns 2011, Erdogan 2008).
8.5.1.1.4. Cholangiocarcinomes distaux
Ils requièrent une duodénopancréatectomie céphalique avec lymphadénectomie standard et résection de la voie biliaire principale en zone saine selon l’examen extemporané (Dickson 2014).
8.5.1.1.5. Cancers de la vésicule biliaire
8.5.1.1.1.5.1. Cancers Tis, T1a, T1b ou T2 découverts fortuitement sur la pièce de cholécystectomie
La découverte fortuite d’un cancer de la vésicule biliaire nécessite une prise en charge spécifique rapide en raison du risque élevé de récidive précoce et de dissémination métastatique (Sikora 2006). Les éléments du compte rendu opératoire initial (indication, voie d’abord, description peropératoire, éventuelle perforation, extraction de la vésicule biliaire dans un sac protecteur) et du compte-rendu anatomopathologique (localisation de la tumeur, atteinte pariétale, marge de résection au niveau du canal cystique et du lit vésiculaire, statut ganglionnaire) doivent être analysés en détail. L’ouverture peropératoire de la vésicule biliaire doit être considérée comme une effraction tumorale, avec un risque de récidive péritonéale très élevé, même en cas d’extraction dans un sac de protection (Goetze 2009). Dans de tels cas, l’intérêt de la résection chirurgicale à visée curative paraît discutable (Tian 2015).
Le taux d’envahissement ganglionnaire augmente avec le stade : Tis : 0 % ; T1a : 2-5 % ; T1b : 15-20 % ; T2 : 20-60 % (Yamaguchi 1992, Shirai 1992, Wakai 2001, Toyonaga 2003, Suzuki 2004). La cholécystectomie seule est suffisante en cas de stade Tis ou T1a (survie à 5 ans : 95-100 %) (Fuks 2011, Goetze 2008). Une résection hépatique associée et un curage ganglionnaire sont recommandés pour les tumeurs T1b et plus (Lee 2014, Ogura 1991, de Aretxabala 1992). La survie à 5 ans a augmenté de 42 % avec la cholécystectomie seule à 79 % avec cette attitude dans le registre Allemand (Goetze 2008). La résection complémentaire secondaire à visée curative améliore également significativement la survie en cas de stade T2, sans influence péjorative nette de la voie d’abord (cœlioscopique ou laparotomique), à condition qu’il n’y ait pas eu ouverture de la vésicule pendant la cholécystectomie. La survie est meilleure et le taux de récidive tumorale plus faible chez les patients ayant eu une résection complémentaire précoce (Shirai 1992, Wakai 2001). Toutefois, l'introduction récente de la sous-classification en T2a et T2b est à la base d’un nouveau débat. La localisation sur le versant hépatique (T2b) est associée à un pronostic défavorable avec un taux élevé de récidive hépatique (23 % vs 3 %) et ganglionnaire (16 % vs 3 %) malgré une chirurgie curative complémentaire (Shindoh 2015), alors qu’aucune récidive n’a été observée chez les patients avec une tumeur T2 sur le versant péritonéal (T2a) après cholécystectomie seule (Lee 2015).
L’intervention secondaire de référence est la bi-segmentectomie IVb-V avec curage ganglionnaire et éventuellement résection de la voie biliaire. Une résection du lit vésiculaire peut être une alternative à la bi-segmentectomie, notamment si le cancer est de petite taille et est situé sur le versant libre de la vésicule. La résection de la voie biliaire n’est recommandée qu’en cas d’atteinte du cystique ou d’envahissement ganglionnaire patent.
La résection secondaire systématique des orifices de trocart (Z’graggen 1998) est actuellement controversée (Maker 2012).
Une conversion est recommandée en cas de suspicion per-cœlioscopique de cancer de la vésicule biliaire.
Une évaluation par TDM, IRM hépatique avec séquences biliaires et éventuellement TEP est nécessaire avant d’envisager une réintervention.
8.5.1.1.5.2. Cancers localement avancés > T2
L’intérêt de la résection hépatique reste controversé. Peuvent être proposées une bi-segmentectomie IVb-V, une tri-segmentectomie, et pour les tumeurs envahissant le pédicule hépatique, une hépatectomie droite élargie ou une hépatectomie centrale (IV, V, VIII) associée à une résection du segment I. La résection du segment I est utile surtout pour les tumeurs envahissant le hile hépatique.
L’envahissement direct du côlon, du duodénum ou du foie n’est pas une contre-indication absolue à la résection mais la morbi-mortalité de ces résections combinées est élevée.
En cas d’envahissement ganglionnaire, la survie à 5 ans est faible à nulle, notamment lorsque plus d’un à deux ganglions sont envahis (Dixon 2005, Endo 2006). Le curage ganglionnaire doit comporter une résection étendue des ganglions du pédicule hépatique, des ganglions pancréatiques antérieurs et postérieurs ainsi qu’un « pelage » de l’artère hépatique jusqu’à sa naissance au niveau du tronc cœliaque. Certains auteurs recommandent un curage extensif, étendu au tronc cœliaque et au tronc de l’artère mésentérique supérieure en descendant le long de la face antérieure de l’aorte (ganglions para-aortiques) (Kondo 2000).
L’envahissement du pédicule hépatique et de la voie biliaire principale est précoce dans le cancer de la vésicule biliaire sans qu’il y ait nécessairement un retentissement clinique (ictère) ni un contact par la tumeur (Shimizu 2004). L’exérèse de la voie biliaire principale facilite le curage ganglionnaire du pédicule hépatique. Elle est donc fréquemment réalisée en cas de tumeur > T2.
8.5.1.2. Thermo-ablations percutanées
Une revue systématique récente des thermo-ablations percutanées (radiofréquence, cryothérapie, électroporation irréversible, micro-ondes) dans les cholangiocarcinomes intra-hépatiques a évalué 15 études rétrospectives (645 patients) (Edeline 2021). La radiofréquence était la technique la plus utilisée (7/15 études). Aucune chimiothérapie systémique concomitante n'était utilisée. La taille médiane des lésions était de 27 mm (15-44), le taux de réponse (ablation) complète globale était de 93,9 %, et la médiane de survie globale de 30,2 mois (IC95% : 21,8-38,6). Ces résultats sont proches de ceux des séries chirurgicales mais les populations traitées sont différentes. Les thermo-ablations percutanées intéressent des tumeurs uniques (ou peu nombreuses) et plus petites (diamètre en règle < 3 cm), et sont souvent réalisées après chirurgie antérieure (51,2 % des patients dans cette revue systématique), chez des patients cirrhotiques ou chez des patients considérés comme non opérables (comorbidité, fragilité).
8.5.1.3. Transplantation hépatique
Les taux de survie 5 ans après transplantation hépatique pour cancer biliaire dans les séries historiques sont de l'ordre de 25-30 %. Cependant, la majorité des patients récidivent dans les 2 ans. Dans une étude rétrospective multicentrique américaine chez 287 patients avec cholangiocarcinome péri-hilaire initialement non résécable, traités entre 1993 et 2010 par radio-chimiothérapie, curiethérapie et chimiothérapie néo-adjuvantes, puis laparotomie exploratrice, et enfin transplantation hépatique (protocole Mayo Clinic), la survie à 5 ans en intention de traiter était de 53 % (Darwish Murad 2012). Cependant, un biais de sélection pour l’analyse est probable, du fait d’une sous-estimation du nombre de patients sortis du parcours néo-adjuvant pour progression liée au caractère rétrospectif de l’étude. En outre, deux tiers des patients avaient une cholangite sclérosante primitive et une tumeur relativement plus petite que les autres patients. Une méta-analyse de 20 études totalisant 428 patients transplantés pour cholangiocarcinome péri-hilaire non résécable rapportait un taux de survie globale à 5 ans de 31,6% sans radio-chimiothérapie néo-adjuvante et de 65,1 % avec (taux de récidive à 3 ans : 51,7 % et 24,1 % respectivement) (Cambridge 2021). Les patients avec cholangite ssclérosante primitive avaient le meilleur pronostic. Actuellement, la transplantation hépatique dans le cadre de ce protocole préopératoire est admise en cas de cholangiocarcinome péri-hilaire non résécable, et fait l’objet d’une priorisation sur liste d’attente. Il faut souligner la complexité de ce programme thérapeutique, le taux élevé de complications vasculaires postopératoires en rapport avec la radiothérapie et le faible bénéfice en intention de traiter issu de la stricte sélection des candidats. L’intérêt de cette stratégie en raison des résultats de survie à long terme a été également évoqué pour les cholangiocarcinomes péri-hilaires résécables et a été évalué dans l’essai TRANSPHIL, interrompu précocement et dont les résultats n’ont pas encore été communiqués.
Une étude internationale multicentrique rétrospective a montré un taux de survie à 5 ans de 65 % après transplantation hépatique pour cholangiocarcinome intra-hépatique ≤ 2 cm développé sur cirrhose (Sapisochin 2016). L’effectif limité (81 patients) et la sélection des patients (cholangiocarcinome intra-hépatique de découverte fortuite sur le foie natif de patients transplantés pour cirrhose) rendent ces résultats peu extrapolables à la pratique.
8.5.1.4. Traitement néo-adjuvant et adjuvant
En l’absence d’essai randomisé rapporté à ce jour, un traitement néo-adjuvant, qui n’est envisagé que pour les cholangiocarcinomes intra-hépatiques, ne devrait être réalisé que dans le cadre d’un essai clinique. Une confirmation cytologique ou histologique préalable est indispensable avant un éventuel traitement néo-adjuvant.
En cas de réponse d’un cholangiocarcinome intra-hépatique initialement non-résécable à un traitement systémique et/ou loco-régional, la chirurgie doit de nouveau être discutée (Le Roy, Brit J Surg 2018 et Riby, Ann Surg Oncol 2020)
Une méta-analyse sur les données publiées de 20 études (essentiellement rétrospectives ou de registres) entre 1960 et 2010 (6712 patients) a montré un bénéfice de survie globale à la limite de la significativité d’un traitement adjuvant quel qu’il soit (chimiothérapie, radiothérapie ou radio-chimiothérapie) par rapport à la chirurgie seule pour tous les types de cancer biliaire (ratio de risque [HR] : 0,74 ; p=0,06). Le bénéfice de la chimiothérapie et de la radio-chimiothérapie était significativement supérieur à celui de la radiothérapie seule (odds ratio [OR] : 0,39, 0,61, et 0,98, respectivement ; p=0,02). Le bénéfice du traitement adjuvant était également plus marqué en cas de statut N+ (OR : 0,49 ; p=0,004) ou R1 (OR : 0,36 ; p=0,002) (Horgan 2012).
Les résultats de cinq essais randomisés adjuvants sont disponibles :
- L’essai asiatique BCAT a randomisé 225 patients entre chimiothérapie adjuvante par gemcitabine (6 mois) et surveillance seule (Ebata 2018). La survie sans récidive (critère de jugement principal) n’était pas significativement supérieure dans le bras gemcitabine (médiane : 36,0 vs. 39,9 mois ; HR : 0,93 ; p=0,69), de même que la survie globale (62,3 vs 63,8 mois ; HR : 1,01 ; p=0,96).
- L’essai français PRODIGE 12-ACCORD 18-UNICANCER GI a randomisé 196 patients entre chimiothérapie adjuvante par GEMOX (12 cycles soit 24 semaines) et surveillance seule (Edeline 2019). La survie sans récidive (critère de jugement principal) n’était pas significativement supérieure dans le bras GEMOX (médiane : 30,4 vs. 18,5 mois ; HR : 0,88 ; p=0,48), de même que la survie globale (75,8 vs. 50,8 mois ; HR : 1,08 ; p=0,74). Une méta-analyse des données individuelles des 419 patients inclus dans les études BCAT et PRODIGE 12 confirmait l’absence de bénéfice d’une chimiothérapie adjuvante par gemcitabine seule ou associée à l’oxaliplatine tant en survie sans récidive (HR : 0,91 [IC95% 0,71-1,16] ; p=0,46 ; 40,8 % vs 36,6 % à 5 ans) qu’en survie globale (HR : 1,03 [IC95% 0,78-1,35] ; p=0,85 ; 50,5 % vs 49,3 % à 5 ans) (Edeline 2022).
- L’essai de phase 2 randomisé sud-coréen STAMP a randomisé 101 patients après résection d'un cholangiocarcinome péri-hilaire ou distal N+ à recevoir une chimiothérapie adjuvante par gemcitabine 1000 mg/m² et cisplatine 25 mg/m² J1 et J8, toutes les 3 semaines (schéma CISGEM) pendant 8 cycles (24 semaines) ou par capécitabine 1250 mg/m² x2/jour pendant 14 jours toutes les 3 semaines pendant 8 cycles (24 semaines) (Yoo 2022). La survie sans maladie, critère de jugement principal de l'étude, n'a pas été améliorée avec le CISGEM (médiane 14,3 vs. 11,1 mois avec la capécitabine, HR 0,96, IC95 0,71-1,30, p = 0,43), de même que la survie globale (médiane 35,7 vs. 35,7 mois, HR 1,08, IC95 0,72-1,64, p = 0,40).
- L’essai britannique BILCAP a randomisé 447 patients entre chimiothérapie adjuvante par capécitabine (8 cycles soit 24 semaines) et surveillance seule (Primrose 2019). La tolérance de la capécitabine était bonne, sans effet délétère sur la qualité de vie. Le bénéfice de survie globale (critère de jugement principal) n’a pas atteint la significativité statistique en analyse primaire (médiane : 51,1 vs. 36,4 mois ; HR : 0,81 ; p=0,097), mais l’a atteint après ajustement selon le sexe, le statut ganglionnaire et le grade histologique (HR : 0,71 ; p=0,01). La survie sans récidive (critère de jugement secondaire) était significativement améliorée dans le bras capécitabine (médiane : 24,4 vs. 17,5 mois ; HR : 0,75 ; p=0,033) ; toutefois, le bénéfice n’était significatif que pendant les 24 premiers mois suivant la chirurgie, et la survie sans récidive à 5 ans n’était que de 34 % vs 31 % dans le bras contrôle dans l’actualisation de l’étude (Bridgewater 2022).
- Les résultats de l’essai contrôlé randomisé de phase III japonais ASCOT, comparant chez 440 patients le S-1, une fluoropyrimidine orale très utilisée en Asie, mais non validée en population européenne, à la surveillance après résection à visée curative R0 d’un cancer biliaire (Nakachi 2023). Les résultats étaient positifs sur l’objectif principal de survie globale (HR=0,69 ; IC95% 0,51-0,94 ; 77,1 % vs 67,6 % à 3 ans ; p=0·008). La survie sans récidive n’était, elle, pas améliorée de façon statistiquement significative avec le S-1 (HR=0,80, IC95% 0,61-1,04 ; 62,4 % vs 50,9 % à 3 ans ; p=0,088). Cette étude, bien que non transposable en population européenne, renforce le rationnel de l’utilisation d’une fluoropyrimidine en traitement adjuvant.
Contrairement à la chimiothérapie adjuvante, on ne dispose d’aucune donnée d’essai randomisé concernant la radiothérapie ou la radio-chimiothérapie adjuvante. La seule étude de phase II disponible, non randomisée, n’a inclus que des patients avec cholangiocarcinome extra-hépatique ou carcinome de la vésicule biliaire pT2-T4 ou N+ ou R1, et la radio-chimiothérapie adjuvante (avec capécitabine) a été administrée après 3 mois de chimiothérapie adjuvante par gemcitabine plus capécitabine (Ben-Josef 2015). Les résultats montraient une survie globale à 2 ans similaire pour les résections R0 et R1, suggérant un rattrapage du mauvais pronostic habituel des résections R1. La méta-analyse citée précédemment (Horgan 2012) ne suggérait pas de bénéfice de la radiothérapie seule, et un bénéfice plus net à la chimiothérapie seule qu’à la radio-chimiothérapie, de sorte que l’apport spécifique de la radiothérapie reste non démontré à ce jour. En pratique, il est difficile de savoir comment articuler la radio-chimiothérapie adjuvante avec une chimiothérapie adjuvante de 6 mois par capécitabine. On ne peut exclure que différer la chimiothérapie adjuvante par capécitabine après une éventuelle radio-chimiothérapie adjuvante puisse être délétère, comme dans l’essai ESPAC-1 dans le cancer du pancréas (Neoptolemos 2004). Ces incertitudes pourront être clarifiées par l’essai de phase III allemand ACTICCA-1 en cours, qui évalue non seulement une chimiothérapie adjuvante par CISGEM (vs chirurgie seule initialement, désormais vs capécitabine par amendement après les résultats de l’essai BILCAP), mais aussi l’apport d’une radiochimiothérapie avec capécitabine en cas de statut R1.
8.5.2. Traitements palliatifs
La survie globale médiane en cas de tumeur non résécable est de 9 à 15 mois (Endo 2008, Eckel 2007, Valle 2010, Sharma 2010). L’objectif premier du traitement palliatif doit être le maintien ou l’amélioration de la qualité de vie. Les soins de support doivent accompagner la prise en charge des cancers biliaires quel qu’en soit le stade, dès le diagnostic : drainage si obstacle biliaire, traitement antalgique, prise en charge nutritionnelle, activité physique adaptée (cf. chapitre 17 du TNCD https://www.snfge.org/content/17-nutrition-et-activite-physique-0)...
Les soins de support (hors traitement antitumoral) ne doivent pas être différés du seul fait de l’absence de confirmation histologique.
8.5.2.1. Chirurgie palliative
Les résections macroscopiquement incomplètes (R2) n’ont pas d’intérêt palliatif.
Les dérivations (et les intubations transtumorales) biliaires chirurgicales ne sont pas supérieures au drainage biliaire endoscopique ou radiologique. La mortalité (> 25% dans plusieurs séries) et la morbidité ne sont pas négligeables. Toutefois, le drainage biliaire chirurgical permet généralement une palliation prolongée.
L’efficacité antalgique de la neurolyse cœliaque n’est pas démontrée pour les cancers biliaires.
8.5.2.2. Drainage biliaire
Le drainage en cas d’obstruction biliaire est le premier temps de la prise en charge thérapeutique. Il est urgent en cas d’angiocholite. Il est indispensable si une bilirubinémie normale est requise avant chimiothérapie. Il doit être confié à un centre expert en endoscopie et radiologie biliaires interventionnelles. La cholangio-IRM est l'examen de choix pour planifier la pose de drain(s) ou prothèse(s).
Le drainage biliaire palliatif allonge la survie des patients (Barkay 2013). Le drainage doit être anatomiquement le plus complet possible. Il doit privilégier les secteurs fonctionnels. Le risque iatrogène doit être minimisé et doit pour cela comporter une antibiothérapie péri-opératoire et concerner tout secteur opacifié lors de la cholangiographie (Vienne 2010). La voie d’abord dépend du site et de l’extension du cancer : rétrograde endoscopique dans les cholangiocarcinomes extra-hépatiques distaux (percutanée si échec), rétrograde endoscopique ou percutanée trans-hépatique, voire échoendoscopique transgastrique (selon les compétences locales) dans les cholangiocarcinomes péri-hilaires (Sharaiha 2017, Moryoussef 2017). Les prothèses métalliques non couvertes sont plus longtemps perméables que les prothèses plastiques, notamment en l’absence de métastases hépatiques et pour une taille tumorale < 3 cm et une localisation sous-hilaire (Almadi 2016, Sangchan 2012, Almadi 2017, Hong 2013). Les prothèses couvertes n’ont pas d’avantage démontré en situation palliative. Les prothèses métalliques hilaires non couvertes sont à réserver strictement aux traitements palliatifs (chirurgie définitivement exclue). La pose d’une prothèse métallique unilatérale sur un obstacle tumoral hilaire pourrait selon certains être aussi efficace qu’une pose bilatérale. Cependant, les gestes ultérieurs peuvent être rendus plus difficiles : leur pose doit être soigneusement réfléchie par un opérateur expérimenté (Dumonceau 2018). Une destruction locale par radiofréquence endocanalaire endoscopique peut être discutée en cas de difficulté de drainage d’un secteur hépatique fonctionnel ou d’obstruction tumorale prothétique précoce (Laquière 2016). Les résultats de plusieurs essais randomisés récents sont discordants quant au bénéfice de la radiofréquence sur la survie et la durée de fonctionnalité des prothèses (Yang 2018, Gao 2021, Kang 2021, Andrasina 2021). Le drainage externe percutané est une solution de dernier recours en cas d’échec ou d’impossibilité du drainage prothétique interne. Si cela est possible, on privilégiera au drainage purement externe (extrémité du drain en amont de la sténose), un drain interne-externe (perforé en amont et en aval de la sténose) permettant un passage de bile vers le tube digestif et potentiellement de fonctionner temporairement clampé.
8.5.2.3. Radiothérapie et radio-chimiothérapie palliatives
Aucun essai randomisé contrôlé n’a démontré un bénéfice de survie de la radiothérapie, seule ou associée à une curiethérapie, ou de la radio-chimiothérapie dans les cancers biliaires localement avancés.
L’essai randomisé de phase III FFCD 9902 a comparé chez des patients atteints de cancer biliaire localement avancé (non résécable, non métastatique) une radio-chimiothérapie (50 Gy, 5FU et cisplatine) à une chimiothérapie systémique par GEMOX (Phelip 2014). L’essai a été fermé prématurément après 34 inclusions sur 72 prévues du fait d’un rythme d’inclusion insuffisant, réduisant de fait sa puissance statistique. La survie sans progression a été de 11,0 et 5,8 mois (HR : 0,65 [IC : 0,32-1,33]) et la survie globale de 19,9 et 13,5 mois (HR : 0,69 [IC : 0,31-1,55]) respectivement dans les bras chimiothérapie et radio-chimiothérapie.
Une revue systématique récente a colligé 17 études sur la radiothérapie ou la radio-chimiothérapie des cholangiocarcinomes intra-hépatiques non résécables (541 patients) (Edeline 2021). La survie globale médiane a été en moyenne de 18,9 mois. La comparaison avec les traitements systémiques est difficile compte tenu de l’hétérogénéité des études disponibles, majoritairement rétrospectives, unicentriques et de petite taille. Cependant, des données prospectives concernant spécifiquement la radiothérapie stéréotaxique pourraient faire poser des indications dans des tumeurs uniques non opérables et non traitables par radiofréquence (Frakulli, Brit J Radiol 2019).
8.5.2.4. Traitements intra-artérielle hépatiques
Les traitements intra-artériels hépatiques (chimiothérapie, embolisation, chimio-embolisation, radio-embolisation) sont proposés aux patients avec cholangiocarcinome intra-hépatique non résécable, soit en première intention, soit après progression tumorale sous traitement systémique. Le niveau de preuve de l’efficacité de ces traitements est faible, les études disponibles étant quasiment toutes non randomisées et le plus souvent unicentriques, rétrospectives, de petite taille et hétérogènes, notamment quant à la sélection des patients (traitements antérieurs, taille et nombre de lésions traitées, présence d’une invasion macrovasculaire ou d’une maladie extra-hépatique…), les techniques employées et les critères de jugement (Edeline 2021).
Une revue systématique récente a colligé : 27 études sur la radio-embolisation (1232 patients ; chimiothérapie systémique concomitante chez 29,9 % des patients) ; 22 études sur la chimio-embolisation, conventionnelle ou par billes chargées (1145 patients ; chimiothérapie systémique concomitante chez 74,4% des patients) ; 16 études sur la chimiothérapie intra-artérielle (5-fluoro-uracile, floxuridine, gemcitabine, oxaliplatine, cisplatine, épirubicine, mitomycine C, etc. ; 331 patients ; chimiothérapie systémique concomitante chez 96 % des patients) (Edeline 2021). Le taux de réponse objective a été en moyenne de 23,4 %, 26,3 % et 41,3 % avec la radio-embolisation, la chimio-embolisation et la chimiothérapie, respectivement. La survie sans progression a été en moyenne de 7,8, 15,0 et 10,1 mois et la survie globale de 14,1, 15,9 et 21,3 mois, respectivement. La comparaison des différents traitements intra-artériels est rendue difficile par la grande hétérogénéité des populations incluses. Les résultats du seul essai randomisé disponible (gemcitabine-cisplatine plus chimio-embolisation avec billes chargées d’irinotécan vs gemcitabine-cisplatine) ont été en faveur de la combinaison : taux de résection/ablation secondaire plus élevé (25 % vs 8%, p < 0,005), survie globale médiane plus longue (33,7 vs 12,6 mois, p = 0,048) (Martin 2020). La radio-embolisation par microsphères d’yttrium 90 (Therasphere®, Biocompatibles UK Limited, Groupe BTG International, UK) est approuvée en France pour le traitement palliatif de première ligne, avec ou sans association à une chimiothérapie systémique, des cholangiocarcinomes intra-hépatiques non résécables ou récidivant après résection, sans maladie extra-hépatique, avec charge tumorale <50%, chez des patients présentant un indice de performance préservé (0-1 en association à une chimiothérapie concomitante ou 0-2 si Therasphere® seul) et une fonction hépatique préservée.
8.5.2.5. Traitements palliatifs systémiques
8.5.2.5.1. Chimiothérapie
8.5.2.5.1.1. Chimiothérapie de première ligne
Les résultats des essais randomisés disponibles démontrent la supériorité d’une bi-chimiothérapie comportant un platine, principalement avec gemcitabine, sur une monothérapie par fluoropyrimidine ou gemcitabine ou sur les meilleurs soins de support exclusifs. Dans un essai de phase III scandinave chez 90 patients avec cancer biliaire ou pancréatique avancé, une chimiothérapie par 5FU et acide folinique (plus étoposide chez les patients en bon état général) n’a pas été significativement supérieure aux soins de support exclusifs dans le sous-groupe des patients avec cancer biliaire, et la toxicité a été importante (grade 3-4 : 41%) (Glimelius 1996). Un essai de phase III monocentrique indien chez 81 patients avec carcinome de la vésicule biliaire avancé a montré un bénéfice de survie globale d’une association gemcitabine-oxaliplatine par rapport aux soins de support exclusifs, mais aussi par rapport à une association 5FU-acide folinique (9,5, 4,5 et 4,6 mois respectivement, p=0,039) (Sharma 2010). Un essai randomisé de phase II italien a montré la supériorité d’une association 5FU, acide folinique et oxaliplatine (schéma FOLFOX) par rapport à une association 5FU-acide folinique (schéma LV5FU2) (survie globale : 13,0 vs 7,5 mois ; p=0,001) (Schinzari 2017). Dans une revue systématique de 104 études de chimiothérapie de première ligne rapportés entre 1985 et 2006 (5 à 65 patients par étude, 2810 patients analysés au total) et tous non randomisés sauf trois (deux de phase II et un de phase III sur 47 patients), les taux de réponse objective et de contrôle tumoral les plus élevés étaient obtenus avec les schémas associant gemcitabine et platine (cisplatine ou oxaliplatine) (Eckel 2007). Une actualisation des données portant sur 6337 patients inclus dans 161 études, avec une extension aux thérapies ciblées, a été publiée en 2014 par les mêmes auteurs (Eckel 2014). L’analyse groupée montrait des taux de réponse objective et de contrôle tumoral de respectivement 25,9% et 63,5%, et des médianes de survie sans progression et de survie globale de 5,3 mois et 9,5 mois chez les patients traités par un schéma gemcitabine-platine.
Surtout, l’essai de phase III britannique ABC-02 a démontré chez 410 patients (indice de performance ECOG 0-1 : 88% et bilirubinémie totale < 1,5 N) la supériorité de l’association cisplatine-gemcitabine (CISGEM, cisplatine 25 mg/m2, gemcitabine 1000 mg/m2, jours 1 et 8, toutes les 3 semaines) administrée pendant 24 semaines sur la gemcitabine seule (survie globale : 11,7 vs. 8,1 mois ; HR : 0,64 ; IC : 0,52-0,80 ; p < 0,001), indépendamment du stade (localement avancé ou métastatique) et de la localisation du cancer biliaire (Valle 2010). A noter qu’en analyse de sous-groupes, la combinaison n’a été bénéfique qu’en cas d’indice de performance 0-1. La tolérance de la combinaison a été acceptable, et la faible dose unitaire de cisplatine ne requiert qu’une hydratation réduite. Ces résultats ont été confortés par ceux de l’essai randomisé de phase II japonais BT-22 chez 84 patients (Okusaka 2010), repris avec ABC-02 dans une analyse groupée (Valle 2014). A noter que la durée d’administration double dans l’essai BT-22 (48 semaines) n’a pas semblé améliorer les résultats. L’intérêt d’une poursuite de la chimiothérapie par CISGEM au-delà de 24 semaines (Okusaka 2010), ou d’une maintenance par gemcitabine seule, n’est pas démontré à ce jour car elles n’ont fait l’objet que d’études rétrospectives ou prospectives de faible ampleur suggérant un éventuel bénéfice en survie sans progression mais sans amélioration de la survie globale (Hyung 2019, Sharma 2021).
L’association gemcitabine-oxaliplatine (schéma GEMOX) a été évaluée dans de nombreuses études, dont plusieurs essais prospectifs (André 2004, Malka 2014, Phelip 2014). Dans une revue systématique de 33 études portant sur 1470 patients, la médiane de survie globale était de 9,7 mois dans le groupe gemcitabine-cisplatine et de 9,5 mois dans le groupe gemcitabine-oxaliplatine et la médiane de survie sans progression de 6,3 et 4,9 mois respectivement (Fiteni 2014). La chimiothérapie à base de cisplatine était associée à une toxicité significativement supérieure (asthénie grade 3 et 4, diarrhée, toxicité hépatique et toxicité hématologique). La survie globale médiane augmentait de 9,7 à 11,7 mois dans une analyse de sensibilité restreinte aux études avec un schéma cisplatine standard (25-35 mg/m² jours 1 et 8), mais au prix d’une toxicité restant supérieure à celle des schémas gemcitabine-oxaliplatine. Un essai randomisé de phase III indien de non-infériorité a comparé un schéma GEMOX modifié (gemcitabine 900 mg/m², oxaliplatine 80 mg/m², jour 1 et 8 toutes les 3 semaines, maximum 6 cycles) au schéma CISGEM (maximum 8 cycles) chez 260 patients atteints de carcinome vésiculaire avancé avec indice de performance 0 à 2 (Sharma 2019). La neuropathie périphérique et la thrombopénie ont été plus fréquentes avec le mGEMOX et la néphrotoxicité avec le CISGEM. Malgré une médiane de survie globale numériquement supérieure dans le bras mGEMOX (9,0 mois vs 8,3 mois ; HR : 0,78 ; IC95% : 0,60-1,02 ; p=0,057), cet essai n'a pas réussi à démontrer l'équivalence des deux schémas (différence de médiane : 0,8 mois, borne supérieure de l’IC95% supérieure à 2 mois [-1,1-2,7]), ni une éventuelle supériorité du mGEMOX. Un essai randomisé de phase III de non-infériorité a comparé en première ligne chez 222 patients avec cancer biliaire avancé CAPOX (capécitabine-oxaliplatine) et GEMOX modifié (gemcitabine 1000 mg/m² jours 1 et 8, oxaliplatine 100 mg/m² jour 1, toutes les 3 semaines), pour 8 cycles au total (Kim 2019). La survie sans progression médiane a été de 5,8 mois dans le bras CAPOX contre 5,3 mois dans le bras GEMOX, pour une survie sans progression à 6 mois (critère de jugement principal de l’essai) de 46,7% et 44,5% respectivement (non-infériorité démontrée). Il n’y avait pas de différence en termes de taux de réponse et de survie globale.
L'essai randomisé de phase II PRODIGE 38-AMEBICA a comparé la chimiothérapie par FOLFIRINOX modifié (5-fluorouracile, acide folinique, irinotécan et oxaliplatine) au standard CISGEM (Phelip 2021). L’étude était négative pour son critère de jugement principal, le taux de survie sans progression à 6 mois (51,1 % avec le FOLFIRINOX modifié contre 59,0% avec le CISGEM), et l’évaluation du FOLFIRINOX n’a pas été poursuivie en phase III.
L'essai randomisé de phase III SWOG 1815 a évalué l’addition du nab-paclitaxel au CISGEM chez 441 patients (Shroff 2023). Les résultats présentés en congrès étaient négatifs pour son critère de jugement principal, la survie globale (médiane 14 mois avec le CISGEM-nab-paclitaxel contre 12,7 mois avec le CISGEM ; HR 0,93, IC95% 0,74-1,19, p=0,58), de même que pour le taux de réponse (34 % vs 25 %, p=0,11) et la survie sans progression (médiane 8,2 vs 6,4 mois ; HR 0,92, IC95% 0,72-1,16, p=0,47). La toxicité hématologique a été supérieure dans le bras triplet (grade 3-4 : 60% vs 45 %, p=0,003).
En Asie, où le composé S-1 est disponible, un essai randomisé de phase II sud-coréen a montré chez 96 patients une efficacité comparable des combinaisons gemcitabine-cisplatine (schéma différent du CISGEM) et S-1-cisplatine (Kang 2012). L’association gemcitabine-S-1 a été montrée supérieure au S-1, mais pas à la gemcitabine dans trois essais randomisés de phase II asiatiques (Sasaki 2013, Morizane 2013, Li 2016). Une étude de phase III chez 354 patients a démontré la non-infériorité de l’association gemcitabine-S-1 par rapport à l’association gemcitabine-cisplatine (survie globale médiane : 15,1 vs 13,4 mois ; survie sans progression médiane : 6,8 vs 5,8 mois) (Morizane 2019). Enfin, une étude de phase III chez 246 patients a montré la supériorité du triplet gemcitabine-cisplatine-S-1 sur le doublet gemcitabine-cisplatine (survie globale médiane : 13,5 vs 12,6 mois, HR 0,79, IC95% 0,60-1,04, p = 0,046 ; survie sans progression médiane : 7,4 vs 5,5 mois, HR 0,75, IC95% 0,58-0,97 ; p = 0,0015 ; taux de réponse : 41,5 % vs 15,0 %) (Sakai 2018). Néanmoins, la non-disponibilité du S-1 en France limite la portée pratique de ces résultats.
L'essai allemand NIFE était un essai de phase II randomisé et non comparatif, dans lequel des patients atteints de cholangiocarcinome intra- ou extra-hépatique naïfs de chimiothérapie et avec un indice de performance ECOG 0 ou 1 ont reçu soit une chimiothérapie par CISGEM, soit une association de 5FU-leucovorine avec l’irinotécan nano-liposomal chez 93 patients recrutés dans 21 centres allemands (Perkhofer 2021). Le critère principal a été atteint avec un taux de survie sans progression à 4 mois de 51% avec l’association 5FU-leucovorine-irinotécan nano-liposomal, mais ne semblant cependant pas supérieur au bras standard (59,5% avec le schéma CISGEM). La survie sans progression médiane était de 6,0 mois avec l’association 5FU-leucovorine-irinotécan nano-liposomal et de 6,9 mois avec le schéma CISGEM. La survie globale médiane (données non matures) était de 15,9 mois et 13,6 mois, et le taux de réponse globale était de 24,5% et 11,9%, respectivement. Un effet différentiel était observé selon la localisation de la tumeur primitive, avec une survie sans progression médiane dans les cholangiocarcinomes intra-hépatiques de 3,5 mois avec l’association 5FU-leucovorine-irinotécan nano-liposomal contre 7,7 mois avec le schéma CISGEM (survie globale médiane 14,2 contre 16,4 mois, n=66), et 9,6 contre 1,8 mois dans les cholangiocarcinomes extra-hépatiques (survie globale médiane 18,2 contre 6,3 mois, n=25). Les effectifs de cette analyse de sous-groupes étaient toutefois faibles.
Les résultats de l’essai contrôlé randomisé international de phase III TOPAZ-1 montrent un bénéfice en taux de réponse, survie sans progression et survie globale du durvalumab comparativement à un placebo, administrés jusqu’à progression en association à une chimiothérapie de première ligne par CISGEM (8 cycles maximum), chez des patients atteints de cancer biliaire avancé en bon état général (indice de performance 0 ou 1) (Oh 2022a). La magnitude de ce bénéfice était toutefois modérée (taux de réponse : 26,7 % vs 18,7 % ; survie sans progression médiane : 7,2 vs 5,7 mois, HR : 0,75, IC95 0,63-0,89, p=0,001 ; survie globale médiane : 12,8 vs 11,5 mois, HR : 0,80, IC95 0,66-0,97, p=0,021). Le bénéfice de survie globale se maintenait toutefois à plus long terme dans une analyse actualisée, avec une médiane de 12,9 vs 11,3 mois (HR 0,76, IC95 0,64-0,91) et un taux de survie globale à 24 mois de 23,6 % vs 11,5 % (Oh 2022b). En analyse de sous-groupes, le bénéfice de survie globale semblait moindre chez les patients non asiatiques, en cas de carcinome de la vésicule biliaire et en l’absence d’immunomarquage anti-PD-L1 (score TAP < 1%) (Oh 2022b). En revanche, le bénéfice de survie sans progression ou de survie globale semblait similaire chez les patients avec ou sans altération moléculaire tumorale (TP53, KRAS, IDH1, FGFR2, BRCA, BRAF…) (Valle 2022). Le durvalumab a obtenu le 16 décembre 2022 une autorisation européenne de mise sur le marché, et est actuellement disponible en France via une autorisation d’accès précoce (AAP). Récemment, les résultats d’un autre essai contrôlé randomisé international de phase III (KEYNOTE-966), comparant pembrolizumab (200 mg toutes les 3 semaines, maximum 35 cycles) et placebo en association à une chimiothérapie par CISGEM chez 1069 patients, ont montré des résultats similaires en termes de survie globale (médiane : 12,7 vs 10,9 mois ; HR 0,83 [IC95% 0,72-0,95]; p=0,0034) (Kelley 2023).
8.5.2.5.1.2. Chimiothérapie de deuxième ligne et au-delà
L’intérêt d’une deuxième ligne de chimiothérapie était jusqu’à récemment mal évalué dans la littérature. Les études disponibles, très majoritairement non randomisées et pour la plupart rétrospectives, rapportent des taux de réponse faibles (3-12 %) et des médianes de survie sans progression (1,9-4,0 mois) et de survie globale (6,2-11,0 mois) modestes (Walter 2013, Lamarca 2014, Brieau 2015, Fornaro 2015, Kim 2017, Neuzillet 2019).
L’essai randomisé britannique ABC-06 (le seul essai de phase III rapporté à ce jour) a comparé un schéma FOLFOX associé aux meilleurs soins de support seuls chez 162 patients avec cancer biliaire avancé, en bon état général (indice de performance 0-1) et dont la maladie avait progressé sous (ou après) CISGEM (Lamarca 2021). Les patients traités par FOLFOX ont eu une amélioration de la survie globale (objectif principal ; médiane : 6,2 vs. 5,3 mois, HR : 0,69 [IC95% 0,50-0,97], p=0,031) ; la survie globale à 12 mois était en faveur du bras FOLFOX (25,9 % vs. 11,4 %). Le FOLFOX a été aussi voire plus efficace chez les patients résistant au cisplatine (progression pendant ou dans les 3 mois suivant la première ligne par CISGEM). Le taux de réponse a été faible, de l’ordre de 5%. La chimiothérapie a été associée à plus de neutropénies, d’asthénie et d’infections et à trois décès toxiques.
Un essai randomisé de phase II italien chez 57 patients avec indice de performance 0-2 a montré des taux de survie sans progression à 6 mois similaires avec la capécitabine seule (2/28 patients, 8 %) ou combinée à la mitomycine C (3/29 patients, 10%) (Cereda 2016). Dans un essai randomisé de phase II chinois ayant comparé chez 60 patients en bon état général (indice de performance 0-1) avec cancer biliaire avancé ayant progressé après gemcitabine et cisplatine en première ligne l’association capécitabine-irinotécan (irinotécan 180 mg/m² J1, capécitabine 1000 mg/m² x2/j, J1 à J10, tous les 14 jours) à l’irinotécan seul, la survie sans progression médiane était de 3,7 vs 2,4 mois (p=0,036), le taux de survie à 9 mois de 60,9 % vs 32,0 % (p=0,045) et la survie globale médiane de 10,1 vs 7,3 mois (p=0,107), au prix d’une toxicité acceptable (Zheng 2018). A l’inverse, l’essai de phase II randomisé GB-SELECT comparant capécitabine-irinotécan (capécitabine : 1700 mg/m²/j de J1 à 14 ; irinotécan : 200 mg/m²) à l'irinotécan seul (240 mg/m²), tous les 21 jours jusqu'à progression, chez 98 patients atteints d'un cancer avancé de la vésicule biliaire dont la maladie avait progressé après une chimiothérapie à base de gemcitabine n’a pas montré de différence en termes de survie globale à 6 mois et de survie globale (médiane : 5,2 vs 6,3 mois, HR 1,02 ; IC95%, 0,64-1,49, p=0,93 ; 38,4% vs 54,2% à 6 mois). La dose a été modifiée chez un plus grand nombre de patients dans le groupe CAPIRI par rapport au groupe irinotécan (13 [27 %] contre 4 [9 %], respectivement, p=0,03) (Ramaswamy 2021). Un essai randomisé de phase II sud-coréen a comparé en deuxième ligne après CISGEM mFOLFIRI (irinotecan 150 mg/m², leucovorine 100 mg/m², 5FU 2400 mg/m² sur 46h) et mFOLFOX (oxaliplatine 100 mg/m², leucovorine et 5FU idem mFOLFIRI) toutes les 2 semaines chez 118 patients avec cancer biliaire avancé et indice de performance ECOG 0 à 2 (Choi 2021). Il n’y a pas eu de différence entre mFOLFOX et mFOLFIRI tant en taux de réponse objective (5,9 % vs 4,0 %, p=0,66) qu’en taux de contrôle de la maladie (66,7% vs 64,0%, p=0,78), survie sans progression (médiane : 2,8 vs 2,1 mois ; p=0,97), ou survie globale (médiane : 6,3 vs 5,7 mois, p=0,68 ; 54,1 % vs 44,1 % à 6 mois). Il y a plus de neuropathie périphérique (37,5 % vs 5,2 %) et de thrombopénie (35,7 % vs 15,5 %) avec le mFOLFOX et plus de vomissements (19,0 % vs 1,8 %) et d’angiocholites (10,3 % vs 0,0 %) avec le mFOLFIRI. Aucun décès lié à la chimiothérapie n'a été signalé.
Les résultats actualisés de l’essai randomisé de phase II sud-coréen NIFTY, montrent avec une combinaison 5FU, leucovorine et irinotécan nano-liposomal une amélioration de la survie sans progression (médiane : 4,2 vs 1,7 mois, HR 0,61 [IC95% : 0,44-0,86], p=0,004), de la survie globale (médiane : 8,6 vs 5,3 mois, HR 0,68 [IC95% : 0,48-0,95], p=0,02) et du taux de réponse (12,5 % vs 3,5 %, p=0,04) par rapport au schéma 5FU-leucovorine seul (Hyung 2023). En revanche, les résultats de l’essai randomisé de phase II allemand NALIRICC - AIO-HEP-0116 (5FU-leucovorine +/- irinotécan nano-liposomal) chez 100 patients en échec d'une première ligne avec gemcitabine et à l'état général conservé (indice de performance ECOG 0 ou 1) ne montrent aucun bénéfice à l'ajout d'irinotécan nano-liposomal au LV5FU2 en termes de survie sans progression, critère de jugement principal de l'étude (médiane 2,64 vs 2,30 mois, HR 0,867, IC95 0,559-1,345) ou de survie globale (médiane 6,90 vs 8,21 mois, HR 1,082, IC95 0,681-1,720), même si le taux de réponse était supérieur (14,3 % versus 3,9 %) (Vogel 2022). La toxicité de grade 3 ou plus a été plus fréquente dans le bras combiné (70,8 % vs 50 %).
Aucun essai randomisé n’a évalué l’intérêt d’une chimiothérapie au-delà de la deuxième ligne.
8.5.2.5.2. Traitements ciblés
Tous les essais randomisés rapportés à ce jour ont échoué à démontrer, chez des patients atteints de cancer biliaire avancé non sélectionnés, un bénéfice de survie de l’association à une chimiothérapie d’une thérapie ciblée, notamment anti-EGFR (Malka 2014, Chen 2015) ou anti-angiogénique (Moehler 2014, Santoro 2015, Valle 2015).
Les études de séquençage haut débit de l’ADN et de l’ARN (NGS : Next Generation Sequencing et RNAseq : RNA sequencing) ont montré l’hétérogénéité moléculaire des cancers biliaires et leur richesse en altérations géniques tumorales accessibles à un ciblage thérapeutique : IDH1, FGFR2, HER2, BRAF, MSI, NTRK… (Jain 2016, Farshidfar 2017, Verlingue 2017, Nakamura 2015, Jusakul 2017, Nepal 2018, Zehir 2017). Plusieurs études ont montré l’intérêt clinique d’un tel ciblage moléculaire tumoral :
- Les résultats de l'étude de phase III ClarIDHy ont été les premiers à démontrer l'intérêt clinique d'un traitement ciblé dans les cancers biliaires (Abou-Alfa 2020a, Zhu 2021). Ils ont montré que l'ivosidénib, un médicament oral ciblant la mutation du gène de l'isocitrate déshydrogénase 1 (IDH1), détectée chez environ 15 % des patients atteints de cholangiocarcinome avancé (très majoritairement intra-hépatique), améliorait significativement la survie sans progression par rapport au placebo (2,7 vs 1,4 mois ; HR : 0,37 ; IC 95% : 0,25-0,54, p<0,001) chez des patients avec cholangiocarcinome avancé en échec d’une à deux lignes de traitement systémique et à l’état général conservé (indice de performance 0 ou 1). Le taux de survie sans progression à 6 et 12 mois était de 32 % et 22 % respectivement avec l'ivosidénib, contre 0 % et 0 % dans le groupe placebo. L’amélioration de la survie globale (10,3 vs 7,5 mois ; HR : 0,79, p = 0,09) était significative après analyse statistique prenant en compte le crossover des patients ayant reçu l’ivosidénib après progression dans le bras placebo (70 % des patients ; 10,3 vs 5,1 mois ; HR : 0,49, p < 0,001). L’ivosidénib est actuellement disponible en AAP. Il n’y a pas d’indication à l’ivosidénib en cas de mutations de IDH2, plus rares, qui relèveraient d’autres inhibiteurs dans le cadre d’essais thérapeutiques.
- Les fusions et réarrangements du gène du récepteur 2 du facteur de croissance des fibroblastes (FGFR2) s’observent dans environ 15 % des cholangiocarcinomes, très majoritairement intra-hépatiques. Plusieurs essais non randomisés de phase I/II ou II suggèrent l’intérêt des inhibiteurs oraux de FGFR2 dans ce sous-groupe, avec en deuxième ligne et au-delà, des taux de réponse objective de l’ordre de 20-40 %, des médianes de survie sans progression de l’ordre de 7 à 9 mois et des médianes de survie globale de l’ordre de 12 à 20 mois (Abou-Alfa 2020b, Javle 2021b, Mazzaferro 2019, Goyal 2023, Nogova 2017, Papadopoulos 2017). Parmi ces inhibiteurs de FGFR2, seuls le pémigatinib et le futibatinib disposent d’une autorisation de mise sur le marché européenne chez les patients atteints d’un cholangiocarcinome localement avancé ou métastatique avec fusion ou réarrangement de FGFR2 en rechute ou réfractaires après au moins une ligne de traitement systémique. Le pémigatinib est actuellement remboursé. Des essais de phase III de première ligne sont en cours.
- Les altérations du gène HER2 (ERRB2 ; amplifications, surexpression, moins souvent mutations) s’observent très majoritairement dans les cancers biliaires extra-hépatiques (cholangiocarcinomes péri-hilaires et distaux, adénocarcinomes de la vésicule biliaire, adénocarcinomes ampullaires), avec une fréquence autour de 15 %. Un essai non randomisé de phase II d’une combinaison de deux anticorps monoclonaux anti-HER2 (trastuzumab et pertuzumab) chez 39 patients atteints de cancer biliaire métastatique précédemment traités avec amplification de HER2, surexpression de HER2 ou les deux et un indice de performance ECOG de 0 à 2 a montré un taux de réponse objective de 23 % (Javle 2021a). Le zanidatamab, un anticorps anti-HER2 bispécifique, a montré dans une étude de phase I chez 21 patients atteints de cancer biliaire avancé HER2 positif une bonne tolérance et une efficacité encourageante avec 38% de réponses objectives et 62% de contrôle tumoral (Meric-Bernstam 2022) ; il a obtenu une AAC dans l’attente de la présentation des résultats de l’étude de phase II. Le trastuzumab-deruxtecan, un anticorps anti-HER2 conjugué à un inhibiteur de la topoisomérase I, a montré des résultats encourageants dans l'essai de phase 2 HERB chez 22 patients prétraités avec cancer biliaire HER2 positif et 8 avec cancer biliaire HER2 faible (statut IHC/ISH 0/+, 1+/-, 1+/+ ou 2+/-), avec un taux de réponse objective de 36,4 % et 12,5 %, respectivement, au prix d’une toxicité principalement hématologique, mais aussi pulmonaire avec des pneumopathies interstitielles parfois létales (Ohba 2022). La combinaison FOLFOX-trastuzumab, évaluée en deuxième ou troisième ligne chez 34 patients avec cancer biliaire HER2 positif (IHC2+/ISH+ ou IHC3+) dans l’essai de phase II sud-coréen KCSG-HB19-14, a produit un taux de réponse de 29,4 %, une survie sans progression médiane de 5,1 mois et une survie globale médiane de 10,7 mois (Lee 2023). On ne dispose pas de données d’efficacité en population non asiatique. La combinaison du tucatinib, un inhibiteur de tyrosine kinase anti-HER2 oral, au trastuzumab chez 30 patients prétraités avec cancer biliaire métastatique HER2 surexprimé ou amplifié dans l’essai de phase II SGNTUC-019 a produit un un taux de réponse de 46,7%, une survie sans progression médiane de 5,5 mois et un taux de survie globale à 12 mois de 53,6 % (Nakamura 2023).
- Les mutations V600E du gène BRAF s’observent dans environ 5 % des cancers biliaires (majoritairement des cholangiocarcinomes intra-hépatiques). Un essai non randomisé de phase II d’une association de dabrafénib (inhibiteur de BRAF) et tramétinib (inhibiteur de MEK) chez 43 patients atteints de cancer biliaire avancé précédemment traités avec mutation BRAF V600E et un indice de performance ECOG de 0 à 2 a montré un taux de réponse objective de 47 % (Subbiah 2020).
- Une instabilité des microsatellites (MSI) ou une déficience du système MMR (dMMR), constitutionnelle (syndrome de Lynch) ou acquise (sporadique), s’observe dans environ 2 % des cancers biliaires avancés. Un essai non randomisé de phase II d’immunothérapie avec le pembrolizumab (anticorps monoclonal anti-PD-1) incluant 22 patients atteints de cancer biliaire avancé MSI/dMMR précédemment traités avec un indice de performance ECOG de 0 à 1 a montré un taux de réponse objective de 40,9 %, analogue au taux (30,8 %) observé dans la population globale de l’essai constituée de 321 patients avec cancer non colorectal avancé MSI/dMMR (Maio 2022).
- Des mutations du gène KRAS s’observent dans environ 20 % des cancers biliaires, dont environ 5 % (soit 1 % des cancers biliaires) sont des mutations G12C, seules accessibles à un ciblage thérapeutique actuellement (Salem 2021). L’adagrasib, un inhibiteur oral spécifique des mutations KRAS G12C, a produit une réponse objective chez 4 des 8 patients (50 %, dont 2 non confirmées) avec cancer biliaire avancé prétraité inclus dans un essai de phase I/II et un contrôle tumoral dans 100 % des cas (Bekaii-Saab 2022). Il n’y a à ce jour pas de données d’activité dans les cancers biliaires concernant le sotorasib, autre inhibiteur oral spécifique des mutations KRAS G12C, approuvé en Europe pour le traitement des cancers bronchiques non à petites cellules avancés prétraités présentant cette mutation, un seul patient avec cancer biliaire a été inclus dans l’essai de phase I publié, avec pour meilleure réponse une stabilité tumorale (Hong 2020).
- Les fusions impliquant l'un des trois gènes de récepteurs neurotrophiques à tyrosine kinase de la tropomyosine (NTRK) s’observent dans < 1% des cancers biliaires (Boilève 2021). Un essai de phase I-II a évalué le larotrectinib, un inhibiteur oral de NTRK, chez 55 patients atteints de 17 types de tumeur avec fusion NTRK (Drilon 2018). Le taux de réponse objective global a été de 75 % (dont un des deux patients atteints de cholangiocarcinome inclus). Dans une analyse groupée de trois essais de phase I-II avec l’entrectinib, autre inhibiteur oral de NTRK, le taux de réponse objective global a été de 57 %, dont le seul patient atteint de cholangiocarcinome inclus (Doebele 2020). Les méthodes de dépistage des fusions NTRK ont fait l’objet de recommandations européennes récentes (Marchiò 2019). Dans une population non sélectionnée où les fusions NTRK sont peu fréquentes (comme les patients avec cholangiocarcinome), il convient de procéder soit à un séquençage NGS en première intention (de préférence par séquençage ARN), soit à un dépistage par immunohistochimie suivi d'un séquençage des cas positifs. Une autorisation européenne de mise sur le marché a été obtenue pour le larotrectinib et l’entrectinib pour le traitement de tumeurs solides ayant une fusion du gène NTRK, mais ces médicaments ne sont actuellement pas remboursés en France.
- D’autres altérations géniques tumorales (BRCA, MET, ERBB3, BAP1, ARID1A, PIK3CA…) n’ont pour l’instant pas fait l’objet d’essais prospectifs publiés.
La richesse des cancers biliaires en altérations géniques tumorales accessibles à un ciblage thérapeutique, et les succès cliniques observés avec plusieurs thérapies ciblées, dont certaines d’ores et déjà disponibles, militent en faveur d’un profilage moléculaire tumoral systématique des cancers biliaires avancés. Un tel profilage moléculaire devrait idéalement être réalisé au cours de la première ligne thérapeutique, pour pouvoir disposer des résultats au moment de la décision de traitement de deuxième ligne. En effet : 1) les altérations oncogéniques drivers surviennent en règle précocement au cours de l’oncogenèse tumorale, et persistent tout au long de l’évolution de la maladie (en l’absence d’une éventuelle pression de sélection thérapeutique par un traitement ciblé) (van de Haar 2021); 2) le délai de mise à disposition des résultats du profilage moléculaire tumoral expose au risque de ne plus pouvoir traiter un patient, en raison d’une altération de l’état général rapide si le profilage est effectué après progression tumorale, ce d’autant que le taux d’attrition des patients d’une ligne à la suivante est élevé dans les cancers biliaires avancés. Le profilage moléculaire tumoral doit permettre de détecter aussi bien les fusions (notamment FGFR2), idéalement par NGS ARN, que les mutations. Il doit être en mesure de détecter toutes les altérations d’intérêt thérapeutique selon la classification européenne ESCAT (ESMO Scale for Clinical Actionability of Molecular Target) (Mateo 2018, Mosele 2020).
En l’absence de matériel tissulaire tumoral disponible et de possibilité de nouvelle biopsie, ou en cas d‘échec du profilage moléculaire tumoral sur tissu, la recherche d’altérations moléculaires tumorales sur ADN circulant peut être envisagée, en notant toutefois que la fiabilité, bonne pour la détection des mutations (IDH1, BRAF V600E,…) (Berchuck 2022, Csoma 2022, Lapin 2022), a été parfois rapportée comme moins bonne (jusqu’à 18% seulement [Berchuck 2022]) pour celle des fusions/réarrangements. La recherche d’ADN tumoral circulant peut être aisément répétée et peut ainsi permettre la détection d’altérations moléculaires tumorales de résistance secondaire à un traitment ciblé (par exemple mutations de FGFR2 après inhibiteur FGFR2) (Goyal 2017, Varghese 2021).
Si le profilage moléculaire n’est pas réalisé, la recherche d’un statut tumoral MSI/dMMR doit en tout état de cause être systématique compte tenu des perspectives d’immunothérapie.
8.6. Indications thérapeutiques
8.6.1. Résection chirurgicale et ablation
REFERENCES
Cholangiocarcinomes
- Intra-hépatiques : résection des segments hépatiques envahis, avec curage ganglionnaire quelle que soit la suspicion d’envahissement sur le bilan préopératoire (grade C). ll est recommandé d’essayer d’obtenir une limite de résection R0 avec une marge de 10 mm et d’obtenir au moins 6 ganglions dans le curage ganglionnaire.
- Extra-hépatiques
- Hile, tiers supérieur de la voie biliaire principale : résection monobloc de la voie biliaire principale et de la convergence biliaire supérieure, hépatectomie incluant la résection des segments I et IVb, curage ganglionnaire pédiculaire ± résection/reconstruction veineuse (grade C). ll est recommandé d’essayer d’obtenir une limite de résection R0 et d’obtenir au moins 5 ganglions dans le curage ganglionnaire.
- Tiers moyen de la voie biliaire principale : résection de la voie biliaire principale, curage ganglionnaire pédiculaire (grade C).
- Tiers inférieur de la voie biliaire principale : duodénopancréatectomie céphalique, curage ganglionnaire pédiculaire (grade C).
- Carcinomes de la vésicule biliaire
- Tis, T1a : cholécystectomie suffisante si vésicule biliaire retirée intacte. Curage ganglionnaire : non recommandé (grade B).
- T1b, T2 : cholécystectomie, résection du lit vésiculaire (segments IVb-V) (tumeur envahissant uniquement le lit vésiculaire et < 20 mm), curage ganglionnaire pédiculaire (grade B).
- > T2 ou N+ : bénéfice de la chirurgie non démontré. Cholécystectomie, résection de la VBP, résection des segments hépatiques envahis, curage ganglionnaire pédiculaire ± résection/reconstruction vasculaire (grade C).
OPTIONS
Une ablation percutanée peut être envisagée pour les cholangiocarcinomes intra-hépatiques uniques < 3 cm sans maladie extra-hépatique si la résection chirurgicale n'est pas possible (grade B).
Une radiothérapie stéréotaxique peut être discutée pour les cholangiocarcinomes intra-hépatiques < 5 cm sans maladie extra-hépatique si la résection chirurgicale et l’ablation percutanée ne sont pas possibles (grade C).
ESSAIS CLINIQUES
Aucun.
8.6.2. Transplantation hépatique
REFERENCES
La transplantation hépatique dans le cadre d’un protocole préopératoire de type Mayo Clinic (radio-chimiothérapie, laparotomie/laparoscopie exploratrice) est admise en cas de cholangiocarcinome péri-hilaire ≤ 3 cm et N0 non résécable (grade B). Elle n’est pas validée pour les cholangiocarcinomes péri-hilaires résécables ni pour les autres cancers biliaires.
ESSAIS CLINIQUES
Aucun.
8.6.3. Traitement néo-adjuvant et adjuvant
REFERENCES
La chimiothérapie, la radiothérapie et la radio-chimiothérapie néo-adjuvante ne peuvent être recommandées compte tenu d’un niveau de preuve insuffisant dans la littérature, et ne devraient être réalisées que dans le cadre d’un essai clinique.
Une confirmation cytologique ou histologique préalable est indispensable avant un éventuel traitement néo-adjuvant.
En cas de réponse à un traitement néo-adjuvant d’un cholangiocarcinome intra-hépatique initialement inopérable, une résection chirurgicale ou d’une ablation à visée curative doit être rediscutée (grade C).
Une chimiothérapie adjuvante par capecitabine pendant 24 semaines (8 cycles) peut être proposée après résection chirurgicale R0 ou R1 d’un cancer vésiculaire avec envahissement de la musculeuse (> pT1) ou d’un cholangiocarcinome intra-hépatique, péri-hilaire ou distal, sous réserve d’un état général conservé (indice de performance 0-1) et d’un délai postopératoire n’excédant pas 16 semaines (grade B).
Il n’est pas recommandé d’utiliser une chimiothérapie adjuvante par gemcitabine seule ou en association.
Si chimiothérapie avec fluoropyrimidine (5FU ou capecitabine) : recherche d’un déficit constitutionnel en DPD recommandée, par phénotypage (dosage de l'uracilémie) (accord d’experts) (HAS 2018). En cas de déficit en DPD partiel : ajustement des doses de 5FU ou capecitabine recommandé ; complet : 5FU ou capecitabine contre-indiquée.
OPTIONS
Une radio-chimiothérapie adjuvante, avec capécitabine et en clôture après 4 à 6 mois de chimiothérapie adjuvante par capécitabine, peut être discutée en cas de résection R1 pour les cholangiocarcinomes péri-hilaires et distaux et les cancers de la vésicule biliaire (avis d’experts).
Génotypage du gène DPYD si uracilémie anormale (accord d’experts).
ESSAIS CLINIQUES
- SIROCHO (EudraCT : 2021-001575-16) : essai de phase II randomisé comparant radio-embolisation néo-adjuvante associée à la capécitabine vs chirurgie d’emblée des cholangiocarcinomes intra-hépatiques opérables à risque de marge positive (coordinateur : Dr Julien Edeline, CLCC Eugène Marquis, Rennes).
https://classic.clinicaltrials.gov/ct2/show/NCT05265208 - IMHOTEP (EudraCT : 2020–004957–62) : essai de phase II évaluant l’intérêt du pembrolizumab en péri-opératoire dans les cancers MSI/dMMR résécables (coordinateur : Dr Christelle de la Fouchardière, CLCC Léon Bérard, Lyon).
https://classic.clinicaltrials.gov/ct2/show/NCT04795661
8.6.4. Traitement palliatif (figure 5)
8.6.4.1. Première ligne
REFERENCES
Drainage biliaire (endoscopique et/ou percutané) recommandé si ictère (grade A).
Selon indice de performance ECOG/OMS (et fonction hépatique) :
- 0-1 : immunothérapie par durvalumab (disponible en AAP) ou pembrolizumab (pas d’AMM à ce jour) (grade A) plus CISGEM (grade A)
- 2 : gemcitabine (ou CISGEM) (grade B)
- 3-4 (et/ou insuffisance hépatique) : soins de support exclusifs (accord d’experts)
- Portrait moléculaire tumoral systématique (grade B), quelle que soit la localisation tumorale, à réaliser dès le traitement de première ligne (voire avant pour orientation vers des essais cliniques), comportant :
- et
- Phénotype HER2 en immunohistochimie, à confirmer par hybridation in situ si HER2+ ou 3+ en immunohistochimie
- Panel NGS (ADN ou ARN) incluant la recherche de mutations tumorales ciblables (incluant IDH1, BRAF, KRAS)
- Recherche de fusions/réarrangements (ARN) incluant les gènes FGFR2 et NTRK
- En cas d’altération moléculaire ciblable par un traitement hors AMM et non accessible via une AAP ou AAC, ou en cas d’altérations moléculaires multiples, les résultats moléculaires devront être discutés et validés en RCP, idéalement moléculaire (accord d’experts).
OPTIONS
- Si contre-indication au cisplatine : GEMOX ; à la gemcitabine : CAPOX (grade B) (si CAPOX : recherche d’un déficit constitutionnel en DPD recommandée, par phénotypage (dosage de l'uracilémie) (accord d’experts) (HAS 2018). En cas de déficit en DPD partiel : ajustement des doses de capecitabine recommandé ; complet : capecitabine contre-indiquée.
- En l’absence de matériel tissulaire tumoral disponible et de possibilité de nouvelle biopsie, ou en cas d‘échec du profilage moléculaire tumoral sur tissu, la recherche d’altérations moléculaires tumorales sur ADN circulant peut être envisagée (accord d’experts)
Traitements locaux
- Il n’est pas recommandé de réaliser un traitement intra-artériel seul si les traitements standards sont possibles.
- Les traitements intra-artériels hépatiques (radio-embolisation, chimio-embolisation, chimiothérapie) et la radiothérapie stéréotaxique peuvent être discutés en cas de cholangiocarcinome intra-hépatique non résécable (ou chez un patient non opérable) sans maladie extra-hépatique.
- Les traitements intra-artériels hépatiques seront combinés à une chimiothérapie systémique (avis d’experts).
- Le choix de la technique dépend de leur disponibilité et de l’expertise locale (grade C).
- Il n’est pas recommandé de proposer un traitement radiologique interventionnel pour les autres cancers biliaires.
- Une résection chirurgicale ou une ablation percutanée devront être discutées en cas de réponse tumorale d’une maladie initialement non résécable.
8.6.4.2. En deuxième ligne et au-delà
REFERENCES
Si altération moléculaire tumorale ciblable (ESCAT I-II ; Mateo 2018, Mosele 2020)) et indice de performance ECOG/OMS 0-2 (et fonction hépatique conservée), traitement ciblé recommandé en première intention, selon l’accessibilité :
- Participation à un essai clinique si disponible
- Mutation IDH1 (ESCAT I-A) : ivosidénib (disponible en AAP en 3ème ligne) (grade A)
- Fusion/réarrangement FGFR2 (ESCAT I-B) : pémigatinib (remboursé), futibatinib (non remboursé ni autorisé en AAP ou AAC) (grade B)
- Amplification/surexpression HER2 (ESCAT I-C) : zanidatamab (disponible en AAC), trastuzumab plus pertuzumab (grade B) (non remboursé ni autorisé en AAP ou AAC); FOLFOX plus trastuzumab (grade B) : pas d’accord consensuel du groupe du travail en l’absence de données en population occidentale (avis d’experts)
- Mutation BRAF V600E (ESCAT I-B) : dabrafénib plus tramétinib (grade B) (non remboursé ni autorisé en AAP ou AAC)
- Statut MSI/dMMR : pembrolizumab (ESCAT I-C) (en l’absence de traitement par durvalumab ou autre anti-PD1/PDL1 en 1ère ligne) (non remboursé ni autorisé en AAP ou AAC) (grade B)
- Mutation KRAS G12C : adagrasib (ESCAT II-B) (non remboursé ni autorisé en AAP ou AAC) (grade C)
- Fusion NTRK : larotrectinib (ESCAT I-C) (non remboursé ni autorisé en AAP ou AAC) (grade B)
N.B. : liste des médicaments accessibles via une AAP ou AAC :
https://ansm.sante.fr/documents/reference/referentiel-des-specialites-en-acces-derogatoireet voir chapitre 20.7 du TNCD https://www.snfge.org/content/20-autres-thematiques-liens-autres-referentiels-soins-oncologiques-de-support-rehabilitation#ancre3206
En l’absence d’altération moléculaire tumorale ciblable identifiée : selon indice de performance ECOG/OMS (et fonction hépatique) :
- 0-1 : FOLFOX (en deuxième ligne de chimiothérapie après CISGEM ou gemcitabine en première ligne) (grade B) ou essai clinique (notamment orienté par portrait moléculaire tumoral ou statut MSI/dMMR)
- 2 : fluoropyrimidine seule (grade C)
- 3-4 (et/ou insuffisance hépatique) : soins de support exclusifs (accord d’experts)
N.B. :
- Pas de standard de chimiothérapie au-delà de la deuxième ligne.
- Si chimiothérapie avec fluoropyrimidine (5FU ou capecitabine) : recherche d’un déficit constitutionnel en DPD recommandée, par phénotypage (dosage de l'uracilémie) (accord d’experts) (HAS 2018). En cas de déficit en DPD : partiel : ajustement des doses de 5FU ou capecitabine recommandé ; complet : 5FU ou capecitabine contre-indiquée.
OPTIONS
En deuxième ligne en cas de contre-indication au FOLFOX (si indice de performance ECOG/OMS 0-1) : FOLFIRI, fluoropyrimidine seule ou irinotécan seul (avis d’experts).
Traitements locaux
- Les traitements intra-artériels hépatiques (radio-embolisation, chimio-embolisation, chimiothérapie) et la radiothérapie stéréotaxique peuvent être discutés en cas de cholangiocarcinome intra-hépatique non résécable (ou chez un patient non opérable) en traitement de recours après échec des traitements standards systémiques en l’absence de progression extra-hépatique (grade C).
- Le choix de la technique dépend de leur disponibilité et de l’expertise locale (grade C).
- Il n’est pas recommandé de proposer un traitement radiologique interventionnel pour les autres cancers biliaires.
- Une résection chirurgicale ou une ablation percutanée devront être discutées en cas de réponse tumorale d’une maladie initialement non résécable.
ESSAI CLINIQUE
- SAFIR ABC10 : essai randomisé de phase III comparant, après 3 mois de chimiothérapie de première ligne par CISGEM +/- durvalumab, la poursuite de ce traitement à la médecine de précision moléculaire (ciblant mutations IDH1, BRAF V600E, BRCA1/2, PALB2, fusions/réarrangements ou mutations FGFR2, amplification ou mutations HER2) (ouverture courant 2023 ; coordinateur : Dr David Malka, Institut Mutualiste Montsouris, Paris).
Figure 5 Cancers biliaires : algorithme thérapeutique
CC : cholangiocarcinome. CISGEM : cisplatine-gemcitabine. CT : chimiothérapie. ESCAT : ESMO Scale for Clinical Actionability of molecular Targets. IH : cholangiocarcinome intra-épatique. IAH : intra-artériels hépatiques. IHC : immunohistochimie. IP : indice de performance. RCP : réunion de concertation pluridisciplinaire. RCT : radiochimiothérapie. RT : radiothérapie.
- Devront être pris en considération : la nécessité d'un drainage biliaire préopératoire ; l’évaluation du futur foie restant ; une chirurgie complémentaire en cas de cancer incident de la vésicule biliaire de stade ≥T1b.
En cas de cytologie/histologie négative à deux reprises, devant un tableau clinique et radiologique évocateur de cholangiocarcinome péri-hilaire/extrahépatique et après cholangioscopie et dosage des IgG4, la prise en charge chirurgicale ne devra pas être retardée en cas de tumeur résécable.
La transplantation épatique dans le cadre d’un protocole préopératoire de type Mayo Clinic (RCT, laparotomie/laparoscopie exploratrice) est admise en cas de CC péri-hilaire ≤ 3 cm N0 non résécable (grade B).
Une ablation percutanée peut être envisagée pour les CCIH uniques < 3 cm sans maladie extra-épatique si la résection chirurgicale n'est pas possible (grade B).
Une RT stéréotaxique peut être discutée pour les CCIH < 5 cm sans maladie extra-épatique si résection chirurgicale et ablation percutanée ne sont pas possibles (grade C). - Les traitements IAH (radio-embolisation, chimio-embolisation, chimiothérapie) et la RT stéréotaxique peuvent être discutés en cas de CCIH non résécable (ou chez un patient non opérable) sans maladie extra-épatique (grade C). Les traitements IAH seront combinés en 1re ligne à une CT systémique (avis d’experts). Une résection chirurgicale ou une ablation percutanée devront être discutées en cas de réponse tumorale d’une maladie initialement non résécable.
- En cas de cytologie/histologie négative à deux reprises, devant un tableau clinique et radiologique évocateur de cholangiocarcinome péri-hilaire/extrahépatique et après cholangioscopie et dosage des IgG4, la possibilité de débuter une chimiothérapie doit être validée en RCP (accord d’experts).
- Si contre-indication au cisplatine : GEMOX ; à la gemcitabine : CAPOX (grade B).
- Portrait moléculaire tumoral systématique (grade B), à réaliser dès le traitement de 1re ligne (voire avant pour orientation vers essais cliniques), comportant :
- Phénotype MMR en IHC, à confirmer par statut MSI en PCR si statut dMMR en IHC
- Phénotype HER2 en IHC, à confirmer par hybridation in situ si HER2+ ou 3+ en IHC
- Panel NGS (ADN ou ARN) incluant la recherche de mutations tumorales ciblables (incluant IDH1, BRAF, KRAS)
- Recherche de fusions/réarrangements (ARN) incluant les gènes FGFR2 et NTRK
En l’absence de matériel tissulaire tumoral disponible et de possibilité de nouvelle biopsie, ou en cas d‘échec du profilage moléculaire tumoral sur tissu, la recherche d’altérations moléculaires tumorales sur ADN circulant peut être envisagée (accord d’experts).
En cas d’altération moléculaire ciblable par un traitement hors AMM et non accessible via une AAP ou AAC, ou en cas d’altérations moléculaires multiples, les résultats moléculaires devront être discutés et validés en RCP, idéalement moléculaire (accord d’experts). - Les traitements IAH (radio-embolisation, chimio-embolisation, chimiothérapie) et la RT stéréotaxique peuvent être discutés en cas de CCIH non résécable (ou chez un patient non opérable) sans maladie extra-épatique (grade C). Les traitements IAH seront utilisés seuls en traitement de recours après échec des traitements standards systémiques en l’absence de progression extra-épatique (grade C). Une résection chirurgicale ou une ablation percutanée devront être discutées en cas de réponse tumorale d’une maladie initialement non résécable.
- FOLFOX plus trastuzumab : pas d’accord consensuel du groupe du travail en l’absence de données en population occidentale (avis d’experts).
- En l’absence de traitement par anti-PD1/PDL1 en 1ère ligne.
- Option : si contre-indication au FOLFOX : FOLFIRI, fluoropyrimidine seule ou irinotécan seul (avis d'experts).
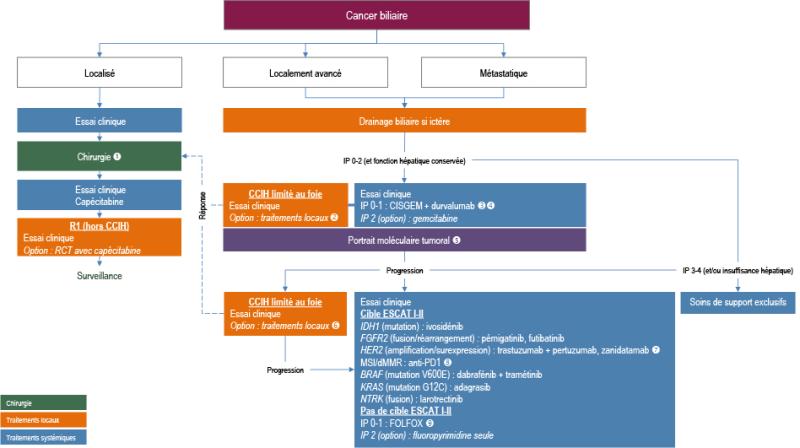
8.7. Surveillance post-thérapeutique
REFERENCES
L’intérêt d’une surveillance n’est pas démontré.
L’intérêt de la répétition des dosages sériques d’un ou plusieurs marqueurs tumoraux pour le suivi au cours du traitement ou la surveillance post-thérapeutique n’est pas démontré.
Une surveillance ne doit être entreprise que chez un patient capable de tolérer le traitement de l’éventuelle récidive tumorale (accord d’experts).
OPTIONS
Après résection à visée curative (accord d’experts) :
- Surveillance clinique et radiologique thoraco-abdomino-pelvienne tous les 3 à 6 mois pendant 2 ans puis tous les 6 mois jusqu’à 5 ans,
- Autres examens (scintigraphie osseuse, TDM cérébrale…) : si signe d'appel.
Après drainage par prothèse biliaire (accord d’experts) :
- Surveillance clinique + bilirubinémie à J8 et J30 puis toutes les 6-8 semaines,
- Ou pas de surveillance systématique (échographie et tests hépatiques si récidive ictérique et/ou signes infectieux).
8.8. Protocoles thérapeutiques
| Protocole | Molécules |
|---|---|
| Chimiothérapies | |
| Capécitabine | 1250 mg/m² x2/j PO de J1 à J14, /21j |
CAPOX J1=J22 | Capécitabine 1000 mg/m² x2/j PO de J1 à J14 Oxaliplatine 130 mg/m² en 2h IV à J1 |
CISGEMa J1, J8=J15 | Cisplatine 25 mg/m² en 1h IV dans 1000 ml NaCl 0,9 % + KCl + MgSO4 puis 500 ml NaCl 0,9 % puis Gemcitabine 1 g/m² en 30 mn IV dans 250 ml NaCl 0,9 % |
FOLFIRI J1=J15 | Irinotécan 180 mg/m² en 90 mn IV à J1 Acide foliniqueb 400 mg/m2 en 2h IV à J1 puis 5FU 400 mg/m2 en bolus IV à J1 puis 5FU 2400 mg/m2 en 46h IV |
FOLFOX J1=J15 | Oxaliplatine 85 mg/m² en 2h IV à J1 Acide foliniqueb 400 mg/m2 en 2h IV à J1 puis 5FU 400 mg/m2 en bolus IV à J1 puis 5FU 2400 mg/m2 en 46h IV |
Gemcitabine J1=J29 | 1 g/m² en 30 mn IV, 7 sem/8 puis 3 sem/4 (ou 3 sem/4 d’emblée) |
GEMOX J1=J15 | Gemcitabine 1 g/m² en 100 mn IV (10 mg/m²/mn) à J1 Oxaliplatine 100 mg/m² (option : 85 mg/m²) en 2h IV à J2 (ou J1) |
LV5FU2 simplifié J1=J15 | Acide foliniqueb 400 mg/m2 en 2h IV à J1 puis 5FU 400 mg/m2 en bolus IV à J1 puis 5FU 2400 mg/m2 en 46h IV |
| Immunothérapies | |
Durvalumab J1=J22 puis J29 | 1500 mg IV à J1, /21j pendant CISGEM, puis /28j |
| Thérapies (et immunothérapies) ciblées | |
| Adagrasib | 600 mg x2/j PO |
| Dabrafenib + trametinib | Dabrafenib 150 mg x2/j PO Trametinib 2 mg/j PO |
| Futibatinib | 20 mg/j PO |
| Ivosidenib | 500 mg/j PO |
| Larotrectinib | 100 mg x2/j PO |
Pembrolizumab J1=J22 ou J43 | 200 mg IV à J1, /21j ou 400 mg IV à J1, /42j |
| Pemigatinib | 13,5 mg/j PO de J1 à J14, /21j |
J1=J22
| Trastuzumab 6 mg/kg (8 mg/kg à C1) IV à J1 Pertuzumab 420 mg (840 mg à C1) IV à J1 |
Zanidatamab J1=J15 | 20 mg/kg IV à J1 |
5FU : 5-fluoro-uracile. C1 : cycle 1. IV : intraveineuse. PO : per os.
1 Ne nécessite pas d’hospitalisation complète ni d’hyperhydratation IV.
2 Ou acide L-folinique 200 mg/m².
8.9. Bibliographie
- Abou-Alfa GK, Macarulla T, Javle MM, et al. Ivosidenib in IDH1-mutant, chemotherapy-refractory cholangiocarcinoma (ClarIDHy): a multicentre, randomised, double-blind, placebo-controlled, phase 3 study. Lancet Oncol 2020a;21:796-807.
- Abou-Alfa GK, Sahai V, Hollebecque A, et al. Pemigatinib for previously treated, locally advanced or metastatic cholangiocarcinoma: a multicentre, open-label, phase 2 study. Lancet Oncol 2020b;21:671-84.
- Almadi MA, Barkun A, Martel M. Plastic vs. self-expandable metal stents for palliation in malignant biliary obstruction: a series of meta-analyses. Am J Gastroenterol 2017;112:260-73.
- Almadi MA, Barkun A, Martel M. Self-expandable metal stents versus plastic stents for malignant biliary obstruction. Gastrointest Endosc 2016;83:852-3.
- Amin MB, Greene FL, Edge SB, et al. The Eighth Edition AJCC Cancer Staging Manual: Continuing to build a bridge from a population-based to a more “personalized” approach to cancer staging. CA Cancer J Clin 2017;67:93-9.
- Andrasina T, Rohan T, Panek J, et al. The combination of endoluminal radiofrequency ablation and metal stent implantation for the treatment of malignant biliary stenosis – Randomized study. Eur J Radiol. 2021;142:109830.
- André T, Tournigand C, Rosmorduc O, et al. Gemcitabine combined with oxaliplatin (GEMOX) in advanced biliary tract adenocarcinoma: a GERCOR study. Ann Oncol 2004;15:1339-43.
- Banales JM, Cardinale V, Carpino G, et al. Cholangiocarcinoma: current knowledge and future perspectives consensus statement from the European Network for the Study of Cholangiocarcinoma (ENS-CCA). Nat Rev Gastroenterol Hepatol 2016;13:261-80.
- Barkay O, Mosler P, Schmitt CM, et al. Effect of endoscopic stenting of malignant bile duct obstruction on quality of life. J Clin Gastroenterol 2013;47:526-31.
- Bekaii-Saab TS, Spira AI, Yaeger R, et al. KRYSTAL-1: Updated activity and safety of adagrasib (MRTX849) in patients (Pts) with unresectable or metastatic pancreatic cancer (PDAC) and other gastrointestinal (GI) tumors harboring a KRASG12C mutation. ASCO Gastrointest Cancer Symposium 2022;A519.
- Ben-Josef E, Guthrie KA, El-Khoueiry AB, et al. SWOG S0809: A Phase II intergroup trial of adjuvant capecitabine and gemcitabine followed by radiotherapy and concurrent capecitabine in extrahepatic cholangiocarcinoma and gallbladder carcinoma. J Clin Oncol 2015;33:2617-22.
- Benson AB, D'Angelica MI, Abrams T, et al. NCCN Guidelines® insights: biliary tract cancers, version 2.2023. J Natl Compr Canc Netw 2023;21:694-704.
- Berchuck JE, Facchinetti F, DiToro DF, et al. The clinical landscape of cell-free DNA alterations in 1671 patients with advanced biliary tract cancer. Ann Oncol 2022;33:1269-83.
- Bird N, Elmasry M, Jones R, et al. Role of staging laparoscopy in the stratification of patients with perihilar cholangiocarcinoma. Br J Surg 2017;104:418-25.
- Bismuth H, Corlette MB. Intrahepatic cholangioenteric anastomosis in carcinoma of the hilus of the liver. Surg Gynecol Obstet 1975;140:170-8.
- Boilève A, Verlingue L, Hollebecque A, Boige V, Ducreux M, Malka D. Rare cancer, rare alteration: the case of NTRK fusions in biliary tract cancers. Expert Opin Investig Drugs 2021;30:401-9.
- Boudjema K, Sulpice L, Garnier S, Bretagne J-F, Gandon Y, Rohou T. A simple system to predict perihilar cholangiocarcinoma resectability. J Gastrointest Surg 2013;17:1247-56.
- Bridgewater J, Fletcher P, Palmer DH, et al. Long-term outcomes and exploratory analyses of the randomized Phase III BILCAP study. J Clin Oncol 2022;40:2048-57.
- Brieau B, Dahan L, De Rycke Y, et al. Second-line chemotherapy for advanced biliary tract cancer after failure of the gemcitabine-platinum combination: A large multicenter study by the Association des Gastro-Entérologues Oncologues. Cancer 2015;121:3290-7.
- Burke EC, Jarnagin WR, Hochwald SN, Pisters PW, Fong Y, Blumgart LH. Hilar Cholangiocarcinoma: patterns of spread, the importance of hepatic resection for curative operation, and a presurgical clinical staging system. Ann Surg 1998;228:385-94.
- Burnett AS, Calvert TJ, Chokshi RJ. Sensitivity of endoscopic retrograde cholangiopancreatography standard cytology: 10-y review of the literature. J Surg Res 2013;184:304-11.
- Cambridge WA, Fairfield C, Powell JJ, et al. Meta-analysis and meta-regression of survival after liver transplantation for unresectable perihilar cholangiocarcinoma. Ann Surg 2021;273:240-50.
- Castro FA, Koshiol J, Hsing AW, Devesa SS. Biliary tract cancer incidence in the United States-Demographic and temporal variations by anatomic site: Biliary tract cancer incidence in the US by anatomic site. Int J Cancer 2013;133:1664-71.
- Cereda S, Milella M, Cordio S, et al. Capecitabine with/without mitomycin C: results of a randomized phase II trial of second-line therapy in advanced biliary tract adenocarcinoma. Cancer Chemother Pharmacol 2016;77:109-14.
- Chascsa DM, Lindor KD. Cancer risk, screening and surveillance in primary sclerosing cholangitis. Minerva Gastroenterol Dietol 2019;65:214-28.
- Chen JS, Hsu C, Chiang NJ, et al. A KRAS mutation status-stratified randomized phase II trial of gemcitabine and oxaliplatin alone or in combination with cetuximab in advanced biliary tract cancer. Ann Oncol 2015;26:943-9.
- Choi IS, Kim KH, Lee JH, et al. A randomised phase II study of oxaliplatin/5-FU (mFOLFOX) versus irinotecan/5-FU (mFOLFIRI) chemotherapy in locally advanced or metastatic biliary tract cancer refractory to first-line gemcitabine/cisplatin chemotherapy. Eur J Cancer 2021;154:288-95.
- Clements O, Eliahoo J, Kim JU, Taylor-Robinson SD, Khan SA. Risk factors for intrahepatic and extrahepatic cholangiocarcinoma: A systematic review and meta-analysis. J Hepatol 2020;72:95-103.
- Coelen RJS, Roos E, Wiggers JK, et al. Endoscopic versus percutaneous biliary drainage in patients with resectable perihilar cholangiocarcinoma: a multicentre, randomised controlled trial. Lancet Gastroenterol Hepatol 2018;3:681-90.
- Conway AM, Morris GC, Smith S, et al. Intrahepatic cholangiocarcinoma hidden within cancer of unknown primary. Br J Cancer 2022;127:531-40.
- Csoma SL, Bedekovics J, Veres G, et al. Circulating cell-free DNA-based comprehensive molecular analysis of biliary tract cancers using next-generation sequencing. Cancers (Basel) 2022;14:233.
- Curcio G, Traina M, Mocciaro F. Intraductal aspiration: a promising new tissue-sampling technique for the diagnosis of suspected malignant biliary strictures. Gastrointest Endosc 2012;75:798-804.
- Darwish Murad S, Kim WR, et al. Efficacy of neoadjuvant chemoradiation, followed by liver transplantation, for perihilar cholangiocarcinoma at 12 US centers. Gastroenterology 2012;143:88-98.e3; quiz e14.
- de Aretxabala X, Roa I, Burgos L, et al. Gallbladder cancer in Chile. A report on 54 potentially resectable tumors. Cancer 1992;69:60-5.
- de Jong MC, Nathan H, Sotiropoulos GC, et al. Intrahepatic cholangiocarcinoma: an international multi-institutional analysis of prognostic factors and lymph node assessment. J Clin Oncol 2011;29:3140-5.
- De Michele S, Remotti HE, Del Portillo A, Lagana SM, Szabolcs M, Saqi A. SATB2 in neoplasms of lung, pancreatobiliary, and gastrointestinal origins. Am J Clin Pathol 2021;155:124-32.
- Defossez G, Le Guyader‑Peyrou S, Uhry Z, et al. Estimations nationales de l’incidence et de la mortalité par cancer en France métropolitaine entre 1990 et 2018. Synthèse. Saint‑Maurice : Santé publique France, 2019. http://www.santepubliquefrance.fr
- Deoliveira ML, Schulick RD, Nimura Y, et al. New staging system and a registry for perihilar cholangiocarcinoma. Hepatology 2011;53:1363-71.
- Dickson PV, Behrman SW. Distal cholangiocarcinoma. Surg Clin North Am 2014;94:325-42.
- Dixon E, Vollmer CM, Sahajpal A, et al. An aggressive surgical approach leads to improved survival in patients with gallbladder cancer: a 12-year study at a North American Center. Ann Surg 2005;241:385-94.
- Doebele RC, Drilon A, Paz-Ares L, et al. Entrectinib in patients with advanced or metastatic NTRK fusion-positive solid tumours: integrated analysis of three phase 1-2 trials. Lancet Oncol 2020;21:271-282. Errata in: Lancet Oncol 2020;21:e70, Lancet Oncol 2020;21:e341, Lancet Oncol 2020;21:e372, Lancet Oncol 2021;22:e428.
- Dokmak S, Ftériche FS, Borscheid R, Cauchy F, Farges O, Belghiti J. 2012 Liver resections in the 21st century: we are far from zero mortality. HPB (Oxford) 2013;15:908-15.
- Drilon A, Laetsch TW, Kummar S, et al. Efficacy of larotrectinib in TRK fusion-positive cancers in adults and children. N Engl J Med 2018;378:731-9.
- Dumonceau J-M, Tringali A, Papanikolaou IS, et al. Endoscopic biliary stenting: indications, choice of stents, and results: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline - Updated October 2017. Endoscopy 2018;50:910-30.
- Ebata T, Hirano S, Konishi M, et al. Randomized clinical trial of adjuvant gemcitabine chemotherapy versus observation in resected bile duct cancer. Br J Surg 2018;105:192-202.
- Eckel F, Schmid RM. Chemotherapy and targeted therapy in advanced biliary tract carcinoma: a pooled analysis of clinical trials. Chemotherapy 2014;60:13-23.
- Eckel F, Schmid RM. Chemotherapy in advanced biliary tract carcinoma: a pooled analysis of clinical trials. Br J Cancer 2007;96:896-902.
- Edeline J, Benabdelghani M, Bertaut A, et al. Gemcitabine and oxaliplatin chemotherapy or surveillance in resected biliary tract cancer (PRODIGE 12-ACCORD 18-UNICANCER GI): A randomized Phase III study. J Clin Oncol 2019;37:658-67.
- Edeline J, Hirano S, Bertaut A, et al. Individual patient data meta-analysis of adjuvant gemcitabine-based chemotherapy for biliary tract cancer: combined analysis of the BCAT and PRODIGE-12 studies. Eur J Cancer 2022;164:80-87.
- Edeline J, Lamarca A, McNamara MG, et al. Locoregional therapies in patients with intrahepatic cholangiocarcinoma: A systematic review and pooled analysis. Cancer Treat Rev 2021;99:102258.
- Endo I, Gonen M, Yopp AC, et al. Intrahepatic cholangiocarcinoma: rising frequency, improved survival, and determinants of outcome after resection. Ann Surg 2008;248:84-96.
- Endo I, Shimada H, Tanabe M, et al. Prognostic significance of the number of positive lymph nodes in gallbladder cancer. J Gastrointest Surg 2006;10:999-1007.
- Erdogan D, Kloek JJ, ten Kate FJW, et al. Immunoglobulin G4-related sclerosing cholangitis in patients resected for presumed malignant bile duct strictures. Br J Surg 2008;95:727-34.
- Farges O, Fuks D, Boleslawski E, et al. Influence of surgical margins on outcome in patients with intrahepatic cholangiocarcinoma: a multicenter study by the AFC-IHCC-2009 study group. Ann Surg 2011;254:824-9; discussion 830.
- Farshidfar F, Zheng S, Gingras MC, et al. Integrative genomic analysis of cholangiocarcinoma identifies distinct IDH-mutant molecular profiles. Cell Rep 2017;18:2780-94.
- Fiteni F, Nguyen T, Vernerey D, et al. Cisplatin/gemcitabine or oxaliplatin/gemcitabine in the treatment of advanced biliary tract cancer: a systematic review. Cancer Med 2014;3:1502-11.
- Florio AA, Ferlay J, Znaor A, et al. Global trends in intrahepatic and extrahepatic cholangiocarcinoma incidence from 1993 to 2012. Cancer 2020;126:2666e78.
- Fornaro L, Vivaldi C, Cereda S, et al. Second-line chemotherapy in advanced biliary cancer progressed to first-line platinum-gemcitabine combination: a multicenter survey and pooled analysis with published data. J Exp Clin Cancer Res 2015;34:156.
- Fuks D, Regimbeau JM, Le Treut YP, et al. Incidental gallbladder cancer by the AFC-GBC-2009 Study Group. World J Surg 2011;35:1887-97.
- Gao DJ, Yang JF, Ma SR, et al. Endoscopic radiofrequency ablation plus plastic stent placement versus stent placement alone for unresectable extrahepatic biliary cancer: a multicenter randomized controlled trial. Gastrointest Endosc. 2021;94:91-100.
- Gerges C, Beyna T, Tang RSY, et al. Digital single-operator peroral cholangioscopy-guided biopsy sampling versus ERCP-guided brushing for indeterminate biliary strictures: a prospective, randomized, multicenter trial (with video). Gastrointest Endosc 2020;91:1105-13.
- Glimelius B, Hoffman K, Sjödén PO, et al. Chemotherapy improves survival and quality of life in advanced pancreatic and biliary cancer. Ann Oncol 1996;7:593-600.
- GLOBOCAN. Cancer incidence in 5 continents. Volume XI. International Agency for Research on Cancer, 2017.
- Goetze TO, Paolucci V. Benefits of reoperation of T2 and more advanced incidental gallbladder carcinoma: analysis of the German registry. Ann Surg 2008;247:104-8.
- Goetze TO, Paolucci V. Use of retrieval bags in incidental gallbladder cancer cases. World J Surg 2009;33:2161-5.
- Goyal L, Saha SK, Liu LY, et al. Polyclonal secondary FGFR2 mutations drive acquired resistance to FGFR inhibition in patients with FGFR2 fusion-positive cholangiocarcinoma. Cancer Discov 2017;7:252-63.
- Goyal L, Meric-Bernstam F, Hollebecque A, Valle JW, Morizane C, Karasic TB. Futibatinib for FGFR2-rearranged intrahepatic cholangiocarcinoma. N Engl J Med 2023;388:228-39.
- Grandadam S, Compagnon P, Arnaud A, et al. Role of preoperative optimization of the liver for resection in patients with hilar cholangiocarcinoma type III. Ann Surg Oncol 2010;17:3155-61.
- Hainsworth JD, Rubin MS, Spigel DR, et al. Molecular gene expression profiling to predict the tissue of origin and direct site-specific therapy in patients with carcinoma of unknown primary site: a prospective trial of the Sarah Cannon research institute. J Clin Oncol 2013;31:217-23.
- HAS. Avis n°2018.0053/AC/SEAP du 28 novembre 2018 du collège de la HAS relatif à l’inscription sur la LAP mentionnée à l’article L. 162-1-7 du CSS de méthodes de recherche d’un déficit en dihydropyrimidine deshydrogénase [Internet]. Haute Autorité de Santé 2018 [cited 2019 Oct 15]. Available from: https://www.has-sante.fr/jcms/c_2891062/fr/avis-n2018-0053/ac/seap-du-28-novembre-2018-du-college-de-la-has-relatif-a-l-inscription-sur-la-lap-mentionnee-a-l-article-l-162-1-7-du-css-de-methodes-de-recherche-d-un-deficit-en-dihydropyrimidine-deshydrogenase
- Hemminki K, Li X. Familial liver and gall bladder cancer: a nationwide epidemiological study from Sweden. Gut 2003;52:592-6.
- Hong W, Sun X, Zhu Q. Endoscopic stenting for malignant hilar biliary obstruction: should it be metal or plastic and unilateral or bilateral? Eur J Gastroenterol Hepatol 2013;25:1105-12.
- Hong DS, Fakih MG, Strickler JH, et al. KRASG12C inhibition with sotorasib in advanced solid tumors. N Engl J Med 2020 ;383:1207-17.
- Horgan AM, Amir E, Walter T, Knox JJ. Adjuvant therapy in the treatment of biliary tract cancer: a systematic review and meta-analysis. J Clin Oncol 2012;30:1934-40.
- Hsing AW, Bai Y, Andreotti G, et al. Family history of gallstones and the risk of biliary tract cancer and gallstones: a population-based study in Shanghai, China. Int J Cancer 2007;121:832-8.
- Hu JH, Tang JH, Lin CH, Chu YY, Liu NJ. Preoperative staging of cholangiocarcinoma and biliary carcinoma using 18F-fluorodeoxyglucose positron emission tomography: a meta-analysis. J Investig Med 2018;66:52-61.
- Huang X, Yang J, Li J, Xiong Y. Comparison of magnetic resonance imaging and 18-fludeoxyglucose positron emission tomography/computed tomography in the diagnostic accuracy of staging in patients with cholangiocarcinoma. Medicine 2020;99:e20932.
- Hyung J, Kim B, Yoo C, et al. Clinical benefit of maintenance therapy for advanced biliary tract cancer patients showing no progression after first-line gemcitabine plus cisplatin. Cancer Res Treat 2019;51:901-9.
- Hyung J, Kim I, Kim KP, et al. Treatment with liposomal irinotecan plus fluorouracil and leucovorin for patients with previously treated metastatic biliary tract cancer: The Phase 2b NIFTY randomized clinical trial. JAMA Oncol 2023;9:692-9.
- Ikeda M, Nakachi K, Konishi M, et al. Adjuvant S-1 versus observation in curatively resected biliary tract cancer: A phase III trial (JCOG1202: ASCOT). J Clin Oncol 2022;40(4_suppl):382-382.
- Jain A, Javle M. Molecular profiling of biliary tract cancer: a target rich disease. J Gastrointest Oncol 2016;7:797-803.
- Jarnagin WR, Fong Y, DeMatteo RP, et al. Staging, resectability, and outcome in 225 patients with hilar cholangiocarcinoma. Ann Surg 2001;234:507-17; discussion 517-9.
- Javle M, Borad MJ, Azad NS, et al. Pertuzumab and trastuzumab for HER2-positive, metastatic biliary tract cancer (MyPathway): a multicentre, open-label, phase 2a, multiple basket study. Lancet Oncol 2021a ;22:1290-300.
- Javle M, Roychowdhury S, Kelley RK, et al. Infigratinib (BGJ398) in previously treated patients with advanced or metastatic cholangiocarcinoma with FGFR2 fusions or rearrangements: mature results from a multicentre, open-label, single-arm, phase 2 study. Lancet Gastroenterol Hepatol 2021b ;6:803-15.
- Joo I, Lee JM, Yoon JH. Imaging diagnosis of intrahepatic and perihilar cholangiocarcinoma: recent advances and challenges. Radiology 2018;288:7-13.
- Juntermanns B, Kaiser GM, Reis H, et al. Klatskin-mimicking lesions: still a diagnostical and therapeutical dilemma? Hepatogastroenterology 2011;58:265-9.
- Jusakul A, Cutcutache I, Yong CH, et al. Whole-genome and epigenomic landscapes of etiologically distinct subtypes of cholangiocarcinoma. Cancer Discov 2017;7:1116-35.
- Kamisawa T, Kaneko K, Itoi T, Ando H. Pancreaticobiliary maljunction and congenital biliary dilatation. Lancet Gastroenterol Hepatol 2017;2:610-8.
- Kang H, Chung MJ, Cho IR, et al. Efficacy and safety of palliative endobiliary radiofrequency ablation using a novel temperature-controlled catheter for malignant biliary stricture: a single-center prospective randomized phase II TRIAL. Surg Endosc 2021;35:63-73.
- Kang MJ, Lee JL, Kim TW, et al. Randomized phase II trial of S-1 and cisplatin versus gemcitabine and cisplatin in patients with advanced biliary tract adenocarcinoma. Acta Oncol 2012;51:860-6.
- Kawashima H, Itoh A, Ohno E, Goto H, Hirooka Y. Transpapillary biliary forceps biopsy to distinguish benign biliary stricture from malignancy: how many tissue samples should be obtained? Dig Endosc 2012;24 Suppl 1:22-7.
- Kelley RK, Ueno M, Yoo C, et al. Pembrolizumab in combination with gemcitabine and cisplatin compared with gemcitabine and cisplatin alone for patients with advanced biliary tract cancer (KEYNOTE-966): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2023;401:1853-65.
- Kilander C, Lagergren J, Ljung R, Sadr-Azodi O. The population based incidence and mortality of biliary tract cancer in Sweden. Cancer Epidemiol 2018;56:14-20.
- Kim BJ, Yoo C, Kim KP, et al. Efficacy of fluoropyrimidine-based chemotherapy in patients with advanced biliary tract cancer after failure of gemcitabine plus cisplatin: retrospective analysis of 321 patients. Br J Cancer 2017;116:561-7.
- Kim ST, Kang JH, Lee J, et al. Capecitabine plus oxaliplatin versus gemcitabine plus oxaliplatin as first-line therapy for advanced biliary tract cancers: a multicenter, open-label, randomized, phase III, noninferiority trial. Ann Oncol 2019;30:788-95.
- Kitagawa Y, Nagino M, Kamiya J, et al. Lymph node metastasis from hilar cholangiocarcinoma: audit of 110 patients who underwent regional and paraaortic node dissection. Ann Surg 2001;233:385-92.
- Kluge R, Schmidt F, Caca K, et al. Positron emission tomography with [(18)F]fluoro-2-deoxy-D-glucose for diagnosis and staging of bile duct cancer. Hepatology 2001;33:1029-35.
- Kobayashi M, Ryozawa S, Araki R, et al. Investigation of factors affecting the sensitivity of bile duct brush cytology. Intern Med Tokyo Jpn 2019;58:329-35.
- Kondo S, Nimura Y, Hayakawa N, Kamiya J, Nagino M, Uesaka K. Regional and para-aortic lymphadenectomy in radical surgery for advanced gallbladder carcinoma. Br J Surg 2000;87:418-22.
- Koshiol J, Wozniak A, Cook P, et al. Salmonella enterica serovar Typhi and gallbladder cancer: a case-control study and metaanalysis. Cancer Med 2016;5:3310-35.
- Lamarca A, Hubner RA, David Ryder W, Valle JW. Second-line chemotherapy in advanced biliary cancer: a systematic review. Ann Oncol 2014;25:2328-38.
- Lamarca A, Barriuso J, Chander A, et al. 18F-fluorodeoxyglucose positron emission tomography (18FDG-PET) for patients with biliary tract cancer: systematic review and meta-analysis. J Hepatol 2019;71:115-29.
- Lamarca A, Palmer DH, Wasan HS, et al. Second-line FOLFOX chemotherapy versus active symptom control for advanced biliary tract cancer (ABC-06): a phase 3, open-label, randomised, controlled trial. Lancet Oncol 2021;22:690-701.
- Laquière A, Boustière C, Leblanc S, Penaranda G, Désilets E, Prat F. Safety and feasibility of endoscopic biliary radiofrequency ablation treatment of extrahepatic cholangiocarcinoma. Surg Endosc 2016 ;30:1242-8.
- Lapin M, Huang HJ, Chagani S, et al. Monitoring of dynamic changes and clonal evolution in circulating tumor DNA from patients with IDH-mutated cholangiocarcinoma treated with isocitrate dehydrogenase inhibitors. JCO Precis Oncol 2022;6:e2100197.
- Lee H, Choi DW, Park JY, et al. Surgical strategy for T2 gallbladder cancer according to tumor location. Ann Surg Oncol 2015;22:2779-86.
- Lee JH, Salem R, Aslanian H, Chacho M, Topazian M. Endoscopic ultrasound and fine-needle aspiration of unexplained bile duct strictures. Am J Gastroenterol 2004;99:1069-73.
- Lee SE, Jang JY, Kim SW, et al. Surgical strategy for T1 gallbladder cancer: a nationwide multicenter survey in South Korea. Ann Surg Oncol 2014;21:3654-60.
- Lee CK, Chon HJ, Cheon J, et al. Trastuzumab plus FOLFOX for HER2-positive biliary tract cancer refractory to gemcitabine and cisplatin: a multi-institutional phase 2 trial of the Korean Cancer Study Group (KCSG-HB19-14). Lancet Gastroenterol Hepatol 2023 ;8:56-65.
- Lepage C, Cottet V, Chauvenet M, et al. Trends in the incidence and management of biliary tract cancer: a French population-based study. J Hepatol 2011;54:306-10.
- Levy C, Lymp J, Angulo P, Gores GJ, Larusso N, Lindor KD. The value of serum CA 19-9 in predicting cholangiocarcinomas in patients with primary sclerosing cholangitis. Dig Dis Sci 2005;50:1734-40.
- Lewis JT, Talwalkar JA, Rosen CB, Smyrk TC, Abraham SC. Prevalence and risk factors for gallbladder neoplasia in patients with primary sclerosing cholangitis: evidence for a metaplasiadysplasia-carcinoma sequence. Am J Surg Pathol 2007;31:907-13.
- Li H, Zhang ZY, Zhou ZQ, Guan J, Tong DN, Zhou GW. Combined gemcitabine and S-1 chemotherapy for treating unresectable hilar cholangiocarcinoma: a randomized open-label clinical trial. Oncotarget 2016;7:26888-97.
- Li ZM, Wu ZX, Han B, et al. The association between BMI and gallbladder cancer risk: a meta-analysis. Oncotarget 2016;7:43669-79.
- Lopera JE, Soto JA, Múnera F. Malignant hilar and perihilar biliary obstruction: use of MR cholangiography to define the extent of biliary ductal involvement and plan percutaneous interventions. Radiology 2001;220:90-6.
- Maio M, Ascierto PA, Manzyuk L, et al. Pembrolizumab in microsatellite instability high or mismatch repair deficient cancers: updated analysis from the phase II KEYNOTE-158 study. Ann Oncol 2022;33:929-38.
- Maker AV, Butte JM, Oxenberg J, et al. Is port site resection necessary in the surgical management of gallbladder cancer? Ann Surg Oncol 2012;19:409-17.
- Malka D, Cervera P, Foulon S, et al. Gemcitabine and oxaliplatin with or without cetuximab in advanced biliary-tract cancer (BINGO): a randomised, open-label, non-comparative phase 2 trial. Lancet Oncol 2014;15:819-28.
- Marchiò C, Scaltriti M, Ladanyi M, et al. ESMO recommendations on the standard methods to detect NTRK fusions in daily practice and clinical research. Ann Oncol 2019;30:1417-27.
- Martin RC, Rocha F, Simo K, Crocenzi T, Scoggins CR. Drug-eluting bead, irinotecan (DEBIRI) therapy of unresectable intrahepatic cholangiocarcinoma (ICC) with concomitant systemic gemcitabine and cisplatin (Gem-Cis). Ann Surg Oncol 2020;20(suppl1):S21.
- Mateo J, Chakravarty D, Dienstmann R, et al. A framework to rank genomic alterations as targets for cancer precision medicine: the ESMO Scale for Clinical Actionability of molecular Targets (ESCAT). Ann Oncol 2018;29:1895-902.
- Mazzaferro V, El-Rayes BF, Droz Dit Busset M, et al. Derazantinib (ARQ 087) in advanced or inoperable FGFR2 gene fusion-positive intrahepatic cholangiocarcinoma. Br J Cancer 2019;120:165-71.
- Mehmood S, Loya A, Yusuf MA. Biliary brush cytology revisited. Acta Cytol 2016;60:167-72.
- Meric-Bernstam F, Beeram M, Hamilton E, et al. Zanidatamab, a novel bispecific antibody, for the treatment of locally advanced or metastatic HER2-expressing or HER2-amplified cancers: a phase 1, dose-escalation and expansion study. Lancet Oncol 2022;23:1558-70.
- Moehler M, Maderer A, Schimanski C, et al. Gemcitabine plus sorafenib versus gemcitabine alone in advanced biliary tract cancer: a double-blind placebo-controlled multicentre phase II AIO study with biomarker and serum programme. Eur J Cancer 2014;50:3125-35.
- Morizane C, Okusaka T, Mizusawa J, et al. Combination gemcitabine plus S-1 versus gemcitabine plus cisplatin for advanced/recurrent biliary tract cancer: the FUGA-BT (JCOG1113) randomized phase III clinical trial. Ann Oncol 2019;30:1950-8.
- Morizane C, Okusaka T, Mizusawa J, et al. Randomized phase II study of gemcitabine plus S-1 versus S-1 in advanced biliary tract cancer: a Japan Clinical Oncology Group trial (JCOG 0805). Cancer Sci 2013;104:1211-6.
- Moryoussef F, Sportes A, Leblanc S, Bachet JB, Chaussade S, Prat F. Is EUS-guided drainage a suitable alternative technique in case of proximal biliary obstruction? Therap Adv Gastroenterol 2017;10:537-44.
- Mosele F, Remon J, Mateo J, et al. Recommendations for the use of next-generation sequencing (NGS) for patients with metastatic cancers: a report from the ESMO Precision Medicine Working Group. Ann Oncol 2020;31:1491-505.
- Nagino M, Nimura Y, Nishio H, et al. Hepatectomy with simultaneous resection of the portal vein and hepatic artery for advanced perihilar cholangiocarcinoma: an audit of 50 consecutive cases. Ann Surg 2010;252:115-23.
- Nakachi K, Ikeda M, Konishi M, et al. Adjuvant S-1 compared with observation in resected biliary tract cancer (JCOG1202, ASCOT): a multicentre, open-label, randomised, controlled, phase 3 trial. Lancet. 2023;401:195-203.
- Nakamura H, Arai Y, Totoki Y, et al. Genomic spectra of biliary tract cancer. Nat Genet 2015;47:1003-10.
- Nakamura Y, Mizuno N, Sunakawa Y, et al. Tucatinib and trastuzumab for previously treated human epidermal growth factor receptor 2-positive metastatic biliary tract cancer (SGNTUC-019): A Phase II basket study. J Clin Oncol 2023:JCO2300606. doi: 10.1200/JCO.23.00606.
- Navaneethan U, Hasan MK, Lourdusamy V, Njei B, Varadarajulu S, Hawes RH. Single-operator cholangioscopy and targeted biopsies in the diagnosis of indeterminate biliary strictures: a systematic review. Gastrointest Endosc 2015;82:608-14.
- Navaneethan U, Njei B, Lourdusamy V, et al. Comparative effectiveness of biliary brush cytology and intraductal biopsy for detection of malignant biliary strictures: a systematic review and meta-analysis. Gastro-intest Endosc 2015b;81:168-76.
- Neoptolemos JP, Stocken DD, Friess H, et al. A randomized trial of chemoradiotherapy and chemotherapy after resection of pancreatic cancer. N Engl J Med 2004;350:1200-10.
- Nepal C, O'Rourke CJ, Oliveira DVNP, et al. Genomic perturbations reveal distinct regulatory networks in intrahepatic cholangiocarcinoma. Hepatology 2018;68:949-63.
- Neuhaus P, Jonas S, Bechstein WO, et al. Extended resections for hilar cholangiocarcinoma. Ann Surg 1999;230:808-18; discussion 819.
- Neuzillet C, Casadei Gardini A, Brieau B, et al. Prediction of survival with second-line therapy in biliary tract cancer: Actualisation of the AGEO CT2BIL cohort and European multicentre validations. Eur J Cancer 2019;111:94-106.
- Neuzillet C, Emery C, Teissier C, Bouée S, Lièvre A. Patient healthcare trajectories of intrahepatic cholangiocarcinoma in France: A nationwide retrospective analysis. Lancet Reg Health Eur 2022;15:100324.
- Nogova L, Sequist LV, Perez Garcia JM, et al. Evaluation of BGJ398, a Fibroblast Growth Factor Receptor 1-3 kinase inhibitor, in patients with advanced solid tumors harboring genetic alterations in fibroblast growth factor receptors: results of a global phase I, dose-escalation and dose-expansion study. J Clin Oncol 2017;35:157-65.
- Ogura Y, Mizumoto R, Isaji S, Kusuda T, Matsuda S, Tabata M. Radical operations for carcinoma of the gallbladder: Present status in Japan. World J Surg 1991;15:337-43.
- Oh DY, He AR, Qin S, et al. Durvalumab plus gemcitabine and cisplatin in advanced biliary tract cancer. NEJM Evidence 2022a;10.1056/EVIDoa2200015.
- Oh DY, He AR, Qin S, et al. Updated overall survival (OS) from the phase III TOPAZ-1 study of durvalumab (D) or placebo (PBO) plus gemcitabine and cisplatin (+ GC) in patients (pts) with advanced biliary tract cancer (BTC). Ann Oncol 2022b;33 (suppl_7):S19-S26.
- Ohba A, Morizane C, Kawamoto Y, et al. Trastuzumab deruxtecan (T-DXd; DS-8201) in patients (pts) with HER2-expressing unresectable or recurrent biliary tract cancer (BTC): An investigator-initiated multicenter phase 2 study (HERB trial). J Clin Oncol 2022;40(16_suppl):4006-4006.
- Okusaka T, Nakachi K, Fukutomi A, et al. Gemcitabine alone or in combination with cisplatin in patients with biliary tract cancer: a comparative multicentre study in Japan. Br J Cancer 2010;103:469-74.
- Okusaka T, Nakachi K, Fukutomi A, et al. Gemcitabine alone or in combination with cisplatin in patients with biliary tract cancer: a comparative multicentre study in Japan. Br J Cancer 2010;103:469-74.
- Palmer WC, Patel T. Are common factors involved in the pathogenesis of primary liver cancers? A meta-analysis of risk factors for intrahepatic cholangiocarcinoma. J Hepatol 2012;57:69-76.
- Papadopoulos KP, El-Rayes BF, Tolcher AW, et al. A Phase 1 study of ARQ 087, an oral pan-FGFR inhibitor in patients with advanced solid tumours. Br J Cancer 2017;117:1592-9.
- Park HS, Lee JM, Choi JY, et al. Preoperative evaluation of bile duct cancer: MRI combined with MR cholangiopancreatography versus MDCT with direct cholangiography. AJR Am J Roentgenol2008;190:396-405.
- Patel T. Increasing incidence and mortality of primary intrahepatic cholangiocarcinoma in the United States. Hepatology 2001;33:1353-7.
- Perkhofer L, Striefler JK, Sinn M, Opitz B, Goetze TO, Gallmeier E. Nal-IRI with 5-fluorouracil (5-FU) and leucovorin or gemcitabine plus cisplatin in advanced biliary tract cancer: Final results of the NIFE-trial (AIO-YMO HEP-0315), a randomized phase II study of the AIO biliary tract cancer group. Ann Oncol 2021;32 (suppl_5):S1282.
- Phelip JM, Desrame J, Edeline J, et al. Modified FOLFIRINOX versus CISGEM chemotherapy for patients with advanced biliary tract cancer (PRODIGE 38 AMEBICA): A randomized Phase II study. J Clin Oncol 2022;40:262-71.
- Phelip JM, Vendrely V, Rostain F, et al. Gemcitabine plus cisplatin versus chemoradiotherapy in locally advanced biliary tract cancer: Fédération Francophone de Cancérologie Digestive 9902 phase II randomised study. Eur J Cancer 2014;50:2975-82.
- Prat F, Leblanc S, Foissac F, et al. Impact of peroral cholangioscopy on the management of indeterminate biliary conditions: a multicentre prospective trial. Frontline Gastroenterol 2019;10:236-43.
- Primrose JN, Fox RP, Palmer DH, et al. Capecitabine compared with observation in resected biliary tract cancer (BILCAP): a randomised, controlled, multicentre, phase 3 study. Lancet Oncol 2019;20:663-73.
- Ramage JK, Donaghy A, Farrant JM, Iorns R, Williams R. Serum tumor markers for the diagnosis of cholangiocarcinoma in primary sclerosing cholangitis. Gastroenterology 1995;108:865-9.
- Ramaswamy A, Ostwal V, Sharma A, et al. Efficacy of capecitabine plus irinotecan vs irinotecan monotherapy as second-line treatment in patients with advanced gallbladder cancer: A multicenter Phase 2 randomized clinical trial (GB-SELECT). JAMA Oncol 2021;7:436-9.
- Rizvi S, Gores GJ. Pathogenesis, diagnosis, and management of cholangiocarcinoma. Gastroenterology 2013;145:1215-29.
- Romagnuolo J, Bardou M, Rahme E, Joseph L, Reinhold C, Barkun AN. Magnetic resonance cholangiopancreatography: a meta-analysis of test performance in suspected biliary disease. Ann Intern Med 2003;139:547-57.
- Roth GS, Bichard P, Fior-Gozlan M, et al. Performance of bile aspiration plus brushing to diagnose malignant biliary strictures during endoscopic retrograde cholangiopancreatography. Endosc Int Open 2016;4:E997-E1003.
- Rumgay H, Ferlay J, de Martel C, et al. Global, regional and national burden of primary liver cancer by subtype. Eur J Cancer 2022;161:108-18.
- Ruys AT, van Beem BE, Engelbrecht MRW, Bipat S, Stoker J, Van Gulik TM. Radiological staging in patients with hilar cholangiocarcinoma: a systematic review and meta-analysis. Br J Radiol 2012;85:1255-62.
- Saha SK, Zhu AX, Fuchs CS, Brooks GA. Forty-year trends in cholangiocarcinoma incidence in the US: intrahepatic disease on the rise. Oncologist 2016;21:594-9.
- Sahai V, Catalano PJ, Zalupski MM, et al. Nab-Paclitaxel and gemcitabine as first-line treatment of advanced or metastatic cholangiocarcinoma: A Phase 2 clinical trial. JAMA Oncol 2018;4:1707-12.
- Said K, Glaumann H, Bergquist A. Gallbladder disease in patients with primary sclerosing cholangitis. J Hepatol 2008;48:598-605.
- Sakai D, Kanai M, Kobayashi S, et al. Randomized phase III study of gemcitabine, cisplatin plus S-1 (GCS) versus gemcitabine, cisplatin (GC) for advanced biliary tract cancer (KHBO1401-MITSUBA). Ann Oncol 2018;29(Supp 8):viii205-viii270.
- Saleh M, Virarkar M, Bura V, et al. Intrahepatic cholangiocarcinoma: pathogenesis, current staging, and radiological findings. Abdom Radiol 2020;45:3662-80.
- Salem ME, El-Refai SM, Sha W, et al. Characterization of KRAS mutation variants and prevalence of KRAS-G12C in gastrointestinal malignancies. ESMO Gastrointestinal Congress 2021;0-3.
- Sangchan A, Kongkasame W, Pugkhem A, Jenwitheesuk K, Mairiang P. Efficacy of metal and plastic stents in unresectable complex hilar cholangiocarcinoma: a randomized controlled trial. Gastrointest Endosc 2012;76:93-9.
- Santoro A, Gebbia V, Pressiani T, et al. A randomized, multicenter, phase II study of vandetanib monotherapy versus vandetanib in combination with gemcitabine versus gemcitabine plus placebo in subjects with advanced biliary tract cancer: the VanGogh study. Ann Oncol 2015 ;26:542-7.
- Sapisochin G, Facciuto M, Rubbia-Brandt L, et al. Liver transplantation for “very early” intrahepatic cholangiocarcinoma: International retrospective study supporting a prospective assessment. Hepatology 2016;64:1178-88.
- Sasaki T, Isayama H, Nakai Y, et al. A randomized phase II study of gemcitabine and S-1 combination therapy versus gemcitabine monotherapy for advanced biliary tract cancer. Cancer Chemother Pharmacol 2013 ;71:973-9.
- Schinzari G, Rossi E, Mambella G, et al. First-line treatment of advanced biliary ducts carcinoma: A randomized Phase II study evaluating 5-FU/LV plus oxaliplatin (Folfox 4) versus 5-FU/LV (de Gramont regimen). Anticancer Res 2017;37:5193-7.
- Senthil Kumar MP, Marudanayagam R. Klatskin-like lesions. HPB Surg 2012;2012:107519.
- Shaib YH, Davila JA, McGlynn K, El-Serag HB. Rising incidence of intrahepatic cholangiocarcinoma in the United States: a true increase? J Hepatol 2004;40:472-7.
- Sharaiha RZ, Khan MA, Kamal F, et al. Efficacy and safety of EUS-guided biliary drainage in comparison with percutaneous biliary drainage when ERCP fails: a systematic review and meta-analysis. Gastrointest Endosc 2017;85:904-14.
- Sharma A, Dwary AD, Mohanti BK, et al. Best supportive care compared with chemotherapy for unresectable gall bladder cancer: a randomized controlled study. J Clin Oncol 2010;28:4581-6.
- Sharma A, Kalyan Mohanti B, Pal Chaudhary S, et al. Modified gemcitabine and oxaliplatin or gemcitabine + cisplatin in unresectable gallbladder cancer: Results of a phase III randomised controlled trial. Eur J Cancer 2019;123:162-70.
- Sharma M, Talwar V, Maheshwari U, et al. Role of maintenance gemcitabine in advanced carcinoma gallbladder. South Asian J Cancer 2021;9:204-8.
- Shimizu Y, Ohtsuka M, Ito H, et al. Should the extrahepatic bile duct be resected for locally advanced gallbladder cancer? Surgery 2004;136:1012-7; discussion 1018.
- Shindoh J, de Aretxabala X, Aloia TA, et al. Tumor location is a strong predictor of tumor progression and survival in T2 gallbladder cancer: an international multicenter study. Ann Surg 2015;261:733-9.
- Shirai Y, Yoshida K, Tsukada K, Muto T. Inapparent carcinoma of the gallbladder. An appraisal of a radical second operation after simple cholecystectomy. Ann Surg 1992;215:326-31.
- Shroff RT, Javle MM, Xiao L, et al. Gemcitabine, cisplatin, and nab-paclitaxel for the treatment of advanced biliary tract cancers: A Phase 2 clinical trial. JAMA Oncol 2019;5:824-30.
- Shroff RT, Guthrie KA, Scott AJ, et al. SWOG 1815: A phase III randomized trial of gemcitabine, cisplatin, and nab-paclitaxel versus gemcitabine and cisplatin in newly diagnosed, advanced biliary tract cancers. J Clin Oncol 2023;41(4_suppl):LBA490.
- Sikora SS, Singh RK. Surgical strategies in patients with gallbladder cancer: nihilism to optimism. J Surg Oncol 2006;93:670-81.
- Sithithaworn P, Yongvanit P, Duenngai K, Kiatsopit N, Pairojkul C. Roles of liver fluke infection as risk factor for cholangiocarcinoma. J Hepatobiliary Pancreat Sci 2014;21:301-8.
- Spolverato G, Yakoob MY, Kim Y, et al. The impact of surgical margin status on long-term outcome after resection for intrahepatic cholangiocarcinoma. Ann Surg Oncol 2015;22:4020-8.
- Subbiah V, Lassen U, Élez E, et al. Dabrafenib plus trametinib in patients with BRAFV600E-mutated biliary tract cancer (ROAR): a phase 2, open-label, single-arm, multicentre basket trial. Lancet Oncol 2020;21:1234-43.
- Suzuki S, Yokoi Y, Kurachi K, et al. Appraisal of surgical treatment for pT2 gallbladder carcinomas. World J Surg 2004;28:160-5.
- Téllez-Ávila FI, Bernal-Méndez AR, Guerrero-Vázquez CG, Martínez-Lozano JA, Ramírez-Luna MÁ. Diagnostic yield of EUS-guided tissue acquisition as a first-line approach in patients with suspected hilar cholangiocarcinoma. Am J Gastroenterol 2014;109:1294-6.
- Tian YH, Ji X, Liu B, et al. Surgical treatment of incidental gallbladder cancer discovered during or following laparoscopic cholecystectomy. World J Surg 2015;39:746-52.
- Toyonaga T, Chijiiwa K, Nakano K, et al. Completion radical surgery after cholecystectomy for accidentally undiagnosed gallbladder carcinoma. World J Surg 2003;27:266-71.
- Tyberg A, Raijman I, Siddiqui A, et al. Digital pancreaticocholangioscopy for mapping of pancreaticobiliary neoplasia: can we alter the surgical resection margin? J Clin Gastroenterol 2019 ;53:71-5.
- Valle J, Wasan H, Palmer DH, et al. Cisplatin plus gemcitabine versus gemcitabine for biliary tract cancer. N Engl J Med 2010;362:1273-81.
- Valle JW, Furuse J, Jitlal M, et al. Cisplatin and gemcitabine for advanced biliary tract cancer: a meta-analysis of two randomised trials. Ann Oncol 2014;25:391-8.
- Valle JW, Wasan H, Lopes A, et al. Cediranib or placebo in combination with cisplatin and gemcitabine chemotherapy for patients with advanced biliary tract cancer (ABC-03): a randomised phase 2 trial. Lancet Oncol 2015;16:967-78.
- Valle JW, Borbath I, Khan SA, Huguet F, Gruenberger T, Arnold D. Biliary cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2016;27(suppl_5):v28-37.
- Valle JW, Qin S, Antonuzzo L, et al. Impact of mutation status on efficacy outcomes in TOPAZ-1: A phase III study of durvalumab (D) or placebo (PBO) plus gemcitabine and cisplatin (+GC) in advanced biliary tract cancer (BTC). Ann Oncol 2022;33 (suppl_9):S1454-S1484.
- van de Haar J, Hoes LR, Roepman P, et al. Limited evolution of the actionable metastatic cancer genome under therapeutic pressure. Nat Med 2021;27:1553-63.
- Varghese AM, Patel J, Janjigian YY, et al. Noninvasive detection of polyclonal acquired resistance to FGFR inhibition in patients with cholangiocarcinoma harboring FGFR2 alterations. JCO Precis Oncol 2021;5:PO.20.00178.
- Verlingue L, Malka D, Allorant A, et al. Precision medicine for patients with advanced biliary tract cancers: An effective strategy within the prospective MOSCATO-01 trial. Eur J Cancer 2017;87:122-30. Erratum in: Eur J Cancer 2018 14.
- Vienne A, Hobeika E, Gouya H, et al. Prediction of drainage effectiveness during endoscopic stenting of malignant hilar strictures: the role of liver volume assessment. Gastrointest Endosc 2010;72:728-35.
- Vilgrain V. Staging cholangiocarcinoma by imaging studies. HPB (Oxford) 2008;10:106-9.
- Vogel A, Wenzel P, Folprecht G, et al. Nal-IRI and 5-FU/LV compared to 5-FU/LV in patients with cholangio- and gallbladder carcinoma previously treated with gemcitabine-based therapies (NALIRICC – AIO-HEP-0116). Ann Oncol 2022;33(suppl_7):S19-S26.
- Wakai T, Shirai Y, Yokoyama N, Nagakura S, Watanabe H, Hatakeyama K. Early gallbladder carcinoma does not warrant radical resection. Br J Surg 2001;88:675-8.
- Walter T, Horgan AM, McNamara M, et al. Feasibility and benefits of second-line chemotherapy in advanced biliary tract cancer: a large retrospective study. Eur J Cancer 2013;49:329-35.
- Weber A, von Weyhern C, Fend F, et al. Endoscopic transpapillary brush cytology and forceps biopsy in patients with hilar cholangiocarcinoma. World J Gastroenterol 2009;14:1097-101.
- Weber SM, DeMatteo RP, Fong Y, Blumgart LH, Jarnagin WR. Staging laparoscopy in patients with extrahepatic biliary carcinoma. Analysis of 100 patients. Ann Surg 2002;235:392-9.
- Weber SM, Ribero D, O’Reilly EM, Kokudo N, Miyazaki M, Pawlik TM. Intrahepatic cholangiocarcinoma: expert consensus statement. HPB (Oxford) 2015;17:669-80.
- Weilert F, Bhat YM, Binmoeller KF, et al. EUS-FNA is superior to ERCP-based tissue sampling in suspected malignant biliary obstruction: results of a prospective, single-blind, comparative study. Gastrointest Endosc 2014;80:97-104.
- Welzel TM, McGlynn KA, Hsing AW, O’Brien TR, Pfeiffer RM. Impact of classification of hilar cholangiocarcinomas (Klatskin tumors) on the incidence of intra- and extrahepatic cholangiocarcinoma in the United States. J Natl Cancer Inst 2006;98:873-5.
- WHO. ICD-11 implementation or transition guide. Geneva: World Health Organization, 2019.
- Wu LM, Jiang XX, Gu HY, et al. Endoscopic ultrasound-guided fine-needle aspiration biopsy in the evaluation of bile duct strictures and gallbladder masses. Eur J Gastroenterol Hepatol 2011;23:113-20.
- Yamaguchi K, Tsuneyoshi M. Subclinical gallbladder carcinoma. Am J Surg 1992;163:382-6.
- Yang J, Wang J, Zhou H, et al. Efficacy and safety of endoscopic radiofrequency ablation for unresectable extrahepatic cholangiocarcinoma: a randomized trial. Endoscopy 2018;50:751-60.
- Yeh YC, Lei HJ, Chen MH, et al. C-Reactive Protein (CRP) is a promising diagnostic immunohistochemical marker for intrahepatic cholangiocarcinoma and is associated with better prognosis. Am J Surg Pathol 2017;41:1630-41.
- Yoo C, Jeong H, Kim KP, et al. Adjuvant gemcitabine plus cisplatin (GemCis) versus capecitabine (CAP) in patients (pts) with resected lymph node (LN)-positive extrahepatic cholangiocarcinoma (CCA): A multicenter, open-label, randomized, phase 2 study (STAMP). J Clin Oncol 2022;40(16_suppl):4019-4019.
- Yoon SB, Moon SH, Ko SW, Lim H, Kang HS, Kim JH. Brush cytology, forceps biopsy, or endoscopic ultrasound-guided sampling for diagnosis of bile duct cancer: a meta-analysis. Dig Dis Sci 2022;67:3284-97.
- Z’graggen K, Birrer S, Maurer CA, Wehrli H, Klaiber C, Baer HU. Incidence of port site recurrence after laparoscopic cholecystectomy for preoperatively unsuspected gallbladder carcinoma. Surgery 1998 ;124:831-8.
- Zehir A, Benayed R, Shah RH, et al. Mutational landscape of metastatic cancer revealed from prospective clinical sequencing of 10,000 patients. Nat Med 2017;23:703-713. Erratum in: Nat Med 2017;23:1004.
- Zheng Y, Tu X, Zhao P, et al. A randomised phase II study of second-line XELIRI regimen versus irinotecan monotherapy in advanced biliary tract cancer patients progressed on gemcitabine and cisplatin. Br J Cancer 2018;119:291-5.
- Zhu AX, Macarulla T, Javle MM, et al. Final overall survival efficacy results of ivosidenib for patients with advanced cholangiocarcinoma with IDH1 mutation: The Phase 3 randomized clinical ClarIDHy trial. JAMA Oncol 2021;7:1669-77.

