7.2.1. Diagnostic
7.2.1.1. Evaluation du foie non tumoral
- Le diagnostic de la cirrhose peut être fortement évoqué sur des critères cliniques, biologiques (TP, plaquettes, albuminémie, marqueurs de fibrose), endoscopiques (varices œsophagiennes), et morphologiques (dysmorphie hépatique et signes d’hypertension portale en échographie ou scanner).
- En l’absence d’argument clinique, radiologique ou biologique pour une cirrhose, une biopsie du foie non tumoral est indispensable pour faire la preuve de la cirrhose ou d’une hépatopathie chronique sous-jacente. Elle permet en effet d’évaluer la sévérité de l’atteinte hépatique (activité) et aide à l’identification de son étiologie. La valeur des tests non invasifs de fibrose (Fibrotest®, Fibromètre®, Hepascore®, Fibroscan®) n’est pas établie en présence d’une tumeur hépatique.
- De plus, la biopsie en foie non-tumoral peut aider à porter le diagnostic de CHC sur la partie tumorale grâce à la comparaison de la morphologie du tissu (notamment en cas de tumeur très bien différenciée).
7.2.1.2. Diagnostic du CHC
Le diagnostic du CHC est généralement envisagé suite à la découverte d’une lésion hépatique à l’échographie, ou à l’occasion de symptômes lorsque la tumeur est à un stade évolué. La preuve histologique doit être la référence pour le diagnostic de CHC, sauf en cas de contre-indication à une biopsie percutanée. Étant donné que plusieurs options thérapeutiques, y compris à visée curative, sont désormais disponibles, le recours systématique aux critères non invasifs expose au risque d’erreur diagnostique, en particulier pour les nodules de moins de 3 cm de diamètre (Compagnon, Grandadam et al. 2008). Des études indiquent par ailleurs que des cholangiocarcinomes intra-hépatiques (y compris pour des tailles de 2,0 à 3,5 cm) - qui partagent les principaux facteurs de risque de CHC - peuvent avoir une cinétique de rehaussement identique à celle des CHC aussi bien en TDM (Mendiratta-Lala, Park et al. 2016) qu’en IRM (Huang, Wu et al. 2016). Le diagnostic des petits nodules découverts lors de la surveillance des cirrhoses par échographie est souvent difficile ; la sensibilité des critères non invasifs est faible pour les tumeurs de moins de 10 mm (Lee, Lee et al. 2015) pour lesquelles le diagnostic de CHC ne peut être affirmé que dans environ un tiers des cas (Trinchet, Chaffaut et al. 2011).
L’utilisation des critères non invasifs - valables uniquement en cas de cirrhose sous-jacente - doit se faire avec rigueur sur le plan technique et dans leur interprétation, en particulier en ce qui concerne les examens d’imagerie. Cette démarche nécessite une discussion en réunion de concertation pluridisciplinaire (RCP). En l’absence de ces conditions, la biopsie est indispensable.
Par ailleurs, le manque d’examen histologique pénalise la recherche dans la mesure où l’étude de la tumeur, de même celle du foie non tumoral, sont essentielles aux progrès des connaissances sur les mécanismes de carcinogenèse et la détermination de biomarqueurs pronostiques et prédictifs de la réponse aux traitements (intérêt des tumorothèques).
7.2.1.3. Examens complémentaires
7.2.1.3.1. Imagerie
La caractérisation du ou des nodule(s) repose sur l’examen de leur vascularisation. La standardisation de l’imagerie (technique et interprétation) est un enjeu important qui a conduit à la création du système LI-RADS (Liver Imaging Reporting and DataSystem) (Santillan, Cherniayk et al, 2017) qui propose une classification radiologique des nodules hépatiques, selon leur probabilité d’être un carcinome hépatocellulaire, allant de lésions bénignes à des nodules hautement évocateurs de CHC. Les critères (CT/MRI LIRADSVR v2018, CT/MRI LI-RADSVR v2018 et gradés en 5 stades : 1 (définitivement bénin - en imagerie) au 5 (définitivement malin - en imagerie) (https://www.acr.org/-/media/ACR/Files/RADS/LI-RADS/LI-RADS-2018-Core.pdf?la=en) qui prennent en compte le rehaussement à la phase artérielle, la taille tumorale, le lavage et la croissance sur des examens successifs améliorent le diagnostic en particulier pour les petits nodules. Il est à noter que l’AASLD, l’EASL et l’AFEF ont adopté officiellement le système LI-RADS (Marrero JA, Kulik LM 2018). L’utilisation de ces critères est hautement recommandée pour permettre une meilleure standardisation des comptes-rendus radiologiques et un suivi optimal des malades.
Il est important de souligner que les critères de diagnostic non invasifs utilisant LI-RADS n'ont été validés que dans les populations de patients atteints de cirrhose ou d’une infection chronique par le virus de l’Hépatite B (VHB). En dehors de ce cadre, une biopsie à visée diagnostique histologique est nécessaire même si la cinétique semble typique en imagerie (Mitchell DG, Bruix J, 2015).
- Le scanner hélicoïdal et l’IRM avec triple acquisition artérielle, portale et tardive sont les deux examens de référence ; le signe le plus évocateur de CHC est l’existence d’un nodule hypervascularisé au temps artériel précoce (wash-in) avec lavage (wash-out : hypodensité ou hypointensité par rapport au parenchyme hépatique non tumoral) à la phase portale ou à la phase tardive par rapport au parenchyme non-tumoral (EASL2018); cet aspect correspond à des nodules « déportalisés » ayant un apport artériel exclusif ; cette diminution du rehaussement au temps portal par rapport au foie non-tumoral est à distinguer d’une simple diminution du signal par rapport au temps artériel, qui peut être observée dans presque toutes les tumeurs hépatiques bénignes et malignes.
- L’IRM semble être légèrement supérieure au scanner en termes de sensibilité pour la détection et la caractérisation des nodules, permettant notamment de distinguer les nodules de régénération des nodules cancéreux (Colli, Fraquelli et al. 2006).
- L’échographie de contraste est le plus récent des examens permettant de caractériser la vascularisation d’un nodule. Sa sensibilité pour dépister l’hypervascularisation à la phase artérielle est supérieure à celle du scanner (Bolondi, Gaiani et al. 2005). La cinétique du wash-out en échographie de contraste est d’autant plus lente que le CHC est bien différencié. Cependant, des cholangiocarcinomes peuvent avoir en échographie de contraste de type SonoVue une dynamique de remplissage et de lavage identiques à celle d’un CHC (Rimola, Forner et al. 2009). De ce fait, l’échographie avec produit de contraste n’est pas recommandée pour le diagnostic non invasif de CHC.
Par ailleurs, l’échographie de contraste est peu accessible et n’est pas adaptée au bilan d’extension du fait de son incapacité à étudier l’ensemble du foie. Par définition, un wash-out suppose l’existence d’une hypervascularisation à la phase artérielle, qui peut être fugace et survenir entre 15 et 30 secondes après le début de l’injection intraveineuse. Cependant les nodules hypodenses à toutes les phases sont a priori des macronodules cirrhotiques, qui doivent être particulièrement surveillés en raison de leur risque de transformation en CHC. Une étude ayant comporté un suivi longitudinal rapporte l’apparition d’une prise de contraste dans 60% des cas (Vullierme, Paradis et al. 2010). - Le TEP-scan au 18F-FDG et/ou à la choline n'ont pas leur place dans le diagnostic du CHC. En effet, la captation du FDG-PET est observée dans moins de 40% des cas (Chalaye, Costentin 2018) et la plupart des CHC bien différenciés sont négatifs. Un autre traceur, la 11C-choline, pourrait être utile pour détecter des tumeurs bien différenciées. Cependant, le taux global de détection de la TEP/CT est inférieur à celui de la TDM et de l'IRM (Chotipanich, Kunawudhi 2016). Enfin, une étude récente évaluant l’utilisation systématique de la TEP-TDM au 18FDG et à la Choline, n’a pas retrouvé d’amélioration significative par rapport à l’utilisation de l’imagerie en coupe par TDM et IRM.
7.2.1.3.2. Ponction biopsie du foie tumoral
La biopsie est utile au diagnostic
La valeur prédictive positive des résultats d'imagerie est directement proportionnelle à la taille de la tumeur, avec une précision sensiblement plus faible pour les lésions plus proches du seuil de 1 cm (Roberts LR, 2018). Les critères secondaires parfois utilisés tels que le rehaussement concentrique progressif, le rehaussement périphérique à la phase artérielle sont associés à une tumeur maligne dans plus de 90 % des cas, mais seulement 36 % sont des CHC. Il est donc recommandé de classer tous les cas présentant des caractéristiques douteuses dans la catégorie LR-M au lieu de LR-5 et de procéder à une biopsie pour établir un diagnostic définitif. (Fowler KJ, Tang AN 2018). La distinction précise des observations LR-5 et LR-M peut être difficile, en particulier pour les lecteurs non experts, ce qui peut conduire à un sur-diagnostic de CHC (Fowler KJ, Tang AN 2018).
Dans 10-15 % des cas le CHC est d’aspect infiltrant à l’imagerie sans lésion focale évidente. Une biopsie en foie tumoral et non tumoral est alors recommandée.
Par ailleurs, un certain nombre de nodules correspondent, après examen histologique, à des nodules bénins hépatocytaires (régénératifs ou non), à des hémangiomes, à des lésions malignes (cholangiocarcinomes ou tumeurs mixtes de type hépato-cholangiocarcinomes). Des études récentes ont montré qu’il existait un taux d’erreur diagnostique, même en centre expert, de 5 à 17 %, ce qui ne semble pas acceptable vu les modalités thérapeutiques très différentes de ces tumeurs (Brusset B, Jacquemin M 2023).
Enfin, la cirrhose peut être considérée comme un environnement pré-néoplasique dans lequel se développent des nodules cirrhotiques dont certains évoluent en nodules dysplasiques, présentant un risque de transformation maligne allant d’environ 20 % (nodules dysplasiques de bas grade de malignité) à 60 % (nodules dysplasiques de haut grade de malignité). Leur caractérisation et le diagnostic différentiel entre nodule dysplasique de haut grade et CHC bien différencié est possible par la biopsie en combinant une analyse histologique standard et une analyse immunohistochimique (Park YN. 2011; Di Tommaso L, Destro A, 2009). La caractérisation précise de ces nodules (de moins de 2 cm) est importante pour la prise en charge. La coexistence possible de nodules de CHC et de nodule de cholangiocarcinome sur foie cirrhotique peut conduire à réaliser des biopsies sur plusieurs nodules chez le même patient si ceux-ci ont des comportements différents en imagerie.
La biopsie est utile pour la caractérisation des tumeurs à visée thérapeutique
La caractérisation des tumeurs devient un élément indispensable pour la prise en charge. En effet, de plus en plus de données démontrent que les CHC présentent une grande hétérogénéité tant sur les plans histologiques que moléculaires, se répartissant en différents sous-types patho-moléculaires caractérisés par des anomalies génétiques et des profils d’expression moléculaire qui permettent d’établir des classifications transcriptomiques du CHC (Zucman-Rossi, Villanueva et al. 2015). UnUn groupe français a proposé une classification identifiant 6 sous-types basés sur des critères cliniques, histologiques, génétiques et moléculaires (Calderaro, Couchy et al. 2017). L’ensemble de ces connaissances permettront dans un futur proche un diagnostic plus précis ouvrant la voie à une stratégie thérapeutique personnalisée, adaptée à chaque groupe de patients. À l'heure actuelle, il semble judicieux que chaque patient potentiellement candidat à un traitement dispose d'un prélèvement tant de la tumeur que du tissu hépatique non tumoral, afin d’anticiper les avancées futures dans ce domaine. La biopsie est également utile pour l’évaluation pronostique dans la mesure où le grade de différenciation tumorale est un facteur pronostique du CHC (Sia, Villanueva et al. 2017) et qu’il a été montré que les sous-types moléculaires (G1 à G6) identifiables sur l’histologie sont associés à des profils évolutifs différents (Calderaro, Couchy et al. 2017). Ainsi, le sous-type « macrotrabéculaire massif », souvent associé à des mutations p53 et représentant environ 12 % des CHC, est de mauvais pronostic (Ziol et al. 2017). Les sous-types de CHC de mauvais pronostic (macro-trabéculaire massif et peu différenciés), sont de plus moins souvent typiques en imagerie selon les critères LI-RADS (Brusset et al. 2023). D’autres marqueurs prédictifs sont en cours d’étude (par exemple, VETC pour l’association atezolizumab-bevacizumab), mais n’ont pas encore atteints le stade de validation clinique (CO AFEF 2025). Ceci renforce l’intérêt de disposer d’une biopsie pour informer les décisions thérapeutiques dans le futur.
Conditions techniques de réalisation et risques de la biopsie
La biopsie utilisant des aiguilles de 14 à 18 G, qui fournit un matériel tissulaire permettant une analyse histologique, doit être préférée à la ponction aspiration à l’aiguille fine de 20 à 25 G qui ne permet qu’une analyse cytologique, insuffisante en particulier pour le diagnostic différentiel entre les nodules dysplasiques et le CHC reposant sur des critères architecturaux. Il est essentiel, de comparer des fragments de foie tumoral et non tumoral (Vullierme, Paradis et al. 2010).
La biopsie doit être faite au travers d’une épaisseur notable de parenchyme non tumoral et avec une protection du trajet pariétal (aiguille coaxiale). Cette technique limite le risque d’essaimage sur le trajet de ponction (1,3 % contre 3,1 % sans protection) (Fotiadis N, De Paepe KN 2020). Du fait de ce risque, même mineur, lorsqu’une transplantation est envisagée, la biopsie ne doit pas être faite avant d’avoir contacté le centre référent même si la réalisation d’une biopsie ne semble pas affecter l’évolution oncologique des patients avec un CHC en indication de transplantation (Fuks, Cauchy et al. 2014).
En cas de traitement percutané, une biopsie peut être faite soit avant la séance soit par l’aiguille introductrice lors de la première séance.
Performances diagnostiques de la biopsie hépatique
Une étude prospective a évalué la performance de la biopsie dans le diagnostic des nodules solitaires de diamètre inférieur à 2 cm, détectés par échographie. Le diagnostic de CHC est confirmé à la première biopsie dans 70 % des cas et, en cas de première biopsie négative, le taux de faux négatifs atteint encore 39 % à la seconde biopsie (Forner, Vilana et al. 2008). Il est probable que la performance de la biopsie sera augmentée par l’utilisation de marqueurs moléculaires de CHC, d’autant que certains sont applicables sur tissu inclus en paraffine (Di Tommaso L Destro A 2007).
Parmi ceux-ci, la présence des mutations du promoteur de TERT permet d’affirmer que le nodule est déjà engagé dans le processus de malignité et doit être considéré comme un CHC (Nault JC, Martin Y 2020, Beaufrère A Paisley S 2023).
En pratique, une biopsie « négative » n’élimine pas le diagnostic de CHC
Selon les recommandations de l'AASLD, les biopsies des nodules de petite taille doivent être examinées par des anatomopathologistes experts. En cas de résultat non concluant ou discordant avec l’imagerie (par exemple description de tissu cirrhotique uniquement alors qu’il existe un nodule hyperartérialisé en imagerie), une deuxième biopsie est conseillée. Après deux biopsies négatives, les malades doivent être suivis par échographie et/ou scanner ou IRM tous les 3 à 6 mois jusqu'à ce que le nodule disparaisse, augmente de taille ou remplisse les critères diagnostiques de CHC ; si le nodule augmente de taille et reste atypique, une nouvelle biopsie est recommandée.
7.2.1.3.3. Marqueurs tumoraux
- Une élévation de l’ α-fœtoprotéine (aFP), même supérieure à 400 ng/ml, n’est pas en elle-même assez spécifique pour poser le diagnostic de CHC, celle-ci pouvant être augmentée en cas de tumeurs germinales ou d’autres tumeurs digestives (Bruix and Sherman 2011, 2012). Un tel résultat doit néanmoins faire activement rechercher un CHC avec la réalisation d’une imagerie en coupes hépatique, notamment en contexte d’hépatopathie chronique.
7.2.1.4. Critères de diagnostic du CHC
REFERENCES
Analyse histologique d’un fragment tumoral obtenu par ponction biopsie dirigée sous échographie ou scanner, comparée à un fragment de foie non tumoral prélevé simultanément (niveau de recommandation : accord d’experts).
OPTIONS
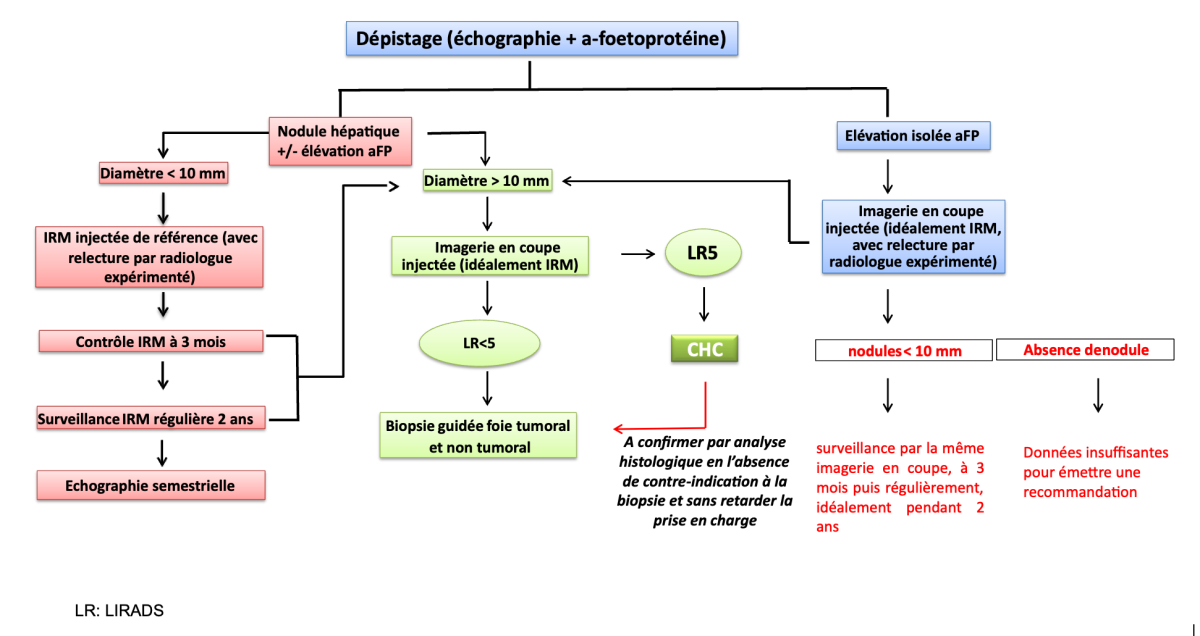
Lorsqu'un nodule est détecté chez un patient atteint de cirrhose confirmée, l’utilisation de critères non invasifs (suivant la classification LIRADS) est proposée, particulièrement chez les patients non accessibles à la biopsie.
Il est indispensable de respecter les recommandations techniques concernant la réalisation des examens d’imagerie, décrites sur le site de la Société française de radiologie et de faire valider le diagnostic non invasif par une RCP « spécialisée », c’est-à-dire comportant au moins les compétences en hépato-gastroentérologie/hépatologie, radiologie diagnostique et interventionnelle, chirurgie hépatique et transplantation, oncologie médicale et oncologie radiothérapie.
Les nodules de moins de 1 cm doivent être surveillés par échographie (et/ou TDM ou IRM) tous les 3 mois. S’il n’y a pas d’augmentation du diamètre avec un recul de 2 ans, on peut revenir à la périodicité habituelle de la surveillance échographique (niveau de recommandation : grade C).
7.2.2. Eléments nécessaires à la discussion thérapeutique
Contrairement aux autres tumeurs solides, dont la prise en charge est guidée par la classification TNM, il n’y a pas de système pronostique universellement consensuel pour le CHC (Olthoff, Forner et al. 2011). De nombreuses système de classifications ou scores pronostiques ont été proposés (Okuda, CLIP, GRETCH, TNM-AJCC…) ou le BCLC qui est plus un algorithme décisionnel qu’un score strictement pronostique. Toutefois, les études comparatives entre ces classifications ont rapporté des résultats hétérogènes La classification BCLC est le plus souvent utilisée dans les recommandations internationales.
En pratique, ces classifications ont en commun trois paramètres indispensables à la prise de décision thérapeutique : l’extension tumorale (nombre, taille des tumeurs, extension vasculaire / extra-hépatique), l’état du foie sous-jacent (fonction hépatique, hypertension portale) et l’état général du patient.
7.2.2.1. Bilan d'extension tumorale
Il comporte, outre l’examen clinique et l’AFP (intérêt dans le pronostic et le suivi), une imagerie adaptée par IRM abdominale + scanner thoracique ou scanner thoraco-abdominal (avec injection de produit de contraste). L’imagerie correctement réalisée permet de préciser la morphologie tumorale (localisation, nombre et taille des lésions, présence d’une capsule et/ou de tumeurs « filles »), la vascularisation portale et sus-hépatique, l’existence d’adénopathies ou de métastases viscérales (poumons, os, surrénales…), et le retentissement sur les voies biliaires. Le scanner permet le calcul des volumes hépatiques Un scanner cérébral et une scintigraphie osseuse seront réalisés en cas de point d’appel clinique.
- Certaines études ont évalué l’utilisation du TEP-scan (Sharma, Martin et al. 2013) avec de nouveaux traceurs telle que la choline qui semble améliorer la détection des lésions extra-hépatiques (Lopci, Torzilli 2015) et pourrait modifier certains choix thérapeutique (Chalaye, Costentin 2018). La captation du 18-FDG pourrait être associée à des formes histologiques de plus mauvais pronostic (HU S, 2023), à l’invasion tumorale (Hong, Suh 2016) et à un risque accru de récidive post-opératoire (Lim C 2019). Cependant, l’étude prospective PET-HCC01, n’a pas permis de montrer l’intérêt de l’utilisation d’une double TEP (18FDG et Choline) lors de l’évaluation pré-thérapeutique des patients (Nault, Boubaya 2025). Il n’est donc pas recommandé de faire une TEP-scanner dans le bilan pré-thérapeutique d’un CHC.
7.2.2.2. L’évaluation du foie non tumoral est essentielle
L’aspect histologique du foie non tumoral, incluant le degré de l’atteinte en termes de fibrose, doit être connue.
Un bilan étiologique de l'hépatopathie est également nécessaire, car les indications thérapeutiques peuvent varier en fonction de l'étiologie sous-jacente.
En cas de fibrose sévère (score F3) ou cirrhose (score F4), il est essentiel d’évaluer la sévérité de l’hépatopathie. Cela implique un bilan clinique, biologique (TP, albuminémie, bilirubinémie, ALAT/ASAT), détermination du score de Child-Pugh, du score MELD (Model for end-stage liver disease), du score ALBI (Johnson PJ, Berhane S. 2015) et la recherche de signes d’hypertension portale. Lorsqu’une résection est envisagée, le volume de foie restant est évalué par volumétrie. D’autres analyses ne sont pas recommandées de façon systématique mais peuvent être faites au cas par cas avant résection chirurgicale (tests « fonctionnels » mesure de la pression portale par cathétérisme sus-hépatique…)
Le Fibroscan® est recommandé pour l’évaluation de la fibrose ou de l’hypertension portale. Dans le contexte de CHC, il y a peu de données concernant l’interprétation ou la faisabilité du Fibroscan®. Le CHC est un facteur associé à l’échec des mesures (Cescon,M; Colecchia, A 2012 ; Dong J, Qing S, 2014) avec des variations importantes des valeurs seuil optimales selon la localisation du CHC (Huang TH, Lin MT 2021)
La présence d’une hypertension portale conditionne la prise en charge. Les recommandations sur la gestion de l’HTP ont été fortement révisées lors de la dernière conférence de Baveno VII, redéfinissant le dépistage et élargissant les indications de prophylaxie.
Dans le contexte de CHC, les critères de BAVENO posent plusieurs problèmes d’utilisation dont l’incertitude sur l’interprétation de l’élastométrie (Grgurevic I, Bokun T 2018) ou une augmentation du taux de plaquettes liée à l’inflammation et au CHC (Thabut, D, Kudo M 2023) avec des risques de faux négatifs.
L’endoscopie digestive haute à la recherche de signe d’HTP est donc recommandée avant prise en charge de CHC.
La fonction hépatique est évaluée par les scores suivants ci-dessous : Child-Pugh, MELD et ALBI.
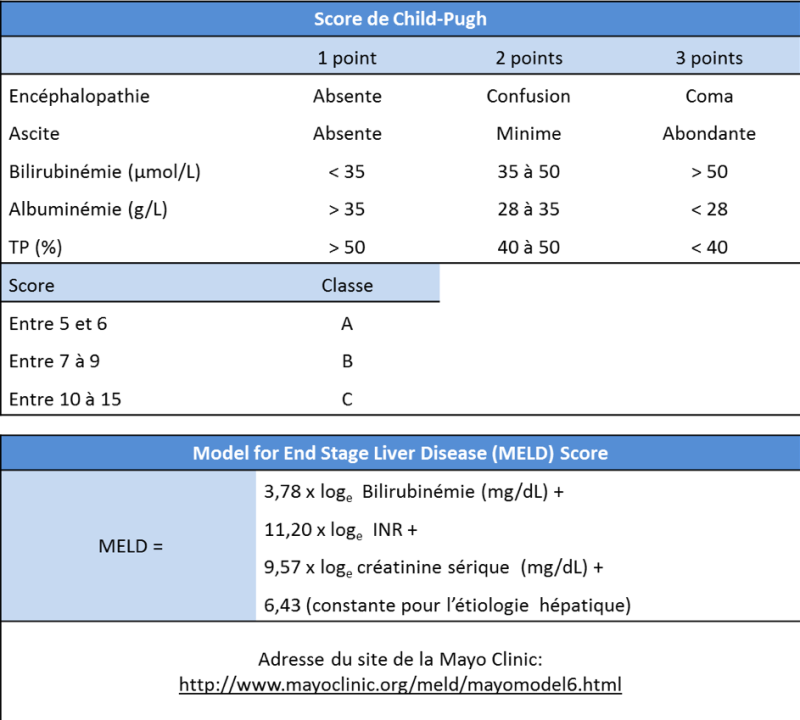
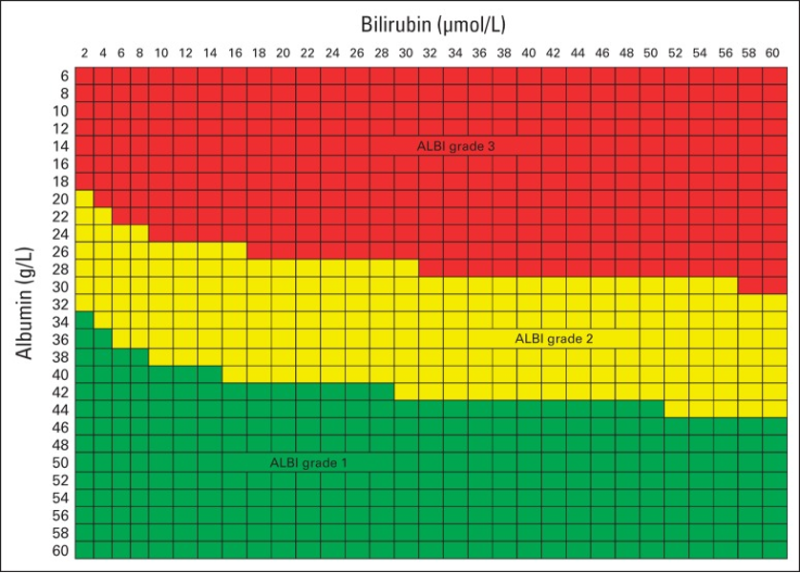
(log10bilirubine (µmol/L)*0,66) + (Albumine (g/L)*-0,085) (Johnson. J Clin Oncol 2015).
7.2.2.3. Bilan général
- L’état général et d’activité doit être évalué (grade OMS), selon les recommandations de l’EORTC c’est-à-dire en tenant compte de l’état général induit par le cancer.
- Les comorbidités et cancers liés au terrain doivent être recherchés, en particulier en cas de cirrhose alcoolique et/ou de tabagisme associé, notamment si une transplantation est envisagée : insuffisance cardiaque et respiratoire, cancers broncho-pulmonaires, ORL et du tractus digestif supérieur.
- Les éléments du syndrome dysmétabolique (HTA, diabète, dyslipidémie) et ses complications (en particulier les coronaropathies), doivent être recherchés car fréquemment associés au CHC et sources possibles de difficultés dans la prise en charge (risque opératoire, traitement par anti-agrégants plaquettaires, stents actifs…).
- Un bilan pré-opératoire en concertation avec l’anesthésiste (EFR, gazométrie, ECG, échocardiographie, scintigraphie myocardique…) doit être effectué si la chirurgie est envisagée.
- Si un traitement systémique est envisagé des contre-indications à l’immunothérapie et aux traitement anti-angiogéniques seront recherchées.
7.2.2.4. Au terme du bilan, plusieurs éléments doivent impérativement être renseignés :
- L’évaluation de la fonction hépatique sous-jacente
- La confirmation diagnostique, ou à défaut une forte probabilité de CHC
- L’analyse de l’extension tumorale
- L’identification de critères de mauvais pronostic tumoral tels que l’extension vasculaire tumoral, le caractère infiltrant à l’imagerie, une élévation de l’AFP > 1 000 μg/L, ou une évolutivité rapide jugée sur l’imagerie et/ ou biologique
- L’évaluation l’état général et des comorbidités du patient

