7.3.1. Traitements à visée curative
7.3.1.1. Transplantation
Elle est indiquée chez les patients atteints de CHC sur cirrhose, et elle est considérée comme le traitement théorique « idéal » car traitant la tumeur et sa cause. L’indication consensuelle au niveau international est le CHC strictement localisé au foie, soit unique et mesurant de 2 à 5 cm de diamètre, soit sous forme de 2 ou 3 nodules ne dépassant pas 3 cm de diamètre, en l’absence de thrombose portale ou hépatique, y compris segmentaire (= critères de Milan = « petit CHC ») (Mazzaferro , Regalia et al. 1996). Dans ces conditions, la transplantation hépatique (TH) guérit 2/3 des malades avec des résultats comparables à ceux de la TH pour cirrhose sans tumeur (Bruix and Sherman 2005) ; (Clavien, Lesurtel et al. 2012). Des études rétrospectives ont montré à 5 ans des taux de survie globale de 63 à 80 % et des taux de récidive de 4 à 20%. Cependant, de fréquentes contre-indications (âge, état physiologique, comorbidités, alcoolisme actif, refus d'un traitement au long cours), et la pénurie de greffons en limitent les indications.
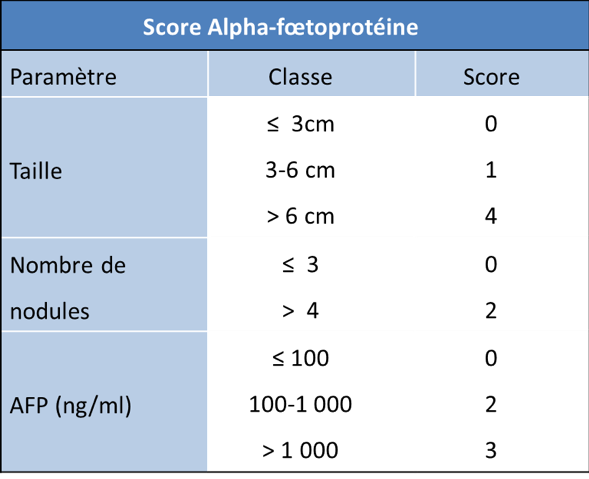
Le CHC représente en France 30 % des 1000 transplantations réalisées chaque année. En pratique, une indication de TH est discutée chez 10% des patients atteints de CHC, et elle est réalisée chez 3 à 4 %. Cette autolimitation est la conséquence de la pénurie de greffons et l’on observe deux tendances pour optimiser les résultats de la transplantation. La première est de privilégier la résection ou la destruction per-cutanée pour les CHC uniques. La seconde, à l’inverse, est d’élargir, de façon prudente, les indications de TH au-delà des critères de Milan. Plusieurs équipes ont rapporté de bons résultats chez des malades rentrant dans des critères plus larges que ceux de Milan : critères de San Francisco, critères 55-5, critères « up-to seven », score AFP même s’il n’a pas été trouvé de consensus international sur l’utilisation de ces critères étendus (Mehta N, Bhangui P et al. 2020). En France, cet élargissement des critères n’a pas été associé à une aggravation du pronostic, le taux de survie à 5 ans semblant identique à celui d’autres pays ayant conservé des critères restrictifs. Les critères d’attribution des greffons ont donc changé en 2013 avec l’adoption par l’Agence de la BioMédecine du score alpha-fœtoprotéine (aFP). En effet, il a été montré que jusqu’à un score de 2, les résultats de la greffe pour CHC sont excellents (Duvoux, Roudot-Thoraval et al. 2012). Ces résultats français ont été confirmés par une étude sud-américaine (Piñero, TisiBaña etet al. 2016) et italienne (Notarpaolo, Layese etet al. 2017).
- En pratique, pour les patients ayant un CHC au-delà des critères de Milan et pas de contre-indication à la TH, il est conseillé d’en référer à un centre de TH et de discuter cette option en RCP de recours.
En raison de l’allongement du délai avant TH, qui est passé pour les CHC de 3 mois dans la période 2003-2005 à 12 à 18 mois en 2014, il existe un risque de progression tumorale qui pose le problème d’un traitement « d’attente ». Son intérêt et ses modalités ne sont pas clairement définis. - En pratique, la plupart des centres décident soit d’effectuer un traitement d’attente par chimioembolisation (CE) artérielle, ou par radiothérapie interne sélective (SIRT) soit d’opter pour un « premier traitement curatif », résection ou destruction percutanée.
Un down-staging par ces traitements ramène parfois dans les critères de transplantation des tumeurs initialement au-delà de ces critères conduisant à rediscuter une transplantation. Un essai de phase 2, bien qu’interrompu précocement montre clairement le bénéfice en termes de survie sans récidive et de survie globale de la transplantation chez les patients initialement hors critères de Milan ayant pu être « downstagés » (Mazzaferro V, Citterio D et al. 2020). Il est donc capital de penser à la transplantation hépatique à chaque nouvelle évaluation tumorale des malades et de ne pas hésiter à demander un avis en centre de transplantation.
En pratique, compte-tenu de l’ensemble de ces données, l’inscription et le maintien sur la liste de transplantation en France se fait actuellement en fonction du score (aFP) élaboré par les centres de transplantation, réévalué tous les 3 mois en liste d’attente (cf. tableau).
Il n’y a pas d’accès à la greffe autrement que selon de score MELD en cas de tumeur unique de moins de 2 cm. Ces malades doivent donc en premier lieu être traités de manière curative par chirurgie ou destruction percutanée. Ce n’est que lors de la récidive du CHC, que des points spécifiques peuvent être obtenu pour un accès à la greffe.
De nombreuses composantes expert existent et permettent certains accès à la greffe. Celles-ci évoluent régulièrement et il est nécessaire de prendre contact avec un centre de greffe pour ne pas méconnaitre une possibilité d’accès pour un malade en âge d’être transplanté.
La transplantation hépatique avec donneur vivant pourrait être envisagée si le délai d’attente prévisible parait excessif, mais sa place reste actuellement très marginale en France.
En résumé, la transplantation hépatique s’inscrit dans une stratégie globale de prise en charge du CHC. De ce fait, le choix de réaliser des traitements en attente de greffe et le type de traitements doivent être établis en collaboration avec le centre de transplantation. Les patients potentiellement éligibles à une transplantation doivent donc être discutés dès le diagnostic initial de CHC, avant tout traitement, afin de définir avec le centre la meilleure stratégie. De même, des malades initialement inéligibles qui le deviennent, doivent être adressés à un centre de transplantation.
7.3.1.2. Résection
Pour les CHC sur cirrhose, elle est discutée chez les patients ayant une fonction hépatique préservée (Child-Pugh A) et en tenant compte du degré d’hypertension portale (Bruix and Sherman 2005, Bruix and Sherman 2011). Le volume du futur foie restant doit représenter au moins 40 % du volume hépatique total. Lorsqu’une hépatectomie droite est envisagée, celle-ci ne doit être réalisée que si une embolisation portale droite préalable a hypertrophié le foie gauche.
Dans ces conditions, la mortalité post-opératoire est < 5 %, et les taux à 5 ans de survie globale et sans récidive sont respectivement d’environ 50 % et 30 % (Bruix and Sherman 2005). Du fait de l’amélioration du bilan préopératoire, de la technique chirurgicale et du contrôle de la maladie hépatique sous-jacente, des séries récentes ont rapporté un taux de survie sans récidive à 5 ans de 65 % (Cherqui, Laurent et al. 2009) voire plus (Lim, Chow et al. 2012).
On admet actuellement que candidat idéal à la résection hépatique est un patient présentant un seul nodule un CHC unique de moins de 5 cm. Cependant plusieurs centres spécialisés ont rapporté de bons résultats en termes de survie après résection de tumeurs de plus grande taille et/ou multiples (Regimbeau, Farges et al. 1999, Delis, Bakoyiannis et al. 2010).
L’existence d’une thrombose portale néoplasique homolatérale à la tumeur n’est pas une contre-indication absolue à la résection si elle n’atteint ni la convergence ni le tronc de la veine porte (Shi, Lai et al. 2010). Cependant, dans cette situation, la chirurgie ne semble pas apporter de bénéfice en survie globale par rapport au sorafénib (Costentin C, Decaens T et al 2017). Avec l’arrivée des immunothérapies plus efficaces et mieux tolérées que le sorafénib, et le développement de la SIRT pour les invasions portales non tronculaires (cf. chapitres spécifiques), la chirurgie ne peut plus être considérée comme le traitement de référence dans les cas d’invasions vasculaires macroscopiques portale ou sus-hépatiques.
Idéalement, la résection d’un CHC doit consister en une résection anatomique comportant des marges de 2 cm (Shi, Guo et al. 2007, Slim, Blay et al. 2009).
En l’absence de fibrose importante (< F3) du foie non tumoral, la résection est le traitement de référence, même pour les tumeurs volumineuses.
7.3.1.3. Destruction per-cutanée
Cette méthode simple et habituellement bien tolérée, qui a l'avantage de préserver le parenchyme non tumoral, est une alternative à la chirurgie. Un traitement par radiofréquence monopolaire est envisageable :
- si la tumeur mesure moins de 3 cm, est accessible à la ponction sous échographie ou scanner, et se situe à distance du hile et des grosses voies biliaires ;
- en l’absence d’une anastomose bilio-digestive, d’un stent trans-papillaire ou d’une ascite importante qui sont des contre-indications.
Les durées de survie les plus longues sont observées chez les malades en rémission complète après traitement d’un CHC ≤ 3 cm de diamètre (Camma, Di Marco et al. 2005).
Il est admis qu’une destruction percutanée doit être proposée aux malades ne relevant pas d’une résection ; en fait, cette hiérarchie entre les 2 méthodes ne repose pas sur un niveau de preuve suffisant pour les petits CHC.
A ce jour, les données les plus nombreuses concernent la destruction par radiofréquence. Nous disposons ainsi de 6 études randomisées (Chen, Li et al. 2006, Lü, Kuang et al. 2006, Huang, Yan et al. 2010, Feng, Yan et al. 2012, Fang, Chen et al. 2014, Liu, Wang et al. 2016) et de 6 études rétrospectives (avec score de propension) ayant comparé la résection hépatique à la radiofréquence (Peng, Lin et al. 2012, Pompili, Saviano et al. 2013, Zhou, Lei et al. 2014, Kim, Shim et al. 2016, Liu, Hsu et al. 2016, Song, Wang et al. 2016). L’ensemble de ces études présente une puissance statistique limitée du fait d’effectifs de malades restreints. Parmi les études randomisées, seulement 2 études sont positives en survie globale et 3 en survie sans récidive en faveur de la chirurgie. Parmi les études rétrospectives, 2 études sont positives en survie globale en faveur de la chirurgie et deux en survie sans récidive en faveur de la chirurgie. La majorité des études montre un nombre de complications majeures significativement inférieur après la radiofréquence par rapport à la chirurgie.
Les deux approches semblent donner des résultats équivalents pour les nodules de CHC < 3 cm, le choix de la thérapeutique la plus adaptée au patient, doit se faire en tenant compte de la taille, de la localisation de la tumeur, du stade de l’hépatopathie sous-jacente, du projet thérapeutique global (attente de transplantation hépatique ou non…), de la disponibilité des outils, des techniques et de l’expérience des opérateurs (chirurgie et radiologie interventionnelle), ainsi que) et des souhaits du patient après une information éclairée des 2 options.
- D’autres techniques de destruction percutanée sont disponibles :
L’utilisation de sondes multipolaires permettrait de traiter de façon curative des tumeurs plus volumineuses, en particulier celles mesurant entre 3 et 5 cm et d’avoir un taux de récidive local inférieur à la radiofréquence monopolaire (Seror, N'Kontchou et al. 2008) (Hocquelet, Aubé et al. 2017). - La destruction par micro-ondes semble donner des résultats similaires à ceux obtenus par une ablathermie par radiofréquence selon une méta-analyse récente (Wicks JS, Dale BS et al.2023).
- L’électroporation irréversible est une technique non thermique qui pourrait trouver une place dans le traitement des tumeurs non ablatables par la chaleur (centrales proches du hile, contact avec structures digestives...) par son mode action intrinsèque. Mais plus de données sont nécessaires pour diffuser plus largement son utilisation.
Les intérêts, indications et performances relatives des différentes techniques sont résumés dans le tableau ci-dessous.
| Techniques d'ablation | Indications/Intérêts | Performances |
|---|---|---|
| Radiofréquence monopolaire | - Lésions moins de 3 cm | - Pas de différence de performance (récidive, survie globale) radiofréquence monopolaire et micro-onde |
| Micro-onde | - Lésions moins de 3 cm - Proximité vaisseaux car moins sensible au heat sign effect (théorique) | - Pas de différence de performance (récidive, survie globale) entre radiofréquence monopolaire et micro-onde - Diminution du taux de récidive pour les lésions proche des gros vaisseaux |
| Radiofréquence multipolaire multi-aiguilles | - Lésions jusqu’à 5 cm - Lésion sous capsulaire - Proximité des vaisseaux (dépose de plus d’énergie) | - Diminution du taux de récidive par rapport à radiofréquence monopolaire et micro-onde |
| Ablation monopolaire multi-aiguilles | - Lésions moins de 3 cm - Lésion sous capsulaire | - Diminution du taux de récidive par rapport à radio fréquence ou micro-onde monopolaire – mono-aiguille |
| Electroporation irréversible | - Moins de complication - Respect des structures vasculaires et biliaires | - A valider |
7.3.1.4. SBRT : la radiothérapie stéréotaxique (6 à 20 Gy/séance)
Ce traitement a été évalué depuis le début des années 90. Des études de phase I et II ont montré la faisabilité et la reproductibilité de la technique à plus grande échelle grâce aux accélérateurs de dernière génération, avec des complications rares. Le contrôle local à 1 et 2 ans est entre 90 et 100 %, avec des taux de survie globale à 1 et 2 ans respectivement de 80-90 % et 70 %. Cette technique est réalisable même pour de gros CHC, qui ne sont pas une contre-indication à la radiothérapie stéréotaxique (Andolino, 2011 ; Kwon, 2010 ; Bujold, 2013).
Il n’existe pas de comparaison directe entre les différents fractionnements de radiothérapie utilisés pour le traitement des CHC. Cependant, la plupart des études modernes ont utilisé des protocoles stéréotaxiques à dose curative (ablative) et les résultats obtenus sont basé principalement sur ce type de fractionnement (Bordeau K, Michalet M 2022). La dosimétrie est une étape cruciale et doit tenir compte des organes à risque dont le foie. La toxicité hépatique se limite le plus souvent à une cytolyse et/ou une cholestase anictérique (RILD : radio-induced-liver-toxicity), et une dégradation du score de Child pour certains patients cirrhotiques.
Un essai randomisé de phase III a montré la non-infériorité d’une radiothérapie stéréotaxique à base de protons versus radiofréquence pour les récidives de CHC de taille inférieure à 3 cm (Kim TH, Koh YH et al 2021).
Les résultats d’un essai randomisé réalisé en Chine comparant radiofréquence et radiothérapie stéreotaxique pour des tumeurs de moins de 5 cm ont récemment été publiés (XI M, Yang Z 2024). 166 patients ont été randomisés (83 dans chaque bras) avec des taux de contrôle local à deux ans en faveur de la radiothérapie (75,8 % dans le groupe radiofréquence vs 92,7 % dans le groupe radiothérapie, p=0,014), mais des survies sans progression/globale comparables.
Un essai randomisé de phase 2, clôturé prématurément suggèrerait l’intérêt de la radiothérapie stéréotaxique, même en cas d’invasion vasculaire VP3-4, (Dawson LA, Winter KA 2023) sous réserve de d’un bras contrôle par sorafénib sub-optimal à l’heure des immunothérapies.
Ce traitement peut être offert dans des centres expérimentés, disposant des équipements dédiés. Elle nécessite des accélérateurs de particules de dernière génération avec système d’imagerie intégré pour réaliser un gating respiratoire (synchronisation de la radiothérapie avec les mouvements respiratoires) ou du tracking hépatique (déplacement du faisceau en fonction des mouvements de la cible tumorale) pendant les séances. Ces méthodes permettent une meilleure tolérance en autorisant la respiration libre du patient, et peuvent ainsi être réalisées chez des patients plus fragiles notamment sur le plan cardio-respiratoire. Des systèmes de contention dédiés peuvent également être nécessaires.
La radiothérapie stéréotaxique est réservée aux patients avec CHC unique ou pauci-nodulaire non accessibles à la résection chirurgicale, à la transplantation et à l’ablation per-cutanée. Elle s'applique aux lésions < 10 cm, bien qu’au-delà de 5 cm, il semble exister un risque plus important d’hépatite radique. Cependant il n’existe pas de consensus sur le nombre maximal de lésions que l’on peut traiter dans la même séquence thérapeutique. Ce nombre est dépendant de la taille tumorale, de la localisation des lésions et de la technique utilisée. Il apparaît cependant peu raisonnable et non recommandable de traiter plus de 3 lésions dans la même séquence thérapeutique. Il est par ailleurs recommandé de ne pas considérer comme une contre-indication absolue pour la SBRT le volume tumoral sous réserve de respecter les contraintes dosimétriques.
Pour les CHC de plus grande taille (5-10 cm), les études initiales de cohorte montraient l’importance de l’associer à la CE (Merle, 2014). Cependant, l’intérêt d’associer radiothérapie et CE n'a pas été démontré dans une étude randomisée française, l’essai TACERTE (Féray C, Campion L 2023).
7.3.1.5. Traitement adjuvant
Traitement systémique
Après un traitement à visée curative par résection ou destruction percutanée, il y a un risque élevé de récidive locale (échec du traitement) ou à distance (nouveau CHC). Cela pose la question d’un traitement adjuvant. Plusieurs essais conduits en Asie (essentiellement sur des CHC développés sur cirrhose virale B) suggèrent l’intérêt d’une immunothérapie adoptive (Wang, Liu et al. 2016) mais cette stratégie reste difficile à mettre en place. Le sorafénib en traitement adjuvant après résection ou destruction percutanée a fait l’objet de plusieurs études dont une étude de phase III randomisée (Étude Storm) mais n’a pas montré de bénéfice en termes de survie sans récidive (Bruix, Takayama et al. 2015).
Plusieurs essais de phase III randomisés évaluent l’intérêt d’un traitement adjuvant par immunothérapie ou association immunothérapie - bevacizumab après résection ou destruction percutanée
Les résultats de l’étude internationale de phase III IMbrave050 comparant après résection ou destruction percutanée l’association d’atézolizumab 1200 mg et bevacizumab 15 mg/kg toutes les 3 semaines pendant 1 an, à la surveillance active ont été publiés en 2023 ( Qin S, Chen M,2023) Cette étude incluait des patients considérés comme à haut risque de récidive après résection ((i) ≤ 3 tumeurs dont une > 5 cm ou (ii) ≥ 4 tumeurs de moins de 5 cm ou (iii) présence d’invasion vasculaire et/ou d’une faible différenciation (grade 3-4)) ou des patients traités par radiofréquence (≤ 4 tumeurs entre 2 et 5 cm).
Cette étude comportait une majorité de patients asiatiques (83 %) avec hépatite B (62 %). Les tumeurs réséquées étaient le plus souvent uniques (90 %). 10 % des patients ont reçu une chimio-embolisation adjuvante dans chaque bras. La première analyse intermédiaire était positive pour l’objectif principal de survie sans récidive : 78 % vs 65 % à 1 an (HR 0.72 (0.56-0.93) p = 0.012). Cependant l’analyse finale ne confirmait pas ce résultat (ESMO 2024) et l’étude doit donc être considérée comme négative. Les résultats d’autres essais cliniques évaluant en situation (néo-)adjuvante l’immunothérapie seule ou en association avec un anti-angiogéniques sont encore en attente.
Actuellement aucun traitement adjuvant ne peut être recommandé après chirurgie ou résection percutanée de CHC (quel que soit le degré de risque de récidive).
Traitement de l’hépatopathie sous-jacente
La prise en charge concomitante de l’hépatopathie chronique améliore son pronostic et pourrait réduire le risque de récidive tumorale. Cette prise en charge concerne le traitement étiologique, les comorbidités et, en cas de cirrhose, la prévention des complications de l’hypertension portale.
Le seul intérêt potentiel d’utiliser des antiviraux ciblant le VHB, VHD et/ou VHC, est de prévenir l’évolution naturelle de dégradation progressive des fonctions hépatiques par l’infection virale chronique et de prévenir du risque de décompensation hépatocellulaire.
Pour le VHB, les recommandations internationales préconisent de traiter de façon systématique tous les patients cirrhotiques porteurs de l’AgHBs, quel que soit le niveau de la charge virale. Il en est de même en cas de CHC, même en l’absence de cirrhose.
Pour le VHC et le VHD, il n’existe aucune recommandation préconisant ou au contraire interdisant le traitement virologique en cas de traitement anticancéreux systémique du CHC par ICI ou ITK.
7.3.2. Traitements palliatifs
7.3.2.1. "Chimio"embolisation artérielle (CE)
Deux essais de phase III et deux méta-analyses ont rapporté en 2002 une prolongation de survie (+ 20 % de survie à 2 ans) chez les malades traités par CE (Llovet and Bruix 2003, Bruix and Sherman 2011). La différence avec les essais négatifs précédents était que seuls les malades ayant une fonction hépatique conservée avaient été inclus et d’autre part que les malades étaient atteints principalement de CHC sur hépatopathie chronique virale.
L’indication consensuelle pour la CE est « le traitement palliatif de première ligne des CHC évolués (en pratique multinodulaires), en l’absence de métastase et d’anomalie significative du flux portal, chez les malades Child-Pugh A ou B7, asymptomatiques et en bon état général (OMS 0) ».
Les obstructions tumorales portales non tronculaires (stade C de la classification BCLC) ne constituent pas une bonne indication pour la chimioembolisation, en raison de résultats décevants, et d’un bénéfice non démontré par rapport au traitement systémique.
Plusieurs scores ont été développés pour aider à identifier les bons candidats à la CE. Aucun n'est clairement validé et consensuel, mais certains critères utilisés dans ces scores sont associés à une faible efficacité de la CE tels que le caractère hypovasculaire et/ou infiltratif, la taille maximale des lésions et le caractère multinodulaire (score up-to-seven, score six and twelve…), l’élévation de l’AFP ou de la CRP. Chez ces patients, le choix entre CE et le traitement systémique doit être discuté au cas par cas en RCP spécialisée.
Modalités de chimio-embolisation
- Les modalités de la CE (type de chimiothérapie, agent d’embolisation, avec ou sans lipiodol, répétition systématique ou à la demande des séances) et de surveillance après traitement ne sont pas consensuelles. Néanmoins, l’attitude actuelle dans la plupart des centres est de privilégier des CEs sélectives ou hyper-sélectives permettant une épargne plus importante du parenchyme non tumoral, ce qui est en accord avec les recommandations de l’ESMO 2018 (Vogel A, Cervantes A 2019). Une étude rétrospective suggère que la CE hypersélective est plus efficace que la CE conventionnelle en termes de nécrose tumorale chez des malades en attente de TH (Dharancy, Boitard et al. 2007). Il pourrait s’agir d’une option pour des CHC de petite taille en cas d’impossibilité du traitement chirurgical ou percutané, même si les résultats dans cette situation sont inférieurs à ceux attendus après destruction per-cutanée (Hocquelet, Seror et al. 2016). Pour être réalisable la CE hypersélective doit s’adresser à une tumeur mono- ou pauci pédiculée, étant donc plus souvent périphérique que centro-hépatique, et d’une taille inférieure à 7-10 cm. L’état du foie non tumoral ne semble pas être un facteur limitant dans ce cas puisque le parenchyme non tumoral n’est pas concerné ; des résultats préliminaires suggèrent qu’une nécrose complète est obtenue dans plus de 50 % des cas.
- D’autres modalités de CE utilisant des microsphères chargées de cytotoxiques sont disponibles ; elles ont l’avantage d’une meilleure standardisation de la technique, mais, bien qu’un meilleur profil pharmacocinétique systémique du cytotoxique ait été constaté, leur supériorité sur la CE conventionnelle n’a pas été démontrée en termes de survie (Lammer, Malagari et al. 2010). Les billes chargées présentent par ailleurs une toxicité hépato-biliaire supérieure au lipiodol sur le foie non tumoral (Guiu, Deschamps et al. 2012, Monnier, Guiu et al. 2017).
Association chimio-embolisation et traitement systémique
- Il existe un rationnel scientifique en faveur de l’association de la CE avec des anti-angiogéniques et/ou des immunothérapies. Cependant une telle association, quel que soit le TKI ou l’anti-angiogénique (tel que le sorafénib (Lencioni R 2012) ou le brivanib (Kudo M 2013)) n’a pas montré d’allongement de la survie globale dans les études cliniques de phase II et III et ne doit donc pas être utilisée en pratique.
- La place de l’association de la CE avec une immunothérapie seule ou en association avec un anti-angiogénique a été évaluée dans plusieurs études de phase III dont 2 publiées ; l’étude EMERALD-1 étudiant l’intérêt du durvalumab en induction suivi de durvalumab +/- bevacizumab post-CE et l’étude LEAP 012 évaluant l’intérêt d’associer lenvatinib et pembrolizumab à la chimioembolisation.
- L’étude EMERALD-1 (Sangro B, Kudo M, 2025) était une phase 3 internationale, randomisée, en double aveugle et contrôlée par placebo ayant évalué l'efficacité et la sécurité du durvalumab, avec ou sans bevacizumab, en combinaison avec la chimioembolisation. Les données de l’analyse intermédiaire ont montré que l’ajout du durvalumab et du bevacizumab à la chimioembolisation améliorait de manière significative la survie sans progression (objectif principal) par rapport à la chimioembolisation seule. La SSP médiane était de 15 mois dans le groupe durvalumab + bevacizumab contre 8,2 mois dans le groupe placebo. L'ajout de durvalumab seul à la TACE n'a pas amélioré significativement la SSP par rapport à la TACE seule. La toxicité était essentiellement marquée par le syndrome post-embolisation (de manière similaire dans les 3 bras), et par les toxicités vasculaires (Hypertension, protéinurie) dans le bras bevacizumab. 24,7 % des patients du bras durvalumab + bevacizumab arrêtaient le traitement pour toxicité, vs 7 % dans le bras double placebo. Les données de survie globale sont immatures. Par ailleurs, le traitement était randomisé dès le début de la séquence, et certains patients en non-réponse à la CEL ont été traités par placebo, alors qu’ils relevaient d’un traitement systémique. L’utilisation de l’immunothérapie dès ce stade pose question pour un risque d’inefficacité secondaire au stade avancé, et les résultats actuels ne permettent pas de comparer les différentes séquences.
- L’étude de phase 3 LEAP 012 ( Kudo M, Ren Z 2025) multicentrique, randomisée, en double aveugle, a comparé la CEL combinée au lenvatinib et au pembrolizumab versus double placebo (LEAP-012) avec un co-objectif principal : la SSP et la SG. L'étude a montré une amélioration significative de la SSP avec lenvatinib plus pembrolizumab plus TACE par rapport au placebo plus TACE (SSP médiane de 14,6 mois contre 10,0 mois ; HR 0,66 ; p=0,0002). Il n’existe pas d’amélioration significative de la survie globale (HR 0,80 ; p=0,087) dans la première analyse. Les événements indésirables liés au traitement de grade 3 ou supérieur étaient plus fréquents dans le groupe lenvatinib plus pembrolizumab (71 %) que dans le groupe placebo (32 %). L’intérêt formel de l’association est difficile à déterminer en l’absence données plus matures de survie globale. Les études CARES-05 (TEG ASCO GI 2025) et TALENTACE (ESMO GI 2025) ont été présentées en congrès en 2025 et confirment ces informations : amélioration de la SSP, immaturité des données de SG, augmentation de la toxicité.
En résumé, bien que les essais d’association de la chimio-embolisation aux traitements systémiques (durvalumab/bevacizumab, lenvatinib/pembrolizumab) donnent des signaux encourageants (augmentation de la survie sans progression), les données sont encore immatures (en particulier pour la survie globale) pour recommander ces associations en routine clinique.
Transition chimio-embolisation vers traitement systémique
Compte tenu de la disponibilité de plusieurs thérapies systémiques efficaces, le choix du bon moment pour passer de la CE au traitement systémique est crucial. La poursuite d’un traitement inefficace par CE peut en effet être délétère en retardant voire empêchant l’utilisation de traitements systémiques en cas de dégradation de la fonction hépatique. L'échec de la CE peut être défini par l'apparition d'une invasion macrovasculaire, d'une dissémination extra-hépatique, ou de façon moins consensuelle par une augmentation de l'AFP après CE, l’absence de réponse radiologique objective après deux CE ou l'apparition de nouvelles lésions dans le territoire traité moins de six mois après la réalisation de la CE. La CE doit être également considérée comme en échec en cas de décompensation hépatique secondaire, et le passage aux traitements systémiques doit être discutés en cas de récupération de la fonction hépatique.
7.3.2.2. La radiothérapie interne sélective (Radioembolisation)/SIRT (selective internal radiotherapy)
La radiothérapie interne sélective repose sur l’injection intra-artérielle de microsphères de verre ou de résine marqués à l’Yttrium-90. Cette technique permet d’administrer de manière ciblée des radiations bêta à forte dose aux tumeurs hépatiques et de limiter l’exposition aux radiations du parenchyme hépatique normal. Le terme de « radiothérapie interne sélective » est plus adapté que le terme « radioembolisation » car le traitement repose sur l’irradiation, l’effet emboligène des microsphères utilisées étant peu marqué (Weber M, Lam M 2022).
La procédure se déroule en 2 temps réalisés au maximum à 2 semaines d’intervalle. La première partie consiste en une artériographie hépatique avec injection de macro-agrégats d’albumine marqués au technétium, avec scintigraphie au décours qui permet de vérifier l’absence de contre-indication (shunts digestifs ou pulmonaires). Cette phase « de simulation » permet également de quantifier la dose de radiation absorbée par la tumeur et de calculer l’activité à administrer lors de la 2ème phase. Cette première étape déterminante est un outil prédictif de la réponse tumorale et de la survie globale (Garin E, Guiu B 2022).
La 2ème artériographie, correspond au traitement, avec l’injection des microsphères marquées à l’Yttrium 90, le point d’injection étant nécessairement identique à celui de la 1re artériographie. L’Yttrium n’irradiant pas au-delà de 1 cm de chaque sphère, il n’y a pas de mesure de radioprotection particulière et le traitement peut être organisé en ambulatoire.
Sélection des patients pour la SIRT
Les critères de sélection des patients pour la SIRT sont basés sur la simulation du traitement (angiographie et scintigraphies au MAA) et la fonction hépatique (Weber M, Lam M 2022).
Les contre-indications en lien avec la fonction hépatique sont un score de Child-Pugh > 7, une hyperbilirubinémie > 35 µmol/L, une ascite, même uniquement radiologique.
Les contre-indications en lien avec une sur-irradiation d’organe à risques sont les shunts digestifs excessifs ou les shunts hépato-pulmonaires responsables d’une dose pulmonaire > 30 Gy (50 Gy en dose cumulative).
Les mauvaises indications ou contre-indications relatives sont :
- Les envahissements hépatiques majeurs (> 50 % du foie si cirrhose ; > 70 % du foie sans cirrhose ; maladie diffuse sur foie résiduel post hépatectomie) avec risque de toxicité hépatique trop important.
- Un état général altéré (ECOG > 1).
- Les patients avec maladie extra-hépatique significative
- Sur les données de la simulation de la SIRT, les patients avec un mauvais ciblage des tumeurs (avec dosimétrie insuffisante) ou un mauvais ciblage d’une thrombose porte lors de la simulation, ou les patients dont une particularité anatomique artérielle ne permettant pas de traiter l’ensemble de l’atteinte tumorale.
La SIRT en situation précoce (BCLC A)
Cette approche est apparue après la description de traitements hypersélectifs, appelés « segmentectomie radique » (Vouche M, Habib A 2014). Le principe est la concentration de l’irradiation dans un ou deux segments, permettant une forte dose tumorale, sans crainte de toxicité sur le foie sain car la majeure partie du parenchyme est épargnée. Les résultats ont été confirmés dans la large étude rétrospective multicentrique LEGACY (Salem R, Johnson GE 2021) réalisée chez 162 patients avec lésion unique ≤ 8 cm (taille médiane 2,3cm) traités en première intention par SIRT avec une approche curatrice de segmentectomie radique avec une survie sans progression à 24 mois de 78 %, un taux de survie globale à 3 ans de 86.6 % (IC 95% : 89.5-97.5). Le taux de réponse histologique complet était de 86 % pour une dose > 190 Gy vs 65 % pour une dose < 190 Gy, p=0.0001 (Gabr A, Riaz A 2021). Cette étude a mis en évidence que maximiser la dose au segment en dépassant une dose de 400 Gy entrainait 100 % de réponse histologique complète.
Par ailleurs, des études anatomopathologiques chez des patients secondairement réséqués ou transplantés ont montré des taux de réponse complète histologiques élevés lorsque la dose à la tumeur était supérieure à certains seuils (53 % si > 190 Gy, 75 % si > 500 Gy dans une étude avec microsphères de verre (Toskich B, Vidal LL 2021). L’essai de phase II monobras RASER (Kim E, Sher A 2022) confirme ces résultats rétrospectifs. Ces résultats peuvent faire discuter la place de la SIRT comme une option de traitement au stade A de la classification BCLC en cas de contre-indication à la résection ou à une ablation per-cutanée.
La SIRT dans les stades intermédiaires et en comparaison à la CE (BCLC A et B)
Plusieurs études ont comparé la CE et la RIS. Dans les études rétrospectives et de cohortes, le taux de réponse était de 40 à 50 %, le temps à progression de 13 mois et la médiane de survie globale de 20 mois (Salem, Lewandowski et al. 2011). Dans deux études rétrospectives comparatives, la RIS permettait un temps à progression supérieur à la CE pour un taux de complications moindre, mais sans différence de survie globale (Hilgard, Hamami et al. 2010, Salem, Lewandowski et al. 2011).
Deux études prospectives randomisées monocentriques de faible effectif ont suggéré une supériorité de la SIRT par rapport à la CE.
La première étude (Salem R, Gordon AC 2016) a comparé SIRT (n=24) et chimioembolisation (n=21) dans une population comportant 78 % de patients BLCC A et 22 % de BLCC B. Il s’agissait d’une approche à visée curatrice, soit en attente de transplantation, soit de downstaging vers la transplantation. Dans le bras SIRT, 54% des patients ont été transplantés, contre 33 % dans le bras chimioembolisation. La survie sans progression médiane était non atteinte à 26 mois dans le bras SIRT vs 6.8 mois pour la chimioembolisation, HR= 0,122 (IC 95%: 0,023-0,56), p=0.007.
La seconde étude (Dhondt E, Lambert B 2022) a comparé SIRT (n=38) et DCBeads (n=34) dans une population comportant 15 % de patients BCLCBLCC A et 85 % de BCLCBLCC B. Cette étude a été stoppée dès son analyse intermédiaire pré-planifiée (initialement prévue sur 136 patients) en raison de la positivité de son objectif principal de survie sans progression (17,1 mois dans le bras SIRT contre 9,5 mois dans le bras DCBeads (HR=0,36 ; p=0,02). La survie globale est de 27,6 mois dans le bras SIRT contre 15,6 mois dans le bras DCBeads (HR=0,49 ; p=0,01). Un down-staging avec transplantation a été obtenu dans 33 % dans le bras SIRT vs 10 % dans le bras chimioembolisation.
L’amélioration du temps à progression et la proportion significative de down-staging est d’un intérêt particulier dans le contexte de transplantation hépatique.
Ces études relancent le débat de l’avantage de la SIRT en comparaison avec la CE en particulier dans une stratégie de down-staging ou d’attente de transplantation.
En comparaison ou en association avec les traitements systémiques (BCLC B et C)
Trois essais de phase III randomisés ont évalué la RIS chez des patients ayant échappé à la CE et en indication théorique de traitement par sorafénib.
- L’essai français SARAH (Vilgrain, Pereira et al. 2017) comparant la RIS au traitement par sorafénib a inclus 459 patients. L’objectif principal de l’étude (amélioration de la survie globale) n’était pas atteint (8 mois pour le bras RIS vs 9,9 mois pour le bras sorafénib, HR = 1,15 (IC 95 % : 0,94-1,41) Log-rank p = 0,18). De même il n’existait pas d’amélioration de la survie sans progression (4,1 vs 3,7 mois, p=0,256, HR = 1,03 (IC 95% : 0,85-1,25) Log-rank P = 0,76). Même si les effets indésirables -notamment fatigue et diarrhée- sont moins fréquents dans le groupe RIS (76 % versus 94 %) et que l’analyse de la qualité de vie en faveur de ce groupe, cette étude négative ne permet pas de positionner définitivement la RIS comme une alternative au traitement par sorafénib.
- L’essai SIRveNIB (Chow, Ghandi. 2018) est un essai similaire dans sa conception à l’essai SARAH, mené en Asie. 360 patients (182 Y90, 178 sorafénib) ont été inclus dont 30,6 % avec présence d’une thrombose portale. Cette étude est aussi négative, avec un critère de jugement principal de survie globale de 8,8 mois dans le groupe RIS versus 10,0 mois dans le bras sorafénib (HR 1,1), mois). et une survie sans progression de 5,8 vs 5,1 mois (HR 0,89).
- L’essai SORAMIC (Ricke, Sangro 2018) a inclus 424 patients atteints d'un CHC inopérable qui ont été randomisés pour recevoir un traitement par RIS avec des microsphères de résine d'yttrium-90 (SIR-Sphères®) et sorafénib ou du sorafénib seul. La médiane de survie globale était de 12,1 mois dans le bras radioembolisation + sorafénib (n = 216) et à 11,5 mois dans le bras sorafénib (n = 208) ce qui n’était pas significatif.
Deux facteurs majeurs peuvent contribuer aux résultats négatifs de ces études randomisées : l’absence de dosimétrie personnalisé et le taux élevé de non-réalisation de SIRT à l’issue de la première phase suggérant une sélection sous-optimale des patients.
Les études avec dosimétrie personnalisés et meilleure sélection des patients (Child Pugh A, absence d’ascite radiologique, bilirubine < 35 µmol/mL, peu de thrombose tumorale tronculaire VP4, < 50 % d’envahissement tumoral), incluant une sélection des patients sur les données de simulation (dosimétrie/ciblage tumeur et ciblage thrombose), ont permis de relancer l’intérêt de la SIRT dans les CHC localement avancés.
L’étude DOSISPHERE 01 (Garin A, Tselikas L 2021) a comparé dosimétrie personnalisée (basée sur la dose tumoricide de 205 Gy, 250-300 Gy si possible avec les microbilles de verre) et dosimétrie standard (120 Gy au lobe traité) chez 60 patients (31 dans le bras dosimétrie personnalisée, 29 dans le bras dosimétrie standard) ayant des lésions très volumineuses (moyenne 10.5 cm), et avec un envahissement portal dans 68 % des cas. Le taux de réponse était de 71 % dans le bras dosimétrie personnalisé contre 36 %, p=0.0074, pour le bras dosimétrie standard et la survie globale de 26,6 mois dans le bras dosimétrie personnalisée vs 10,7mois HR=0.22 (IC95% : 0,21-0,82), p=0.0096.
Pour les patients avec invasion portale, la survie globale (ITT) était de 22,9 mois (IC95% : 9,1-NA) dans le bras dosimétrie personnalisée vs 9,5 mois HR=0.39 (IC95% : 0,17-0,92), p=0.023. Enfin une relation dose effet forte est démontrée pour le seuil de dose tumoricide ≥ 205 Gy (microbilles de verre) avec une survie globale médiane de 26,6 mois (IC95% : 13,5-NA) pour une dose 205 Gy vs 7,1 mois (IC95% : 4,6-14,8) mois pour une dose < 205 Gy, HR =0,33 (IC95% : 0,15-0,71), p=0,0029.
L’analyse rétrospective des résultats de SARAH en fonction de la dosimétrie reproduit des résultats similaires avec un seuil de 100 Gy (microsphères de résine, SIRsphere®) (Hermann AL, Dieudonné A et al 2020). Les résultats sont encourageants et ont conduit à des recommandations précises de réalisation technique du traitement permettant d‘améliorer significativement les résultats (Salem R, Padia SA 2019).
Néanmoins, des études prospectives et comparatives de phase 3 restent souhaitables pour positionner la place de la SIRT par rapport aux traitements systémiques actuels d’immunothérapie.
Cas particuliers des envahissements portaux
La possibilité de downstager des CHC avec thrombose porte a été rapporté dans 3 séries observationnelles avec accès à un traitement curateur dans environ 1/3 des cas et dans cette situation des survies 5 ans > 50 % (Serenari M, Cappelli 2021 ; Meerun MA, Allimant C 2023 ; Garin E, Tselikas L 2024).
Enfin, il existe un rationnel pour l’association de la SIRT avec l’immunothérapie. Des premiers essais de phase 1/2 ont montré la faisabilité mais il n’existe pas d’étude randomisée à l’heure actuelle permettant de mieux préciser l’articulation entre la RIS et l’immunothérapie en situation avancée.
La place de la SIRT dans la stratégie thérapeutique est progressivement mieux définie avec une importance majeure de la sélection des patients et de la réalisation d’une phase de simulation avec dosimétrie personnalisée.
Il existe des arguments forts pour un bénéfice de ce traitement à tous les stades de la maladie chez des patients avec une fonction hépatique préservée : BCLC A (en cas de contre-indication à résection, destruction per-cutanée ou SBRT), BCLC B (pour des lésions unilobaires en particulier dans une stratégie de down-staging) ou BCLC C (avec invasion vasculaire ciblable et < VP4).
Si une SIRT est envisagée, une dosimétrie personnalisée cherchant à obtenir une dose seuil délivrée à la tumeur suffisante (205 Gy si sphères de verre, 100 Gy si sphères de résine) doit être utilisée tout en préservant au moins 30 % de réserve hépatique.
7.3.2.3. Traitements médicamenteux
Traitement de première ligne
Association atézolizumab-bévacizumab
Les résultats de l’étude de phase III IMbrave 150 comparant l'association de l'atézolizumab 1200 mg toutes les 3 semaines (immunothérapie anti-PD-L1) et du bevacizumab 15 mg/kg toutes les 3 semaines (anticorps monoclonal ciblant le VEGF) au traitement par sorafénib ont été publiés en 2020 (Finn R, Qin S et al, 2020) avec une mise à jour en janvier 2021 (Finn R, Qin S et al, 2021). Les patients inclus avaient un état général conservé (OMS 0/1) et un score de CHILD A. L’association montre un bénéfice significatif en survie globale (19,2 vs 13,4 mois, HR : 0,66, p < 0.0009), en survie sans progression (6,9 contre 4,3 mois, HR : 0,65, p=0.0001) en taux de réponse selon RECIST 1.1 (30 vs 11 %, p <0.001%). L’étude ne rapporte pas de de suivi à long terme des patients. Le pourcentage d’effets indésirables de grade 3-4 imputables au traitement était similaire entre les 2 bras (43 vs 46 %), néanmoins les effets indésirables imputables à la combinaison expérimentale (HTA, protéinurie, cytolyse) ayant un impact moindre sur la qualité de vie, le temps à détérioration de la qualité de vie était significativement allongé par l’association atézolizumab-bevacizumab. L’analyse des résultats met en évidence un risque accru de saignement par hypertension portale sous bevacizumab (11 % vs 2 % de saignement par rupture de varices œsophagiennes). Ce risque hémorragique semble supérieur en données de vraie vie avec 14 % d’évènements hémorragiques dans la cohorte rétrospective de 216 patients avec CHC avancé traité par atézolizumab-bevacizumab de d’Alessio et al (d’Alessio Hepatology 2020). Un bilan endoscopique est donc justifié avant la mise en route de ce traitement et une prévention efficace de la rupture des varices doit être instaurée, idéalement par béta-bloquants.
L’association a obtenu une AMM en France en 2021 dans le traitement de première ligne des patients atteints de carcinome hépatocellulaire avancé ou non résécable, n’ayant pas reçu de traitement systémique antérieur, avec une fonction hépatique préservée (stade Child-Pugh A), un score ECOG 0 ou 1, et non éligibles aux traitements locorégionaux ou en échec à l’un de ces traitements.
Association durvalumab-trémélimumab
L’étude HIMALAYA publiée en Juin 2022 (Abou-Alfa GK, Lau G 2022) est un essai randomisé de phase III comparant en première ligne de traitement le sorafénib (389 patients) au schéma STRIDE (393 patients) associant une injection unique initiale de trémélimumab à la dose de 300 mg (anti-CTLA4) et des injections de durvalumab à la dose de 1500 mg (anti-PDL1) toutes les 4 semaines jusqu’à progression ou intolérance. Les patients inclus étaient en bon état général (OMS 0/1) avec une fonction hépatique préservée (CHILD A, 50 % ALBI 1). Contrairement à l’étude précédente, l’invasion tronculaire portale (VP4) était un critère d’exclusion. Une infection virale B ou C était présente dans 30 et 37 % des cas respectivement. L’étude est positive dans son objectif principal avec une amélioration significative de la survie globale (16,4 vs 13,8 mois, HR 0,78 (0,65-0,92)). Les taux de survie à 24 mois (40,5 % vs 32,6 %), 36 mois (30,7 vs 20,2 %) et 48 mois (25,2 vs 15,1 %) étaient également augmentés. La médiane de survie sans progression n’était pas différente entre les deux groupes. Le pourcentage d’effets indésirables de grade 3-4 était similaire dans les deux groupes (50 % pour le schéma Stride, 52,4% pour le sorafénib). Les taux de réponse étaient de 20,1% dans le bras bi-immunothérapie vs 5,1% dans le bras sorafénib. On note 35,8 % d’effets immunomédiés dont 12,7 % de grade 3-4 conduisant à un traitement par corticostéroïdes dans 20% des cas et un arrêt du traitement dans 5,7 % des cas. Aucun cas de rupture de varice œsophagienne n’a été rapporté pendant l’étude. Enfin, l’association durvalumab - trémélimumab était associée à une détérioration plus tardive de la qualité de vie. Le suivi au long court des patients de cette étude a permis de montrer qu’à 60 mois de l’inclusion, 19,6% des malades du bras STRIDE étaient encore en vie par rapport à 9,4 % dans le bras sorafénib (Rimassa L,Chan SL 2025).
L’association durvalumab-trémélimumab a obtenu une AMM en France en traitement supplémentaire de 1ère ligne chez les patients adultes atteints d'un CHC avancé ou non résécable, n’ayant pas reçu de traitement systémique antérieur, avec une fonction hépatique préservée (stade Child-Pugh A), un score ECOG 0 ou 1, et non éligibles aux traitements locorégionaux ou en échec à l’un d’eux.
Association ipilimumab-nivolumab
L’étude CHECKMATE 9DW publiée en 2025 (Yau T, Galle PR 2025) était un essai de phase 3, ouvert et randomisé, qui a inclus des patients atteints d'un carcinome hépatocellulaire non résécable sans thérapie systémique antérieure, avec un score de Child A et score OMS de 0 ou 1, et sans envahissement tronculaire de la veine porte. Les patients ont reçu nivolumab (1 mg/kg) plus ipilimumab (3 mg/kg) par voie intraveineuse toutes les 3 semaines jusqu'à un maximum de quatre doses, suivi de nivolumab 480 mg toutes les 4 semaines (335 patients) ou, au choix de l'investigateur, soit lenvatinib oral (8 mg ou 12 mg par jour selon le poids corporel) soit sorafénib oral (400 mg deux fois par jour (n=333). Le lenvatinib a été choisi dans 85 % des cas.
Un croisement précoce des courbes de Kaplan-Meier de la survie globale a reflété un nombre plus élevé de décès au cours des 6 premiers mois après la randomisation dans le bras nivolumab plus ipilimumab (hazard ratio 1,65 [IC à 95 % 1,12–2,43]) (11/18 décès reliés au traitement dans le bras immunothérapie versus 1 dans le bras ITK), mais a été suivi d'une séparation soutenue des courbes par la suite en faveur de nivolumab plus ipilimumab (HR 0,61 [0,48–0,77]). Après un suivi médian de 35,2 mois (IQR 31,1–39,9), la survie globale a été significativement améliorée avec nivolumab plus ipilimumab (médiane 23,7 mois [IC à 95 % 18,8–29,4] vs 20,6 mois [17,5–22,5] ; hazard ratio 0,79 [0,65–0,96] ; p =0,018) ; les taux de survie globale respectifs étaient de 49 % (IC à 95 % 44-55) versus 39 % (34-45) à 24 mois et de 38 % (32-43) versus 24 % (19-30) à 36 mois. Le taux de réponse selon RECIST 1.1 était de 36 % (dont 7 % de réponses complètes) dans le bras nivolumab-ipilimumab vs 13 % dans le bras sorafénib/lenvatinib. Des effets indésirables de grade 3-4 ont été observés dans 41 % des cas sous nivolumab-ipilimumab dont 29% ont nécessité une corticothérapie, et 42 % des cas dans le bras lenvatinib/sorafénib. L’association nivolumab-ipilimumab a obtenu l’AMM européenne, mais n’est pas encore remboursée en France dans cette indication à l’heure de l’écriture de ce référentiel.
Les inhibiteurs de tyrosine kinase
Sorafénib
L’essai randomisé de phase 3 SHARP (N inclus = 602), comparant sorafénib et placebo chez des malades atteints de CHC évolué, montrait un allongement significatif de la survie globale (médiane : 10,7 mois vs 7,9 mois) et de la survie sans progression (5,5 mois vs 2,8 mois) dans le bras sorafénib, mais sans amélioration de la survie sans progression clinique, et avec un taux de réponse tumorale faible selon les critères RECIST 1.1 % (réponses partielles : 2,3 %).
Des effets indésirables sévères (grade ≥3) étaient observés chez 8 % des malades traités (diarrhée et syndrome mains-pieds) (Llovet, Ricci et al. 2008). Des résultats identiques ont été constatés dans un essai de phase III avec les mêmes critères d’inclusion dans la zone Asie-Pacifique (Cheng, King et al. 2009).
A la suite de ces essais, le sorafénib (Nexavar®) a bénéficié d’une extension d’AMM en octobre 2007 avec le libellé « indiqué dans le traitement du carcinome hépatocellulaire ». Considérant cette indication comme insuffisamment précise, compte tenu des critères d’inclusion et des résultats de l’essai SHARP, un groupe de travail PRODIGE-AFEF a retenu comme indication du sorafénib (Nexavar®) : « Traitement palliatif du CHC non éligible pour un traitement spécifique (TH, résection chirurgicale, destruction per-cutanée, CE), ou en récidive après traitement spécifique, chez les malades en état général conservé (OMS 0 à 2) et Child-Pugh A » (Boige, Barbare et al. 2008). Cette recommandation a été reprise par la Commission de transparence de la HAS en 2008. Plus récemment l’étude de phase II prodige 21 comparant chez les patients CHILD B un traitement par sorafénib vs soins de support a confirmé l’absence de bénéfice d’un traitement par sorafénib en cas de cirrhose CHILD-Pugh B8/9 et un bénéfice modeste en cas de score B7 (Blanc, Khemissa 2021). Chez ces patients la décision de traitement par sorafénib doit être prise après discussion du rapport bénéfice/risque en tenant compte de l’état général du patient et des comorbidités.
Lenvatinib
Le lenvatinib (un inhibiteur des récepteurs 1 à 3 du VEGF, des récepteurs 1 à 4 du FGF, du récepteur α du PDGF, de RET et de KIT) a montré une efficacité équivalente à celle du sorafénib (Kudo, Finn 2018) dans une étude de phase III de non-infériorité chez des patients avec un CHC au stade B ou C de la classification BCLC, un stade A de Child-Pugh, et un indice ECOG PS ≤ 1. La SG médiane dans le bras lenvatinib était non inférieure à celle du bras sorafénib avec respectivement 13,6 vs 12,3mois (HR 0,92). La durée médiane du traitement était de 5,7 mois pour le lenvatinib et de 3,7 mois (0,1-38,7) pour le sorafénib. La survie sans progression médiane (7,4 vs 3,7 mois) était significativement augmentée dans le bras lenvatinib (HR 0.66, p<0.0001) ainsi que le taux de réponse objective selon les critères RECIST modifiés (24 % vs 9 %, p<0.0001). Les effets indésirables les plus courants pour le lenvatinib étaient l’hypertension (42 %), la diarrhée (39 %), la diminution de l'appétit (34 %), la perte de poids (31 %) et la fatigue (30 %). Le lenvatinib est donc une alternative au sorafénib en traitement de première ligne. Une extension d’AMM Européenne a été obtenue en 2018 mais le remboursement dans l’indication de CHC n’a pas été accordé en France.
Autres inhibiteurs de tyrosine kinase
D’autres inhibiteurs de tyrosine kinase ont été étudiés en traitement de première ligne du CHC en phase II et III sans efficacité supérieure ou équivalente à celle du sorafénib en phase II ou III, que ce soit en comparaison directe au sorafénib pour le sunitinib ou le brivanib (Johnson, Qin et al. 2013) ou en association avec une thérapie ciblée (erlotinib) ou une chimiothérapie (étude GONEXTt/PRODIGE 10).
Immunothérapie en monothérapie
Trois études de phase III randomisées ont évalué l’intérêt d’une immunothérapie en monothérapie versus sorafénib en traitement de première ligne de CHC chez des patients avec fonction hépatique préservée (CHILD A) et état général conservé (OMS 0-1).
- L’essai CheckMate 459 a étudié le nivolumab (anti-PD1) (Yau T, Park JW 2022). Cette étude de supériorité est négative dans son objectif principal avec une médiane de survie à 16.4 mois pour le bras nivolumab contre 14.7 mois pour le bras sorafénib (HR 0.85 (0.72-1.02), p=0.075). La survie sans progression n’était pas non plus significativement différente. Les taux de réponse étaient de 15 % dans le bras nivolumab vs 7 % sous sorafénib.
- L’essai HIMALAYA comportait un bras durvalumab en monothérapie (Anti-PDL1) comparé au sorafénib avec un objectif de non-infériorité (Abou-Alfa GK; Lau G 2022). Cette étude est positive sur son objectif principal en survie globale de 16,6 mois dans le bras durvalumab vs 13,8 mois (HR 0,86 (0,73-1,03)). Le taux de réponse était de 17 % vs 5.1 % pour le sorafénib. Les effets secondaires immunomédiés étaient moins fréquents qu’avec l’association durvalumab-trémélimumab 16,5 vs 35.8 %, dont 6,4 vs 12.6% de grade 3-4, 9,5 vs 20,1 % d’utilisation de corticoïdes et 2,6 vs 5,7 % d’arrêt de traitement.
- L’essai Rationale-301 étudiant le tislelizumab (anti-PD1) est positive pour son objectif principal de non-infériorité en survie globale (15,9 mois pour le tislelizumab vs 14,1 mois pour le sorafénib HR 0,85 (0,712-1,019)) (Qin S, Kudo M 2022). Le taux de réponse sous tislelizumab était de 14,3 % vs 5,4 % sous sorafénib. On notait 17 % d’effets indésirables immunomédiés dont 12 % ayant nécessité un traitement par corticoïdes.
Combinaison d’immunothérapie et d’inhibiteurs de tyrosine-kinases
Plusieurs études de phase III ont comparé l’association d’inhibiteurs de tyrosine kinase et d’immunothérapie vs sorafénib ou lenvatinib en première ligne chez des patients en bon état général (OMS 0-1) et avec une fonction hépatique préservée (CHILD A).)
- Cabozantinib-atézolizumab (COSMIC 312). Cette étude de phase III a inclus 432 patients traités par cabozantinib (40 mg/j) et atézolizumab 1200 mg IV toutes les trois semaines et 217 patients traités par sorafénib avec un co-objectif principal : survie globale et survie sans progression (Kelley RK, Rimassa L 2022). La survie sans progression était améliorée dans le bras cabozantinib-atézolizumab (6,8 vs 4,2 mois HR 0,63 (0,44-0,91)) ainsi que le taux de réponse (13 % vs 5 %) mais sans bénéfice en survie globale (15,4 vs 15,5 mois HR 0,90 (0,69-1,18)). Les effets secondaires de grade 3-4 étaient plus fréquents dans le groupe atézolizumab-cabozantinib (64 % vs 46 %).
- Lenvatinib-pembrolizumab (LEAP 002). Après une étude de phase I encourageante cette association (lenvatinib 8 ou 12 mg selon le poids – pembrolizumab 200 mg toutes les 3 semaines) a été comparée chez 295 patients au lenvatinib (8 ou 12 mg selon le poids) en monothérapie (399 patients). Même si les résultats de la phase I ont été confirmés avec une médiane de survie supérieure à 20 mois dans le bras lenvatinib -pembrolizumab (21,2 mois), cette étude est négative, avec une médiane de survie élevée dans le bras lenvatinib (19 mois, HR 0,84 (0,708-0,997, p= 0,0227 pour un seuil de significativité à 0,0185). La survie sans progression n’était pas non plus significativement améliorée. Le taux de réponse selon les critères RECIST était de 26,1 % pour la combinaison vs 17,5 % pour le lenvatinib. Le taux d’effets secondaires de grade 3-5 était de 62,2 % pour la combinaison vs 57,5 % pour le lenvatinib.
- Rivoceranib-camrelizumab. Cette étude comportant une majorité de patients asiatiques (82,7 %) avec infection virale B (75 %) a comparé l’association rivoceranib (inhibiteur et tyrosine kinase plus spécifique du VEGFR2, donné à 250 mg/j) et camrelizumab (anti-PD1 200 mg toutes les 2 semaines) au sorafénib (Qin S, Chan LS 2022). L’étude est positive pour ses 2 co-objectifs principaux : la survie sans progression (5,6 vs 3,7 mois HR 0,52 (0,41-0,65) p < 0,0001) et la survie globale (22,1 mois vs 15,2 mois HR 0,62 (0,49-0,8) p < 0,0001). Les taux de réponse étaient de 25,4 % pour la combinaison vs 5,9% pour le sorafénib selon les critères RECIST 1.1. Les effets secondaires de grade 3-4 étaient plus fréquents avec la combinaison (80,5 % vs 52 %). La transposabilité de ces résultats à la population non asiatique reste cependant incertaine.
Traitement de seconde ligne
Après échec d’une première ligne comportant une immunothérapie
La séquence thérapeutique optimale pour les patients atteints de CHC avancé reste à définir. Bien qu’il existe un besoin croissant de recommandations claires, l’absence d’étude randomisée rend difficile l’établissement de celles-ci.
La prescription d’un ITK en seconde ligne est une option proposée par la plupart des sociétés savantes. Une étude de phase 2 évaluant le cabozantinib (Chan SL, Ryoo BY 2024) en deuxième ligne après traitement basé sur l’immunothérapie, a montré une SSP médiane de 4,4 mois et une SG médiane de 9,9 mois, résultats proches de ceux rapportés après sorafénib. Une seconde étude de phase 2 utilisant le lenvatinib (n=50) rapporte un taux de réponse de 14%, une médiane de SG de 9,8 mois (Kim HD, Sym J 2025). Ces observations nécessitent toutefois confirmation dans des essais de plus grande ampleur pour confirmer le choix de ITK après immunothérapie. D’autres études de cohortes rétrospectives doivent être interprétées avec prudence mais montrent dans l’ensemble des taux de réponses et des survie globales similaires à celles observées avec des TKI en première ligne suggérant que la première ligne d’immunothérapie n’impacte pas défavorablement l’efficacité des TKI.
Le tableau ci-dessous synthétise les publications disponibles (études de phase II ou de cohorte) d’utilisation de TKI après atezolizumab et bevacizumab.
N | TKI | RR | SSP | SG | |
|---|---|---|---|---|---|
| Yano S et al. 2023 | 24 | Lenvatinib | 33 % | 4 | 15,3 |
| Persano et al. 2023 | 84 | Lenvatinib |
|
| 17 |
| Marell et al. 2024 | 62 | Lenvatinib |
|
| 10,7 |
| Hirakoa A, 2023 | 101 | Lenvatinib | 15,40 % | 4,4 | 15,7 |
| Chen YH et al. 2023 | 14 | Lenvatinib | 21 % | 6,7 | 10,5 |
| Yoo C et al. 2021 | 19 | Lenvatinib | 15,80 % | 6,1 | 16,6 |
| Muto H et al. 2023 | 20 | Lenvatinib | 25 % | 6 | 10,5 |
| Mohri K et al 2024 | 21 | Lenvatinib | 45 % | 3,5 | 24,2 |
| Falette-Puisieux et al. 2023 | 8 | Lenvatinib |
| 4,4 | 5,7 |
| Cheon J et al. 2025 | 56 | Lenvatinib | 12 % | 4,9 | 13,2 |
| Persano et al. 2024 | 160 | Lenvatinib | 26 % | 3,5 | 18,9 |
| Lee et al. 2024 | 154 | Lenvatinib | 6 % | 4 | 8 |
| Persano et al. 2023 | 43 | Sorafénib |
|
| 14,2 |
| Yoo C et al. 2021 | 29 | Sorafénib | 0 % | 2,5 | 11,2 |
| Falette-Puisieux et al. 2023 | 41 | Sorafénib |
| 2,6 | 7 |
| Cheon J et al. 2025 | 67 | Sorafénib | 8 % | 3,3 | 11,5 |
| Tovoli et al. 2024 | 54 | Sorafénib | 0 % | 3,3 | 6,9 |
| Persano et al. 2024 | 95 | Sorafénib | 20 % | 4,3 | 14,3 |
| Lee et al. 2024 | 324 | Sorafénib | 4,5 % | 2,3 | 6,3 |
| Falette-Puisieux et al. 2023 | 29 | Régorafénib |
| 2,6 | 15,8 |
| Lee et al. 2024 | 36 | Régorafénib | 11,4 % | 3,6 |
|
| Persano et al. 2023 | 23 | Cabozantinib |
|
| 12,4 |
| Marell et al. 2024 | 10 | Cabozantinib |
|
| 12,8 |
| Lee et al. 2024 | 12 | Cabozantinib | 0 % | 5,4 | 11,2 |
| Falette-Puisieux et al. 2023 | 4 | Cabozantinib |
| 2,8 | 9,2 |
Trois études rétrospectives ont évalué l’intérêt d’une seconde immunothérapie après échec d’une première ligne comportant soit un anti-PD1/PD-L1L1PDL1 seul, soit une association atezolizumab-bevacizumab (Wong JSL, Kwok GGW 2021 ; Scheiner B, Roessler D 2022 ; Alden SL, Lim M 2023). Les faibles effectifs et l’hétérogénéité des traitements reçus doivent rendre prudent dans l’interprétation de ces données. Néanmoins, une seconde ligne d’immunothérapie comportant une classe thérapeutique absente en première ligne (anti-CTLA4 ou anti VEGF) semble associée à des taux de réponse tumorale significatifs (16 à 26 %; y compris chez des patients ayant progressé d’emblée en première ligne) et des survies globales de 6 à plus de 14 mois. Les données de tolérance étaient sensiblement analogues à celles rapportées en première ligne d’immunothérapie. Des patients ayant présenté des effets secondaires immuno-médiés en première ligne ont pu recevoir une seconde ligne d’immunothérapie sans sur-toxicité manifeste.
Le tableau ci-dessous regroupe les données disponibles d’utilisation d’immunothérapie après première ligne par atezolizumab et bevacizumab.
1ère ligne | N | Combinaison | RR | SSP | SG | |
|---|---|---|---|---|---|---|
| Mori N et al. 2024 | Atezo-beva | (85) | Durva-treme | 5 % | 2,35 | |
| Miura R et al. 2024 | Atezo-beva | 16 | Durva-treme | 0 % |
| |
| Sho T et al. 2022 | Atezo-beva | 25 | Durva-treme | 14 % |
| |
| Rossler D et al. 2022 | AB 7 Nivo-lenva 3 | 10 | Nivo-ipi | 30 % | 2,9 | 7,4 |
| Lim JS et al. 2024 | Atezo-beva | 49 | Nivo-ipi | 15 % | 1,4 | 5,8 |
| Lee et. al 2024 | Atezo-beva | 50 | ICI + TKI | 13 % | 5,4 | 12,6 |
| El Khoureiry et al. 2024 | Atezo-beva | 68 | Rego-Pembro | 6 % | 2,8 | NE > 14 |
Après échec d’une première ligne par ITK
Plusieurs essais cliniques de phase II et III ont évalué l’intérêt d’un traitement de seconde ligne après échec (ou intolérance) du sorafénib. Ces études ont testé - contre placebo - des inhibiteurs de tyrosine kinase ciblant les voies du VEGF, de l’EGF et c-met, des anticorps monoclonaux (anti-VEGF) et des immunothérapies. A ce jour, quatre études de phase III sont positives après échec (progression ou intolérance) du sorafénib.
Régorafénib
L’étude RESORCE (Bruix, Qin et al. 2017) randomisée contre placebo, en double aveugle a montré une efficacité du régorafenib (un inhibiteur de VEGFR1-3, c-Kit, TIE-2, PDGFR-β, FGFR-1, RAF-1, BRAF, p38) à la dose de 160 mg/jour trois semaines sur quatre, chez des patients CHILD A après progression sous sorafénib. Le régorafenib augmente significativement la survie globale par rapport au placebo (10,6 versus 7,8 mois). Les principaux effets indésirables sont représentés par l’hypertension artérielle le syndrome pied-main et la diarrhée. Le régorafenib est donc un traitement validé de seconde ligne après échec du sorafénib chez des patients ayant une fonction hépatique préservée (CHILD A) et sans intolérance préalable au sorafénib.
Cabozantinib
Les résultats de l’étude CELESTIAL (Abou-Alfa, Meyer, 2018) de phase III randomisée et randomisée en double aveugle comparant le cabozantinib au placebo en deuxième ou troisième ligne ont été publiés en juillet 2018. Les patients en bon état (PS 0-1), présentant une fonction hépatique préservée (CHILD A) et un échec (progression ou intolérance) sous sorafénib ont été inclus. La survie globale médiane était de 10,2 mois avec le cabozantinib contre 8 mois avec le placebo (HR 0,76). La survie sans progression était de 5,2 mois avec le cabozantinib comparativement à 1,9 mois avec le placebo (HR 0,44). Les principaux effets indésirables sont représentés par le syndrome pied-main, la diarrhée, l’hypertension artérielle et l’asthénie. Le cabozantinib peut donc être utilisé en traitement de seconde ligne après échec du sorafénib (progression ou intolérance).
Ramucirumab
Le ramucirumab est un anticorps humanisé inhibant l’activation des ligands du récepteur VEGF-2, testé dans le traitement de deuxième ligne du CHC dans une étude de phase III randomisée versus placebo (étude REACH) (Zhu, Park et al. 2015). Bien que la survie globale médiane n’était pas augmentée de façon significative par rapport au placebo (9,2 vs 7,6 mois), un bénéfice significatif était observé dans le sous-groupe prédéfini de patients présentant une AFP > 400 ng /ml. Une deuxième étude de phase III (REACH-2) spécifiquement dédiée aux patients présentant une AFP > 400 a donc été conduite (Zhu, Kang, 2019) et a montré une amélioration significative de ; la survie globale (SG médiane de 8,5 vs 7,3 mois ; HR 0,710) et de la survie sans progression avec le ramucirumab. L’analyse poolée des études REACH2 et REACH (avec patients ayant une AFP > 400) confirment ces résultats (Zhu, Finn 2018) et montrent que le profil de tolérance du ramucirumab semble être meilleur que celui des inhibiteurs de la tyrosine kinase avec un délai avant détérioration clinique augmenté chez les patients recevant le ramucirumab (Zhu, Finn 2018). Le ramucirumab n’a pas reçu d’extension d’AMM en France.
Apatinib
Cet inhibiteur du VEGF-R2 a été étudié à la dose de 750 mg/j en phase III versus placebo réalisée en Chine en seconde ligne (après échec du sorafénib ou de traitements à base d’oxaliplatine) chez des patients CHILD ≤ ouB7. La survie médiane était significativement allongée dans le bras apatinib (8,7 vs 6,8 mois, HR 0,785 p=0,0476) (Li, Quin et al 2020). Il n’existe pas de données sur l’efficacité de ce traitement dans une population occidentale.
Pembrolizumab
L’intérêt du pembrolizumab après échec du sorafénib a été évalué versus placebo dans deux études de phase III randomisées : une en population majoritairement non asiatique à 75% (Finn RS, Ryoo BY 2020) et une en population asiatique (Qin S, Chen Z 2022).
La première étude est négative pour son objectif principal avec une médiane de survie de 13,,9 mois pour le pembrolizumab versus 10,6 mois pour le placebo (HR 0,78 (0,611-0,998). La survie sans progression était de 3 mois pour le pembrolizumab vs 2,,8 mois pour le placebo et le taux de réponse de 18,4 % vs 4,4 % pour le placebo. L’étude en population asiatique est par contre positive avec une amélioration significative de la survie globale (14,6 vs 13,0 mois ; HR 0,79 (0,63-0,99) p = 0,0180) et de la survie sans progression (2,6 vs 2,3 mois ; HR 0,74; (0,60-0,92) p = 0,0032). Le taux de réponse était de 12,7 % vs 1,3 % dans le groupe placebo.
Traitement systémique en cas de cirrhose CHILD B
Les patients avec fonction hépatique Child B représentent 20-25 % des patients traités pour un carcinome hépatocellulaire (CHC) avancé, mais sont exclus des essais cliniques de phase 3 en raison de leur pronostic plus réservé et du risque accru d’effets indésirables.
Le traitement par inhibiteur de tyrosine kinase de type sorafénib semble faisable sans augmentation significative des effets indésirables, mais avec une survie globalement plus faible par rapport à la population Child A. Une étude (PRODIGE 21) a comparé sorafénib, pravastatine, leur association, et les soins de support, chez des patients avec cirrhose CHILD B sans différence notable en terme de progression ou de survie globale, bien que certains résultats suggèrent un bénéfice potentiel du sorafénib chez les patients Child-Pugh B7 ou ALBI grade 1 ou 2 (médiane de survie globale de 6,5 mois vs 3,0 mois pour Child-Pugh B7 vs B8-9 et 6,1 mois vs 3,1 mois pour ALBI grade 1 ou 2 vs grade 3). ( Blanc JF, Khemissa F 2021).
Pour l’immunothérapie, les données rétrospectives indiquent une faisabilité avec une survie plus faible, un taux de réponse d’environ 14 % et une médiane de survie globale autour de 5,5 mois. La cohorte du nivolumab dans l’étude Checkmate-040 a montré une réponse de 12 % et une médiane de survie globale de 7,6 mois, avec un profil de tolérance acceptable. Cependant, il n’existe pas encore d’études prospectives sur les associations d’immunothérapies dans cette population.
7.3.3. Indications thérapeutiques
7.3.3.1. CHC sur cirrhose
La discussion se fait à partir de 2 critères principaux, l’extension tumorale et l’état anatomique et fonctionnel du foie non tumoral. D’autre part, les indications de résection, destruction per-cutanée et traitements loco-régionaux sont limitées aux malades en bon état général (OMS 0-1) et celles des traitements systémiques aux malades en état général « conservé » (OMS ≤ 2). Un diagramme d’aide à la décision thérapeutique prenant en compte ces différents paramètres est proposé.
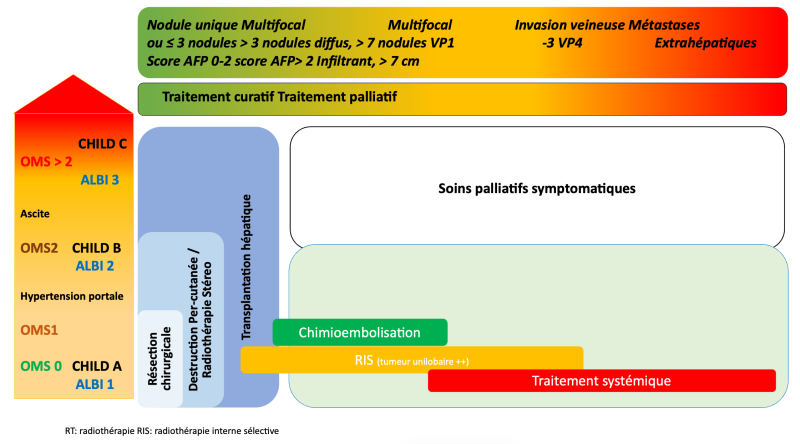
En pratique, en RCP, la stratégie thérapeutique est orientée par le bilan d’extension et le score de CHILD.
Trois situations sont schématiquement possibles :
- CHC sans extension vasculaire ou extra-hépatique avec un score AFP< 2 et/ou entrant dans les classiques critères de Milan (« petits CHC ») : un traitement curatif doit être envisagé de principe. Le choix du traitement est influencé par le score de CHILD.
- En cas d’extension vasculaire macroscopique segmentaire ou tronculaire et/ou d’extension extra-hépatique un traitement palliatif doit être envisagé et discuté selon le score de CHILD et le statut de performance OMS. Cependant, compte-tenu des traitements disponibles (SIRT en cas d’invasion vasculaire, immunothérapie) associés à des taux de réponse supérieurs à 30%, un down-staging vers une situation curative peut être obtenu et les dossiers doivent dans ce cas être re-discutés en RCP.
- Dans certains cas, chez les malades Child-Pugh A, l’option curative ou palliative peut ne pas être évidente et justifier la discussion du dossier en RCP de recours afin de bénéficier, en particulier, de l’expertise d’équipes de transplantation, et de radiologie interventionnelle (niveau de recommandation : accord d’experts). Il s’agit par exemple des patients avec nodule unique volumineux relevant éventuellement d’une résection ou d’un traitement endovasculaire, ou de malades avec CHC multifocal au-delà des critères de transplantation mais pouvant bénéficier d’une stratégie de down-staging.
7.3.3.1.1. CHC accessible à un traitement curatif
Il s’agit des CHC qui sont potentiellement éligibles à une transplantation hépatique (d’emblée ou après down-staging efficace), définis par un score AFP ≤ 2 et incluant le groupe des CHC entrant dans les critères de Milan.
7.3.3.1.1.1. Cirrhose Child-Pugh A
Recherche de contre-indication à la transplantation hépatique (TH) : âge > 70 ans, métastase extra-hépatique y compris ganglionnaire, comorbidités contre-indiquant la transplantation, infection VIH non contrôlée, obstruction portale néoplasique, refus ou non compliance du patient.
7.3.3.1.1.1.1. En l'absence de contre-indication à la TH :
REFERENCES
- Référer à un centre de transplantation (niveau de recommandation : grade B).
- Discussion d’un traitement local ou loco-régional dit d’attente (résection hépatique, destruction per-cutanée, chimioembolisation, radiothérapie interne sélective)). Selon les équipes, trois OPTIONS peuvent être discutées :
a) mise sur liste sans traitement d’attente si le délai d’attente prévisible est court
b) traitement local et inscription sur liste d’attente
c) traitement local à visée curative (destruction per-cutanée ou résection), puis transplantation « de sauvetage » discutée en cas de récidive, option à privilégier en cas de CHC inférieur à 2-3 cm de diamètre. La stratégie thérapeutique doit être d’emblée discutée avec le centre de transplantation (niveau de recommandation : grade C).
7.3.3.1.1.1.2. En présence de contre-indication à la TH :
REFERENCES
- Discussion entre résection et destruction per-cutanée (niveau de recommandation : grade B).
- En cas de contre-indication à la résection ou à une destruction per-cutanée, discussion de radiothérapie stéréotaxique dans un centre régional de référence (niveau de recommandation : grade B) ou de chimioembolisation hypersélective (avis d’experts) ou de radiothérapie interne sélective (niveau de recommandation : grade C).

(aucun critère n’est en lui-même décisif)
Traitement néo-adjuvant ou adjuvant après résection ou radiofréquence :
REFERENCES
- Pas de traitement néo-adjuvant hors essai clinique (niveau de recommandation : grade A).
- Pas de traitement adjuvant recommandé à ce jour (niveau de recommandation : grade A).
- Prise en charge de l’hépatopathie chronique : arrêt de l’alcool, contrôle du VHB, éradication du VHC en cas de traitement curatif (discutable en cas de traitement palliatif du CHC)…
- Prise en charge des comorbidités : alcool, surpoids, diabète…
- En cas de cirrhose, recherche d’une hypertension portale cliniquement significative et mise en place si nécessaire d’un traitement par carvedilol.
ESSAIS CLINIQUES
- AB-LATE 02 : Atézolizumab neoadjuvant et atézolizumab + bévacizumab en adjuvant après ablation percutanée par radiofréquence de CHC : essai de phase II randomisé multicentrique. Coordonnateurs : Boris Guiu/Eric Assenat (Montpellier)
- La liste des essais de traitement adjuvant est disponible sur le site de l’INCa :
https://www.e-cancer.fr/Professionnels-de-sante/Le-registre-des-essais-cliniques/Le-registre-des-essais-cliniques
7.3.3.1.1.2. Cirrhose Child-Pugh B et C
REFERENCES
- Transplantation hépatique (TH) pour cirrhose grave, à discuter avec un centre de référence (niveau de recommandation : grade C).
- Si contre-indication à la TH : destruction per-cutanée pour les malades avec un score ≤ 7 de Child-Pugh ≤ B7 en l’absence d’ascite importante (niveau de recommandation : grade C).
- Lorsqu’un traitement étiologique est possible (sevrage alcoolique, éradication virale C, contrôle de la réplication virale B…), la cirrhose peut s’améliorer et la discussion thérapeutique vis-à-vis du CHC peut être réévaluée.
7.3.3.1.2. CHC non accessible à un traitement curatif
7.3.3.1.2.1. Cirrhose Child-Pugh A
7.3.3.1.2.1.1 CHC sans extension extra-hépatique ni envahissement portal tronculaire (VP4) avec fonction hépatique préservée, OMS 0-2
REFERENCE
- Traitement endovasculaire : chimio-embolisation artérielle ou radiothérapie interne sélective (SIRT) (niveau de recommandation : grade A). Le choix entre les deux traitements peut être orienté en prenant en compte les critères indiqués dans le tableau ci-dessous (niveau de recommandation : grade B).
Critères influençant la discussion entre chimio-embolisation ou radiothérapie interne sélective | ||
| Chimio-embolisation | Radiothérapie interne sélective | |
| Invasion macrovasculaire | Non | Possible en cas d’invasion Vp1 à Vp3 ou de thrombose des veines hépatiques |
| Taille maximale des nodules | < 7 – 10 cm | Pas de taille maximale, selon étude dosimétrique et réserve hépatique |
| Distribution des nodules | Possible si bilobaire ; si approche sélective possible | Unilobaire, avec réserve hépatique > 30 % |
| Caractère infiltrant | Non | Possible |
OPTIONS
- Certaines caractéristiques tumorales (atteinte ne permettant ni CEL ni SIRT (distribution bilobaire pour la SIRT, taille tumorale >7cm pour la CEL, nombre de nodules >7…)), caractère infiltrant / hypovasculaire) limitent le bénéfice des traitements intra-artériels. Ces patients pourraient être orientés préférentiellement vers des traitements systémiques (avis d’expert) ou vers les essais cliniques dédiés. ( https://www.e-cancer.fr/Professionnels-de-sante/Le-registre-des-essais-cliniques/Le-registre-des-essais-cliniques)
- En cas d’échec de chimioembolisation/ SIRT, pour des raisons techniques (sténose du tronc coeliaque ou de l’artère hépatique, Shunts vasculaires), work up négatif (Dosimétrie, réserve hépatique, shunt pulmonaire) un traitement systémique est indiqué. (niveau de recommandation grade A)
7.3.3.1.2.1.2. CHC avec invasion vasculaire portale tronculaire (VP4) ou extra-hépatique ou en échec de la chimio-embolisation chez un patient à l’état général conservé (OMS ≤ 2) avec une fonction hépatique préservée
Traitement de première ligne
REFERENCES
- Atézolizumab (1200 mg) et bévacizumab (15 mg/kg) toutes les 3 semaines (niveau de recommandation : grade A).
- Trémélimumab 300 mg J1 - durvalumab 1500 mg toutes les 4 semaines (niveau de recommandation : grade A).
- Nivolumab (1 mg/kg) et ipilimumab (3 mg/kg) par voie intraveineuse toutes les 3 semaines quatre fois, suivi de nivolumab 480 mg toutes les 4 semaines (pas de remboursement en France dans cette indication en 2025) (niveau de recommandation : grade A).
- Si contre-indication ou sur-risque hémorragique, rénal, cardiovasculaire pressenti sous bévacizumab, privilégier l’association tremelimumab-durvalumab
Si contre-indication à l’immunothérapie
- Sorafénib : 800 mg par jour en deux prises en continu (niveau de recommandation : grade A).
- Lenvatinib : 12 mg par jour si > 60 kg et 8 mg par jour si poids < 60 kg (niveau de recommandation : grade A / en attente de remboursement). Son utilisation en cas d’intolérance (toxicité grade 3-4) non contrôlable précoce au sorafénib pourra être discutée.
OPTION
- En cas de d’atteinte hépatique prédominante et d’extension extra-hépatique non menaçante (micro-nodule pulmonaire, adénomégalies < 15 mm.) un traitement loco-régional hépatique peut être discuté (avis d’experts).
ESSAIS CLINIQUES
La liste des essais cliniques disponibles en traitement de première ligne est disponible sur le site de l’INCa :
https://www.e-cancer.fr/Professionnels-de-sante/Le-registre-des-essais-cliniques/Le-registre-des-essais-cliniques
- PRODIGE 81 - (FFCD 2101) - TRIPLET CHC : Etude évaluant l’intérêt de l’ajout de l’Ipilimumab à la combinaison Atézolizumab-Bévacizumab chez des patients atteints d’un carcinome hépatocellulaire en première ligne de traitement systémique. Coordonnateur : P Merle (Lyon)
https://ramdam.ffcd.fr/CUSTOM/GED/20230104/24498_160448.pdf - http://hector-essais-cliniques.fr/essais-clinique/2994
- TERTIO : Evaluation of the Interest to Combine a CD4 Th1-inducer Cancer Vaccine Derived From Telomerase and Atézolizumab Plus Bévacizumab in Unresectable Hepatocellular Carcinoma (Phase II). Coordonnateur : C Borg (CHU Besancon)
http://hector-essais-cliniques.fr/essais-clinique/2853
Traitement de deuxième ligne
REFERENCES
Après traitement par sorafénib :
- Régorafenib à 160mg/jour trois semaines sur 4 (niveau de recommandation : grade A) : chez des patients ayant une fonction hépatique préservée (CHILD A), un index OMS <2, progressifs (et non intolérants) sous sorafénib.
- Cabozantinib : 60 mg/jour en continu (niveau de recommandation : grade A). Le cabozantinib peut être utilisé après échec du sorafénib en deuxième ou troisième ligne et chez les patients intolérants au sorafénib.
OPTIONS
Après traitement par immunothérapie en première ligne :
- Inhibiteur de tyrosine kinases : sorafénib, lenvatinib, regorafénib, cabozantinib (avis d’experts).
- Immunothérapie selon un autre schéma que la première ligne (avis d’experts).
ESSAIS CLINIQUES
La liste des essais cliniques disponibles en traitement de seconde ligne est disponible sur le site de l’INCa :
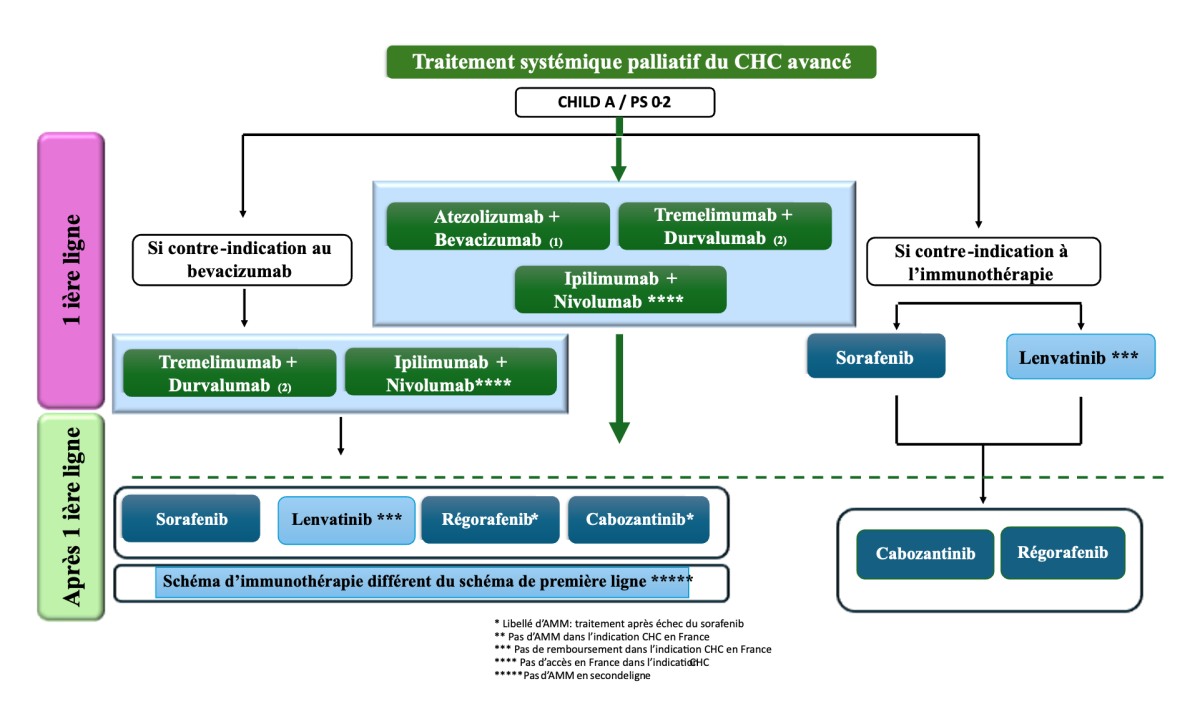
7.3.3.1.2.2. Cirrhose Child-Pugh B ou C
REFERENCE
- Traitement symptomatique (niveau de recommandation : grade C).
OPTION
- Traitement systémique (Immunothérapie ou inhibiteur de tyrosine kinase) à discuter chez les patients en bon état général (OMS 0-2) CHILD B7 ou CHILD B avec score ALBI 1-2. (niveau de recommandation : avis d’experts).
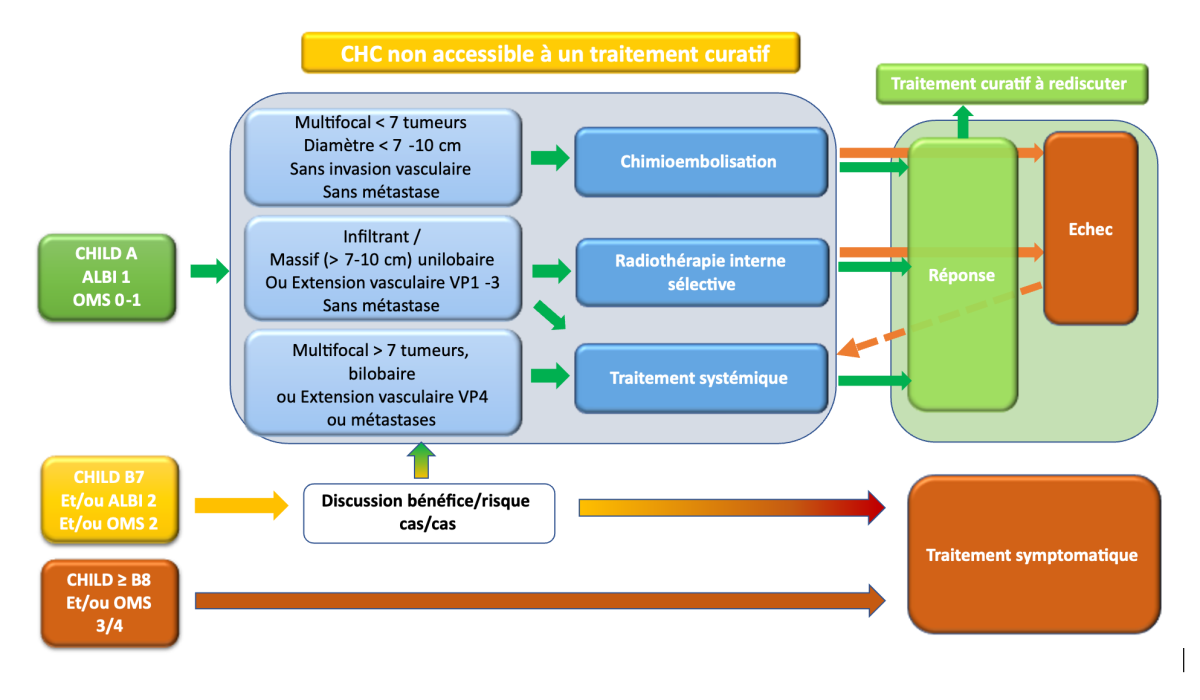
7.3.3.2. CHC sur foie non cirrhotique
REFERENCE
- Résection (niveau de recommandation : grade C) Les indications sont plus larges que lorsqu’il existe une cirrhose. L’examen histologique du foie non tumoral est donc indispensable et doit être disponible au moment de la discussion en RCP. La résection donne de bons résultats lorsqu’il n’y a pas d’envahissement portal.
OPTIONS
- Si une résection n’est pas retenue, la discussion des autres traitements se fait selon les mêmes critères que lorsqu’il existe une cirrhose (niveau de recommandation : accord d’experts).

